1 . 氧气是一种极具发展潜力的清洁高效的二次能源,其生产和储存是科学研究的重要方向。日前制氢的方法主要有化石能源制氢和电解水制氢。氢气的储存有物理储氢和化学储氢。物理储氢包括加压储氢和吸附储氢。由化石能源制得的 中含有
中含有 ,利用液氮的低温可将
,利用液氮的低温可将 液化分离,从而获得纯净的氢气。储氢、释氢、用氢过程中涉及的部分物质转化如图1所示:
液化分离,从而获得纯净的氢气。储氢、释氢、用氢过程中涉及的部分物质转化如图1所示: 与
与 分离,说明氢气的沸点比
分离,说明氢气的沸点比 的沸点
的沸点___________ 。
(2)物理储氢:高压气态储氢是广泛应用的储氢技术,即通过高压将氢气液化至氢瓶中加以储存。高压将氢气液化过程中,发生的改变是___________ (从微观角度解释)。该技术的优点在于其充装释放氢气速度快,但其缺点是___________ 。
(3)化学储氢:图2表示 和
和 在
在 和
和 的催化下,实现
的催化下,实现 的再利用和储氢的原理。图示中生成的
的再利用和储氢的原理。图示中生成的 与
与 的质量比为
的质量比为___________ 。___________ 。
 中含有
中含有 ,利用液氮的低温可将
,利用液氮的低温可将 液化分离,从而获得纯净的氢气。储氢、释氢、用氢过程中涉及的部分物质转化如图1所示:
液化分离,从而获得纯净的氢气。储氢、释氢、用氢过程中涉及的部分物质转化如图1所示: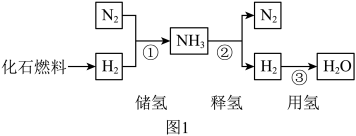
 与
与 分离,说明氢气的沸点比
分离,说明氢气的沸点比 的沸点
的沸点(2)物理储氢:高压气态储氢是广泛应用的储氢技术,即通过高压将氢气液化至氢瓶中加以储存。高压将氢气液化过程中,发生的改变是
(3)化学储氢:图2表示
 和
和 在
在 和
和 的催化下,实现
的催化下,实现 的再利用和储氢的原理。图示中生成的
的再利用和储氢的原理。图示中生成的 与
与 的质量比为
的质量比为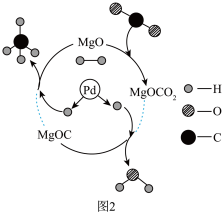
您最近一年使用:0次
2 . 区分下列各组物质的方法错误的是
| 选项 | 需区分的物质 | 方法 |
| A | 一氧化碳和氢气 | 点燃,火焰上方罩干冷烧杯 |
| B | 木炭粉和二氧化锰 | 放在石棉网上灼烧 |
| C | CuSO4溶液和FeSO4溶液 | 观察溶液的颜色 |
| D | 二氧化碳和氮气 | 用燃着的小木条 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 下列实验现象记录正确的是
| A.氢气还原氧化铜:紫红色固体变成黑色,试管口有水生成 |
| B.镁条在空气中燃烧:火星四射,生成黑色固体,放热 |
| C.电解水的实验现象:一段时间后正负极收集到的气体质量比约为1:8 |
| D.硫在氧气中燃烧:产生明亮的蓝紫色火焰,放热 |
您最近一年使用:0次
解题方法
4 . 化学让世界更加绚丽多彩。“化”取自“变化”之意,以下四种变化与其他三种有本质不同的是
| A.分离液态空气制取氧气 | B.燃烧氢气获得能量 |
| C.石油通过分馏得到汽油 | D.蒸发海水获得粗盐 |
您最近一年使用:0次
5 . 氢能是公认的高热值清洁能源。学习小组查得资料:
材料1.目前氢气的来源如图1所示。研究发现高温下水会发生热分解获得氢气,高温下水分解体系中微粒含量与温度的关系如图2所示。
材料2.氢气易燃易爆,不易储存和运输。一种镁铜合金可用于储氢。______ 。
(2)写出高温下水热分解获得氢气的化学方程式______ 。
(3)图中曲线A、B对应的微粒依次是______ 、______ (用化学符号表示)。
(4)氢气易燃易爆,点燃前一定要______ ,氢能是公认的清洁能源的原因______ 。
(5)将镁、铜单质按比例在一定温度下熔炼可得镁铜合金。熔炼时通入氩气的目的是______ 。
材料1.目前氢气的来源如图1所示。研究发现高温下水会发生热分解获得氢气,高温下水分解体系中微粒含量与温度的关系如图2所示。
材料2.氢气易燃易爆,不易储存和运输。一种镁铜合金可用于储氢。
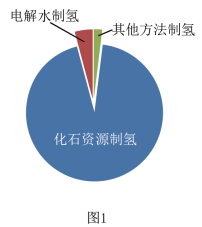

(2)写出高温下水热分解获得氢气的化学方程式
(3)图中曲线A、B对应的微粒依次是
(4)氢气易燃易爆,点燃前一定要
(5)将镁、铜单质按比例在一定温度下熔炼可得镁铜合金。熔炼时通入氩气的目的是
您最近一年使用:0次
名校
解题方法
6 . 下列实验现象描述正确的是
| A.点燃镁条:银白色固体燃烧、放热、产生白雾 |
| B.木炭在氧气中燃烧:黑色固体燃烧发红光,放热 |
| C.氢气与氧化铜反应:黑色固体变成光亮紫红色固体,试管口有水珠生成 |
| D.铁钉与硫酸铜溶液混合:银白色固体表面产生紫红色的铜,溶液由无色变成浅绿色 |
您最近一年使用:0次
7 . 2024年3月20日,我国探月工程四期“鹊桥二号”中继星发射成功。
(1)长征八号遥三运载火箭成功将“鹊桥二号”中继星送入地月转移轨道,它的推进剂为液氢和液氧,在点燃条件下两者发生反应的化学方程式为_______ 。
(2)月球车上的太阳能电池板使用的材料是硅。下图是工业制取高纯硅的反应微观示意图,参加反应的甲、乙微粒个数比为_______ 。_______ (填“氮肥”、“磷肥”或“钾肥”)的原料。
(1)长征八号遥三运载火箭成功将“鹊桥二号”中继星送入地月转移轨道,它的推进剂为液氢和液氧,在点燃条件下两者发生反应的化学方程式为
(2)月球车上的太阳能电池板使用的材料是硅。下图是工业制取高纯硅的反应微观示意图,参加反应的甲、乙微粒个数比为
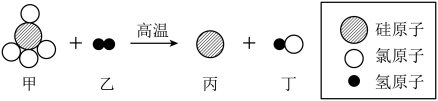
您最近一年使用:0次
8 . 纳米零价铁在环保领域应用广泛。
I.制备纳米铁粉
(1)已知氢气与菱铁矿(主要成分为 )在高温条件下反应能得到铁、水及二氧化碳,请写出化学反应方程式
)在高温条件下反应能得到铁、水及二氧化碳,请写出化学反应方程式_____ 。
Ⅱ.探究所得固体成分
【提出问题】氢气与碳酸亚铁反应后剩余固体的成分是什么?
【做出猜想】
(2)猜想一: 猜想二:
猜想二: 猜想三:
猜想三:_____ 。
【查阅资料】
①氢气具有还原性,能够冶炼金属。
②无水硫酸铜是一种白色固体,遇水会变为蓝色。
【实验探究】某学习小组利用如图1所示装置,对剩余固体成分(杂质不与稀硫酸反应)进行探究,实验操作及现象如下。回答下列问题。_____ 。
(4)向装置A中加入稀硫酸后,A中产生气泡且溶液变为浅绿色,甲同学判断猜想一正确,乙同学认为甲的判断不合理,理由是_____ 。
(5)观察到装置B中澄清石灰水变浑浊,D中_____ (填实验现象),E中固体变蓝。
【实验结论】综上所述,猜想三正确。
【反思交流】
(6)若去掉装置E_____ (填“能”或“不能”)证明固体中含有 。
。
Ⅱ.处理水体中的氮、磷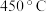 或者
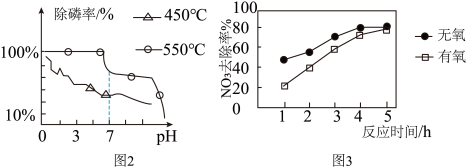
或者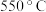 热处理纳米铁粉的除磷率以及
热处理纳米铁粉的除磷率以及 如图2所示。分析:温度为
如图2所示。分析:温度为_____ 时、_____ (填酸性或碱性)条件下处理效果更好。
(8)纳米铁粉能处理水体中的硝态氮。
在酸性条件下,纳米铁粉与 反应生成
反应生成 、
、 和水,该化学反应的化学方程式为
和水,该化学反应的化学方程式为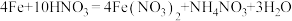 ,反应中化合价改变的元素有
,反应中化合价改变的元素有_____ 。
I.制备纳米铁粉
(1)已知氢气与菱铁矿(主要成分为
 )在高温条件下反应能得到铁、水及二氧化碳,请写出化学反应方程式
)在高温条件下反应能得到铁、水及二氧化碳,请写出化学反应方程式Ⅱ.探究所得固体成分
【提出问题】氢气与碳酸亚铁反应后剩余固体的成分是什么?
【做出猜想】
(2)猜想一:
 猜想二:
猜想二: 猜想三:
猜想三:【查阅资料】
①氢气具有还原性,能够冶炼金属。
②无水硫酸铜是一种白色固体,遇水会变为蓝色。
【实验探究】某学习小组利用如图1所示装置,对剩余固体成分(杂质不与稀硫酸反应)进行探究,实验操作及现象如下。回答下列问题。
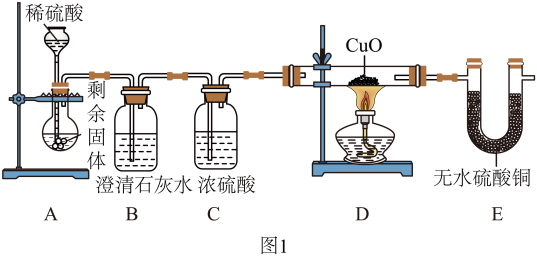
(4)向装置A中加入稀硫酸后,A中产生气泡且溶液变为浅绿色,甲同学判断猜想一正确,乙同学认为甲的判断不合理,理由是
(5)观察到装置B中澄清石灰水变浑浊,D中
【实验结论】综上所述,猜想三正确。
【反思交流】
(6)若去掉装置E
 。
。Ⅱ.处理水体中的氮、磷
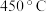 或者
或者 热处理纳米铁粉的除磷率以及
热处理纳米铁粉的除磷率以及 如图2所示。分析:温度为
如图2所示。分析:温度为(8)纳米铁粉能处理水体中的硝态氮。
在酸性条件下,纳米铁粉与
 反应生成
反应生成 、
、 和水,该化学反应的化学方程式为
和水,该化学反应的化学方程式为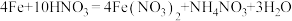 ,反应中化合价改变的元素有
,反应中化合价改变的元素有
您最近一年使用:0次
解题方法
9 . 燃煤发电仍是我国电力的主要来源。如何实现燃煤产生的二氧化碳零排放,是兑现我国“碳中和”承诺必须研究的课题。科学家设想利用煤和氧化铁反应发电并将二氧化碳转变成液体燃料甲醇( )的新工艺获得了一定的进展,该设想的反应原理流程如图所示:
)的新工艺获得了一定的进展,该设想的反应原理流程如图所示:_____ 。将“分离器”分离出的物质用“热空气循环氧化”时,所发生的反应属于基本反应类型中的_____ 反应。
(2)“合成器”中发生反应的化学方程式可表示为: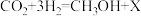 ,则X的化学式为
,则X的化学式为_____ 。
(3)在上述生产过程中,“合成器”需要隔绝空气的原因是_____ 。
(4)该流程主要产生的废弃物是_____ ,通过该流程_____ (填“能”或“不能”)达成燃煤发电的碳中和”。
 )的新工艺获得了一定的进展,该设想的反应原理流程如图所示:
)的新工艺获得了一定的进展,该设想的反应原理流程如图所示: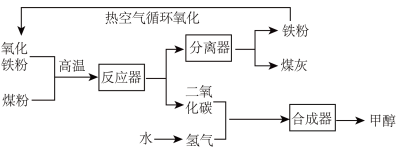
(2)“合成器”中发生反应的化学方程式可表示为:
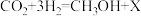 ,则X的化学式为
,则X的化学式为(3)在上述生产过程中,“合成器”需要隔绝空气的原因是
(4)该流程主要产生的废弃物是
您最近一年使用:0次
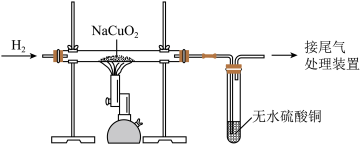
10 . 某小组用如图实验装置研究铜酸钠(NaCuO2)跟H2的反应。(已知无水硫酸铜遇水由白色变为蓝色)_______ 。正确的操作顺序是_______ (填序号)。操作②的目的是_______ 。
(2)经检测反应生成铜、氢氧化钠和水。写出反应的化学方程式:_______ ;根据化学方程式,判断氢气具有还原性的依据是_______ 。
(2)经检测反应生成铜、氢氧化钠和水。写出反应的化学方程式:
您最近一年使用:0次



