解题方法
1 . 如图是三种物质的溶解度曲线,下列说法正确的是
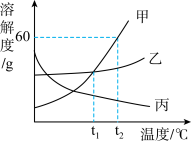

| A.丙物质的饱和溶液升温后,将变成不饱和溶液 |
| B.t1℃时甲物质和乙物质的溶解度相等 |
| C.t2℃时将70g甲物质加入100g水中, 可得到170g溶液 |
| D.甲物质的溶质质量分数一定比乙物质的溶质质量分数大 |
您最近一年使用:0次
2 . 下列说法正确的是( )
A.向 和 和 的混合溶液中加入一定量的镁条,过滤后,滤渣中一定有铜和铝,可能有镁 的混合溶液中加入一定量的镁条,过滤后,滤渣中一定有铜和铝,可能有镁 |
| B.同一温度下分别将两份不同质量的KCl饱和溶液恒温蒸发掉10g水,析出晶体的质量一定不相等 |
| C.将某饱和溶液析出晶体后,该溶液的溶质质量分数可能不变 |
D.金属M与 溶液发生反应: 溶液发生反应: ,M可能是铁 ,M可能是铁 |
您最近一年使用:0次
解题方法
3 . 下图为M、N两种固体饱和溶液溶质的质量分数(C%)随温度(t)变化的曲线,下列说法正确的是
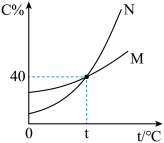

| A.50gM放入150g水中形成不饱和溶液 |
| B.t℃时,M的饱和溶液中溶质与溶液的质量比为2:5 |
| C.M中混有少量N物质,可以用降温结晶法提纯M |
| D.100gN的溶液,蒸发20g水、冷却至t℃后得到10g晶体,原溶液溶质的质量分数为30% |
您最近一年使用:0次
4 . 水是宝贵的资源。
(1)电解水可以得到 和
和 ,这个实验说明组成水的元素是
,这个实验说明组成水的元素是___________ (填元素符号)。电解水时生成 与
与 的体积比约为
的体积比约为___________ 。
(2)水能够溶解许多物质。下列观点正确的是___________。
(3)①溶液的浓度可以用溶质质量分数表示,如医疗上常使用10%的葡萄糖溶液,10%的含义为___________ 。
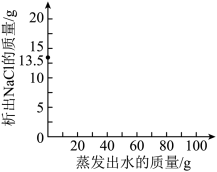
②取100g质量分数为13.5%的NaCl溶液,温度保持60℃,蒸发水分至NaCl完全析出,理论上需蒸发___________ g水后刚好达到饱和状态。在图中 画出析出NaCl的质量与蒸发出水质量的关系___________ (已知60℃时NaCl的溶解度约为37g)。
(4)自来水厂常用加消毒剂(如氯气)去除水中的细菌等微生物,原理是使细菌体卤蛋白质发生___________ (填“变性”或“盐析”),该变化是___________ 过程(填“可逆”或“不可逆”)。国家标准规定自来水经处理,微生物含量达标后,但出厂时仍需留有一定浓度的消毒剂,原因是___________ 。
(5)2023年的世界水日的主题是“加速变革”,呼吁加快落实保护并合理利用水资源的措施,以应对全球淡水资源匮乏的挑战。请写出家庭中可采取的一个节水措施:___________ 。
(1)电解水可以得到
 和
和 ,这个实验说明组成水的元素是
,这个实验说明组成水的元素是 与
与 的体积比约为
的体积比约为(2)水能够溶解许多物质。下列观点正确的是___________。
| A.自然界不存在“绝对纯净”的水 | B.水易溶解许多物质,因而水也易被污染 |
| C.在自然界中,不同状态的水处于不断循环中 | D.地下水是重要淡水资源,可持续不断大量开采 |
(3)①溶液的浓度可以用溶质质量分数表示,如医疗上常使用10%的葡萄糖溶液,10%的含义为
②取100g质量分数为13.5%的NaCl溶液,温度保持60℃,蒸发水分至NaCl完全析出,理论上需蒸发

(4)自来水厂常用加消毒剂(如氯气)去除水中的细菌等微生物,原理是使细菌体卤蛋白质发生
(5)2023年的世界水日的主题是“加速变革”,呼吁加快落实保护并合理利用水资源的措施,以应对全球淡水资源匮乏的挑战。请写出家庭中可采取的一个节水措施:
您最近一年使用:0次
5 . 小金分别在等量的蒸馏水中加入不同体积的同种硫酸溶液(硫酸不参与反应),做了三次电解水实验,测出电解水时收集到20毫升氢气所需的时间,数据记录如表所示。
请回答下列问题:
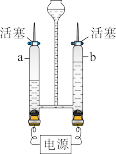
(1)根据上述实验设计可知,小欢要探究的问题是___________ 。
(2)实验中收集20毫升氢气,同时能收集到氧气的体积是___________ 毫升。
(3)第1次实验中,开始时,玻璃管内约有210毫升的硫酸溶液,结束后装置中剩下的硫酸溶液中,发生改变的是___________ (选填数字)。
①水的质量 ②硫酸溶质的质量 ③溶液的总质量 ④溶质的质量分数
| 实验次数 | 1 | 2 | 3 |
| 蒸馏水体积/毫升 | 200 | 200 | 200 |
| 加入硫酸溶液的体积/毫升 | 10 | 5 | 2 |
| 收集20毫升氢气的时间/秒 | 396 | 578 | 1231 |

(1)根据上述实验设计可知,小欢要探究的问题是
(2)实验中收集20毫升氢气,同时能收集到氧气的体积是
(3)第1次实验中,开始时,玻璃管内约有210毫升的硫酸溶液,结束后装置中剩下的硫酸溶液中,发生改变的是
①水的质量 ②硫酸溶质的质量 ③溶液的总质量 ④溶质的质量分数
您最近一年使用:0次
解题方法
6 . 试管内盛有25℃的饱和硝酸钾溶液,其上漂浮一小木块。如下图所示,将试管插入烧杯内的冰水混合物中,一段时间后,下列有关说法正确的是
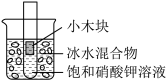

| A.试管内溶液的质量变小 | B.试管内有固体析出 |
| C.试管内溶液的溶质质量分数变大 | D.小木块浸入溶液内的体积变小 |
您最近一年使用:0次
7 . 生活链接:
(1)若现在有两杯无色的糖水,你会如何判断两杯糖水中哪杯更甜?
(2)若现在有两杯红糖水,一杯颜色浅,一杯颜色深,你会如何判断两杯糖水中哪杯更甜?
(1)若现在有两杯无色的糖水,你会如何判断两杯糖水中哪杯更甜?
(2)若现在有两杯红糖水,一杯颜色浅,一杯颜色深,你会如何判断两杯糖水中哪杯更甜?
您最近一年使用:0次
解题方法
8 . 如图是KNO3和KCl的溶解度曲线,请回答下列问题。

(1)60℃时,KNO3的溶解度是________ g。
(2)60℃时,配制相同质量的KNO3、KCI的饱和溶液,所需水的质量KNO3________ (填“>”、“<”或“=”)KCl。
(3)当KNO3中混有少量的KCl时,可用________ 的方法提纯KNO3。
(4)下列说法正确的是________ (填字母)。

(1)60℃时,KNO3的溶解度是
(2)60℃时,配制相同质量的KNO3、KCI的饱和溶液,所需水的质量KNO3
(3)当KNO3中混有少量的KCl时,可用
(4)下列说法正确的是________ (填字母)。
| A.KCl的不饱和溶液只能采用蒸发溶剂的方法变成饱和溶液 |
| B.60℃时,KNO3溶液的溶质质量分数一定比KCl溶液的溶质质量分数大 |
| C.将80℃时等质量的KNO3和KCl两种饱和溶液分别降温至10℃,析出晶体较多的是KNO3 |
您最近一年使用:0次
解题方法
9 . 氨气(NH3)在生产、生活方面应用广泛,请从不同角度对其进行认识。
Ⅰ.分类视角
(1)氮元素的“价类二维图”如图所示:
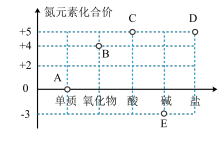
① 氨气中的氮元素的化合价为___________ 。
② 工业上可用氨气经过一系列的反应可以制得硝酸,反应过程中生成NO2的物质类别是__________ (填写名称)。
Ⅱ.变化视角
如图所示,某兴趣小组按以下步骤进行微型实验:实验时,用胶头滴管向W管的左右两端同时注入3mL浓氨水和3mL浓盐酸,一会儿后B处附近看到“白烟”,且管壁微微发热。

【查阅资料】①氨气与氯化氢反应生成白色固体氯化铵;②相同温度下,分子的运动速率与其相对分子质量成反比。
试从不同角度分析:
(2)滴加浓氨水后,A处酚酞变为__________ 色。
(3)氨气与氯化氢反应会__________ (填“放热”或“吸热”)。
(4)分析在B处附近出现“白烟”的微观原因是__________ 。
【实验反思】
(5)该实验使用微型装置的优点是__________ 。
(6)打开装有浓氨水的试剂瓶塞,观察到瓶口出现__________ ;一段时间后,浓氨水的溶质质量分数__________ (填“变大”或“不变”或“变小”)。
Ⅲ.应用视角
(7)工业上常用氨气来检验输送氯气(Cl2)的管道是否泄漏,若泄漏,则有白烟氯化铵(NH4Cl)和N2生成,该反应的化学方程式为__________ 。
Ⅰ.分类视角
(1)氮元素的“价类二维图”如图所示:

① 氨气中的氮元素的化合价为
② 工业上可用氨气经过一系列的反应可以制得硝酸,反应过程中生成NO2的物质类别是
Ⅱ.变化视角
如图所示,某兴趣小组按以下步骤进行微型实验:实验时,用胶头滴管向W管的左右两端同时注入3mL浓氨水和3mL浓盐酸,一会儿后B处附近看到“白烟”,且管壁微微发热。

【查阅资料】①氨气与氯化氢反应生成白色固体氯化铵;②相同温度下,分子的运动速率与其相对分子质量成反比。
试从不同角度分析:
(2)滴加浓氨水后,A处酚酞变为
(3)氨气与氯化氢反应会
(4)分析在B处附近出现“白烟”的微观原因是
【实验反思】
(5)该实验使用微型装置的优点是
(6)打开装有浓氨水的试剂瓶塞,观察到瓶口出现
Ⅲ.应用视角
(7)工业上常用氨气来检验输送氯气(Cl2)的管道是否泄漏,若泄漏,则有白烟氯化铵(NH4Cl)和N2生成,该反应的化学方程式为
您最近一年使用:0次
解题方法
10 . 如图是甲、乙两种固体物质的溶解度曲线。回答以下问题:
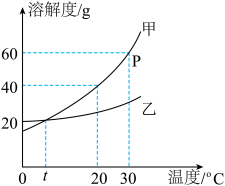
(1)P点的含义是_______ 。
(2)不改变溶液浓度,要使接近饱和的甲溶液变成饱和溶液,采用的方法是_______ ,当甲中含有少量乙时,可采用_______ 的方法提纯甲。
(3)30℃时,将40g甲物质放入盛有50g水的烧杯中,所得溶液中溶质的质量分数为_______ 。若将烧杯内物质升温到50℃(不考虑水蒸发),溶液中不变的是_______ (填字母序号)。
A.溶剂的质量
B.溶质的质量
C.溶液的质量
D.溶质的质量分数
(4)现有20℃等质量的甲、乙饱和溶液,加热蒸发掉等质量的水后恢复至20℃,剩余溶液的质量甲_______ 乙(填>、=或<)。

(1)P点的含义是
(2)不改变溶液浓度,要使接近饱和的甲溶液变成饱和溶液,采用的方法是
(3)30℃时,将40g甲物质放入盛有50g水的烧杯中,所得溶液中溶质的质量分数为
A.溶剂的质量
B.溶质的质量
C.溶液的质量
D.溶质的质量分数
(4)现有20℃等质量的甲、乙饱和溶液,加热蒸发掉等质量的水后恢复至20℃,剩余溶液的质量甲
您最近一年使用:0次



