解题方法
1 . 实验室中有一瓶质量为100g的过氧化氢溶液,已知该溶液中氢元素的含量为10.4%,则该过氧化氢溶液的溶质质量分数为
| A.15% | B.27.2% | C.6.8% | D.13.6% |
您最近一年使用:0次
2 . 将200g20%的硝酸钾溶液与800g10%的硝酸钾溶液混合,混合均匀后,所得溶液的溶质质量分数是
| A.15% | B.20% | C.10% | D.12% |
您最近一年使用:0次
解题方法
3 . 在配制一定溶质质量分数的氯化钠溶液时,下列误差分析错误的是
| A.称量氯化钠时,左盘放了纸片右盘没放纸片,溶质质量分数偏小 |
| B.量取水时,俯视量筒刻度,溶质质量分数偏小 |
| C.往烧杯内转移称量好的氯化钠时,有少量晶体撒落,溶质质量分数偏小 |
| D.往试剂瓶内转移配制好的溶液时,有少量液体洒落,溶质质量分数不变 |
您最近一年使用:0次
解题方法
4 . 海水淡化可采用膜分离技术,如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各种盐的离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是


| A.溶质质量改变 | B.溶剂质量减少 |
| C.溶液质量不变 | D.溶质质量分数不变 |
您最近一年使用:0次
5 . 如图,A、B为两个电极,放在盛有氢氧化钠溶液的玻璃容器里,闭合开关后,电极上将有气泡产生(电解水的过程),B电极上出现的气泡为________________ (填物质名称);在这一过程中,氢氧化钠溶液的浓度________________ (选填“变大”或“变小”),灯泡亮度变________________ (选填“亮”或“暗”)。
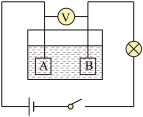

您最近一年使用:0次
名校
解题方法
6 . 实验室用石灰石与稀盐酸反应制取二氧化碳。若要制取4.4g二氧化碳,需要溶质的质量分数为10%的盐酸多少克?
您最近一年使用:0次
解题方法
7 . 市售的“84”消毒液、过氧化氢溶液都是常见的家用消毒剂。两种消毒液混合使用会怎样?化学兴趣小组的同学进行了探究。
【查阅资料】
1 “84”消毒液的有效成分是次氯酸钠(化学式为NaClO),含有次氯酸钠的消毒液具有较强的挥发性,在储存时需要加以防护。
2 “84”消毒液和过氧化氢溶液混合,能产生氧气。
【提出问题】次氯酸钠(NaClO)和过氧化氢反应中,次氯酸钠的作用是什么?
【猜想假设】
(1)猜想1:作反应物,NaClO与过氧化氢溶液发生化学反应。
猜想2:作___________ ,类似双氧水分解制氧气反应中MnO2的作用。
【进行实验】
①按图所示组装实验装置,并检查装置气密性。
③将注射器中过氧化氢溶液平均分5次推入锥形瓶中;每次推入过氧化氢溶液,待不再产生气泡后,记录生成气体的总体积如下表。(忽略其他因素对测量结果的影响)
(2)表中的数据x=___________ 。
(3)分析表中数据得出“猜想1正确”,其依据是___________ 。
【分析讨论】
(4)次氯酸钠与过氧化氢溶液反应除生成氧气外,还生成氯化钠和水。写出该反应的化学方程式:___________ 。
(5)测定该过氧化氢溶液中溶质的质量分数。将136g过氧化氢溶液滴入盛有2g二氧化锰的烧杯中,完全反应后,得到1.6g氧气。则过氧化氢溶液中溶质的质量分数为___________ 。
【拓展应用】
生活中常用消毒剂除“84”消毒液、过氧化氢溶液外,还有75%酒精、过氧乙酸等。
(6)生活中使用消毒剂应注意的是:___________ 。(写出1条)
(7)使用75%的酒精消毒,应远离明火,防止火灾。从燃烧条件分析,酒精是___________ ;“明火”的作用是___________ 。
【查阅资料】
1 “84”消毒液的有效成分是次氯酸钠(化学式为NaClO),含有次氯酸钠的消毒液具有较强的挥发性,在储存时需要加以防护。
2 “84”消毒液和过氧化氢溶液混合,能产生氧气。
【提出问题】次氯酸钠(NaClO)和过氧化氢反应中,次氯酸钠的作用是什么?
【猜想假设】
(1)猜想1:作反应物,NaClO与过氧化氢溶液发生化学反应。
猜想2:作
【进行实验】
①按图所示组装实验装置,并检查装置气密性。
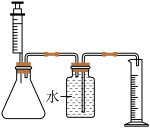
③将注射器中过氧化氢溶液平均分5次推入锥形瓶中;每次推入过氧化氢溶液,待不再产生气泡后,记录生成气体的总体积如下表。(忽略其他因素对测量结果的影响)
| 过氧化氢溶液的用量 | 第1次加入5mL | 第2次加入5ml | 第3次加入5mL | 第4次加入5mL | 第5次加入5mL |
| 收集气体的总体积/mL | 140 | 280 | 365 | x | 365 |
(2)表中的数据x=
(3)分析表中数据得出“猜想1正确”,其依据是
【分析讨论】
(4)次氯酸钠与过氧化氢溶液反应除生成氧气外,还生成氯化钠和水。写出该反应的化学方程式:
(5)测定该过氧化氢溶液中溶质的质量分数。将136g过氧化氢溶液滴入盛有2g二氧化锰的烧杯中,完全反应后,得到1.6g氧气。则过氧化氢溶液中溶质的质量分数为
【拓展应用】
生活中常用消毒剂除“84”消毒液、过氧化氢溶液外,还有75%酒精、过氧乙酸等。
(6)生活中使用消毒剂应注意的是:
(7)使用75%的酒精消毒,应远离明火,防止火灾。从燃烧条件分析,酒精是
您最近一年使用:0次
解题方法
8 . 40℃时,将80.0g氯化钾加到200g水中,进行如图操作。

(1)氯化钾的溶解度随温度降低的变化趋势是___________ 。
(2)A溶液属于___________ (填“饱和”或“不饱和”)溶液。
(3)溶液A、B、C、D的溶质质量分数的大小关系是___________ 。
(4)20℃时氯化钾的溶解度为___________ g。

(1)氯化钾的溶解度随温度降低的变化趋势是
(2)A溶液属于
(3)溶液A、B、C、D的溶质质量分数的大小关系是
(4)20℃时氯化钾的溶解度为
您最近一年使用:0次
解题方法
9 . 如图是甲、乙两种物质的溶解度曲线。下列说法正确的是


| A.乙的溶解度一定大于甲 |
| B.20℃时,甲的饱和溶液的溶质质量分数为30% |
| C.将60℃时甲的饱和溶液降温至40℃,析出50g晶体 |
| D.当甲中混有少量乙时,可采用降温结晶的方法提纯甲 |
您最近一年使用:0次
名校
解题方法
10 . 某化学兴趣小组的同学为测定稀盐酸样品的溶质质量分数,进行了如下图所示实验。(温馨提示: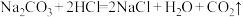 )
)
(1)反应产生的二氧化碳气体的质量为________ g。
(2)稀盐酸中溶质的质量分数。
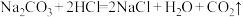 )
)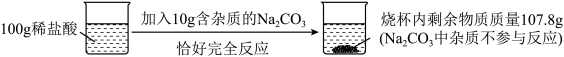
(1)反应产生的二氧化碳气体的质量为
(2)稀盐酸中溶质的质量分数。
您最近一年使用:0次



