1 . 下列实验方案设计合理的是
| 实验目的 | 实验方案 | |
| A | 除去 中的水蒸气 中的水蒸气 | 通过装有浓硫酸的洗气瓶 |
| B | 鉴别 溶液和 溶液和 溶液 溶液 | 分别加入氢氧化钡溶液 |
| C | 分离 和 和 | 加水溶解,过滤,洗涤,干燥 |
| D | 鉴别氯化钠和氢氧化钠 | 加足量水,搅拌,观察是否溶解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-06-12更新
|
33次组卷
|
2卷引用:2024年新疆阿苏克地区中考三模化学试题
名校
解题方法
2 . 物质的性质决定其用途,下列对应关系不正确的是
| A.铁粉能吸收氧气和水蒸气,用于食品防腐 |
| B.浓硫酸有吸水性,可用于干燥氨气 |
| C.甲醛能使蛋白质失去生理活性,可用于浸泡植物标本 |
| D.电木具有热固性,可制成锅具手柄 |
您最近一年使用:0次
2024·河南·模拟预测
解题方法
3 . 酸、碱、盐在生产和生活中有着广泛的应用。
(1)在实验室中常用浓硫酸做干燥剂,是利用了浓硫酸的______ (填字母)。
a.腐蚀性 b.吸水性 c.氧化性 d.酸性
(2)氢氧化锂(LiOH)是制备新能源汽车锂电池的重要原料,与氢氧化钠的化学性质非常相似,氢氧化锂与二氧化碳反应的化学方程式是______ 。
(3)某实验小组用图甲所示装置探究稀盐酸与氢氧化钠的反应,结果如图乙所示。______
②图乙a、b、c、d四点中,对应图甲中烧瓶内溶液呈无色的是______ (填字母)。
(4)采用氨碱法生产纯碱的主要流程如下: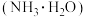 ,二氧化碳能溶于水,我们从酸碱反应的角度知道:在用氨碱法生产纯碱过程中,先向饱和食盐水中通入氨气,制成饱和氨盐水,再向其中通过二氧化碳,其原因是
,二氧化碳能溶于水,我们从酸碱反应的角度知道:在用氨碱法生产纯碱过程中,先向饱和食盐水中通入氨气,制成饱和氨盐水,再向其中通过二氧化碳,其原因是______ 。实际生产中沉淀池内的温度不能太高,原因是______ 。
(5)工业产品中往往含有一些杂质,用“氨碱法”制得的纯碱含有少量氯化钠。为了测定该产品中碳酸钠的纯度,进行以下实验:取16.5g纯碱样品放入烧杯中,将烧杯放在电子天平上,再把150g稀盐酸(足量)加入样品中,观察读数变化如下表所示:
该产品中碳酸钠的质量分数(写出计算过程,结果精确到0.1%)。
(1)在实验室中常用浓硫酸做干燥剂,是利用了浓硫酸的
a.腐蚀性 b.吸水性 c.氧化性 d.酸性
(2)氢氧化锂(LiOH)是制备新能源汽车锂电池的重要原料,与氢氧化钠的化学性质非常相似,氢氧化锂与二氧化碳反应的化学方程式是
(3)某实验小组用图甲所示装置探究稀盐酸与氢氧化钠的反应,结果如图乙所示。
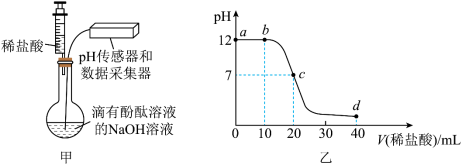
②图乙a、b、c、d四点中,对应图甲中烧瓶内溶液呈无色的是
(4)采用氨碱法生产纯碱的主要流程如下:

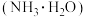 ,二氧化碳能溶于水,我们从酸碱反应的角度知道:在用氨碱法生产纯碱过程中,先向饱和食盐水中通入氨气,制成饱和氨盐水,再向其中通过二氧化碳,其原因是
,二氧化碳能溶于水,我们从酸碱反应的角度知道:在用氨碱法生产纯碱过程中,先向饱和食盐水中通入氨气,制成饱和氨盐水,再向其中通过二氧化碳,其原因是(5)工业产品中往往含有一些杂质,用“氨碱法”制得的纯碱含有少量氯化钠。为了测定该产品中碳酸钠的纯度,进行以下实验:取16.5g纯碱样品放入烧杯中,将烧杯放在电子天平上,再把150g稀盐酸(足量)加入样品中,观察读数变化如下表所示:
| 时间/s | 0 | 5 | 10 | 15 |
| 读数/g | 215.2 | 211.4 | 208.6 | 208.6 |
您最近一年使用:0次
2024·江西·模拟预测
4 . 某同学在教材实验的基础上,设计如图所示装置进行实验。_______ 。
(2)为保证实验顺利进行,实验前需_______ 。
(3)装置A中发生反应的化学方程式为_______ 。
(4)利用装置D验证二氧化碳的性质,a、c为湿润的用紫色石蕊溶液浸泡过的棉花,b为干燥的用紫色石蕊溶液浸泡过的棉花。一段时间后,观察到b处棉花不变色,a、c处棉花变红,且c处棉花先变红,说明CO2的性质是_______ 。
(5)若实验过程中观察到装置D中b处棉花也变红,可能的原因是_______ (写出一种),请写出对应的改进措施_______ 。
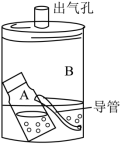
(6)如图是一台简易制氧机,A瓶中装有“茶垢净”(遇到热水后会产生氧气)、二氧化锰和水,氧气可从B瓶盖子上的出气孔排出,供人呼吸。A瓶的导管伸入B瓶水中的目的是_______ 。
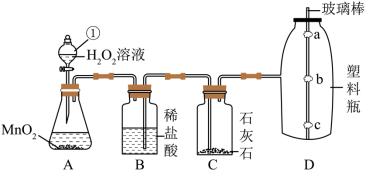
(2)为保证实验顺利进行,实验前需
(3)装置A中发生反应的化学方程式为
(4)利用装置D验证二氧化碳的性质,a、c为湿润的用紫色石蕊溶液浸泡过的棉花,b为干燥的用紫色石蕊溶液浸泡过的棉花。一段时间后,观察到b处棉花不变色,a、c处棉花变红,且c处棉花先变红,说明CO2的性质是
(5)若实验过程中观察到装置D中b处棉花也变红,可能的原因是
(6)如图是一台简易制氧机,A瓶中装有“茶垢净”(遇到热水后会产生氧气)、二氧化锰和水,氧气可从B瓶盖子上的出气孔排出,供人呼吸。A瓶的导管伸入B瓶水中的目的是
您最近一年使用:0次
解题方法
5 . 牙膏中的摩擦剂主要用于增强牙膏的摩擦作用和去污效果,牙膏中常用的摩擦剂有CaCO3和SiO2。我校化学兴趣小组的同学们购买了某品牌牙膏,他们探究该品牌牙膏中摩擦剂的成分,于是开启了探究之旅。
【提出问题1】该品牌牙膏中摩擦剂的成分是什么?
【查阅资料】SiO2不易溶水也不与稀盐酸反应。牙膏中除了CaCO3外其它成分不与稀盐酸反应。
【作出猜想】
(1)猜想一:只含有SiO2;猜想二:只含有CaCO3;猜想三:_______ 。
【实验步骤】
(2)请完善下面表格。
【提出问题2】该品牌牙膏中CaCO3的含量是多少?
兴趣小组同学们设计了如下图的实验装置来测定CaCO3的含量,用气密性良好的装置装上药品并通一会儿氮气后关闭止水夹,再打开分液漏斗活塞。
提示:碱石灰(可以吸收CO2和H2O)和浓硫酸均足量,稀盐酸不考虑其挥发性。_______ (填“活泼”或者“不活泼”)。
(4)浓硫酸的作用是_______ 。
(5)测定CaCO3的含量需要测定两个物理量,其中一个物理量为样品的质量。另一个物理量为 (填序号)。
(6)若去掉丁装置,测得CaCO3含量_______ (填“偏高”、“偏低”或“不变”)。
(7)甲装置中反应结束后打开止水夹再通入一会儿N2的目的是_______ 。
【提出问题1】该品牌牙膏中摩擦剂的成分是什么?
【查阅资料】SiO2不易溶水也不与稀盐酸反应。牙膏中除了CaCO3外其它成分不与稀盐酸反应。
【作出猜想】
(1)猜想一:只含有SiO2;猜想二:只含有CaCO3;猜想三:
【实验步骤】
(2)请完善下面表格。
| 实验操作 | 实验现象 | 实验结论 |
| 取适量的牙膏溶解于水中,搅拌,静置后过滤,向滤渣中加入足量的稀盐酸。 | 猜想三成立 |
【提出问题2】该品牌牙膏中CaCO3的含量是多少?
兴趣小组同学们设计了如下图的实验装置来测定CaCO3的含量,用气密性良好的装置装上药品并通一会儿氮气后关闭止水夹,再打开分液漏斗活塞。
提示:碱石灰(可以吸收CO2和H2O)和浓硫酸均足量,稀盐酸不考虑其挥发性。

(4)浓硫酸的作用是
(5)测定CaCO3的含量需要测定两个物理量,其中一个物理量为样品的质量。另一个物理量为 (填序号)。
| A.滴下的稀盐酸质量 | B.反应前后乙装置增加的质量 |
| C.反应前后丙装置增加的质量 | D.反应前后丁装置增加的质量 |
(6)若去掉丁装置,测得CaCO3含量
(7)甲装置中反应结束后打开止水夹再通入一会儿N2的目的是
您最近一年使用:0次
解题方法
6 . 物质性质决定用途。下列说法正确的是
| A.浓H2SO4有吸水性,可用于干燥氨气 |
| B.75%的酒精能使蛋白质失去生理活性,可用于杀菌消毒 |
| C.氯化钠易溶于水,可以用作食品调味剂 |
| D.明矾溶于水能形成吸附性物质,可用于自来水的杀菌消毒 |
您最近一年使用:0次
2024-06-11更新
|
29次组卷
|
2卷引用:2024年5月山东省曲阜市第二次中考模拟化学试题
解题方法
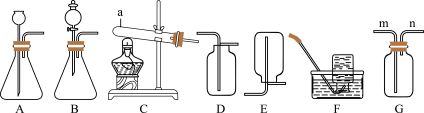
7 . Ⅰ.实验室制取气体所需的装置如图所示,请回答以下问题:__________ 。
(2)实验室C装置制取氧气时,反应的化学方程式为____________________ 。若选用F装置收集较纯净氧气的适宜时间是__________ 。
(3)AB装置都可以制取氧气、二氧化碳和氢气,若要控制液体滴加速率,获得平稳气流,应选择的发生装置是__________ 。若用G装置收集二氧化碳,其验满的方法是____________________ 。
Ⅱ.三草酸合铁酸钾晶体,化学式为K3[Fe(C2O4)3]•3H2O,某小组为探究其热分解产物(除水外),按如图所示装置进行实验。__________ 。
(5)装置中B、C、D的作用分别是__________ 。(填字母)
A.检验CO2、吸收CO2、吸收水分 B.吸收CO2、检验CO2、吸收水分
(2)实验室C装置制取氧气时,反应的化学方程式为
(3)AB装置都可以制取氧气、二氧化碳和氢气,若要控制液体滴加速率,获得平稳气流,应选择的发生装置是
Ⅱ.三草酸合铁酸钾晶体,化学式为K3[Fe(C2O4)3]•3H2O,某小组为探究其热分解产物(除水外),按如图所示装置进行实验。

(5)装置中B、C、D的作用分别是
A.检验CO2、吸收CO2、吸收水分 B.吸收CO2、检验CO2、吸收水分
您最近一年使用:0次
8 . 以下装置常用于实验室制取气体,请回答问题。_____ 。
(2)实验室用氯酸钾和二氧化锰制取氧气,反应的化学方程式为____ ,该反应的基本反应类型是____ 。制取较纯净的氧气可选用____ (填字母序号)装置。
(3)实验室可用装置B制取CO2,该装置的优点是____ 。若利用装置F除去CO2中的水蒸气,气体应从___ (填“m”或“n”)端通入,瓶中盛装的试剂是__ (填试剂名称)。
(4)如图G所示,将CO2缓慢通入竖直放置的玻璃管中,能观察到玻璃管下方湿润的蓝色石蕊试纸先变红。通过此现象可推测CO2的物理性质是___ 。

(2)实验室用氯酸钾和二氧化锰制取氧气,反应的化学方程式为
(3)实验室可用装置B制取CO2,该装置的优点是
(4)如图G所示,将CO2缓慢通入竖直放置的玻璃管中,能观察到玻璃管下方湿润的蓝色石蕊试纸先变红。通过此现象可推测CO2的物理性质是
您最近一年使用:0次
2024-06-11更新
|
94次组卷
|
2卷引用:2024年新疆乌鲁木齐5月检测中考物理、化学试卷-初中化学
名校
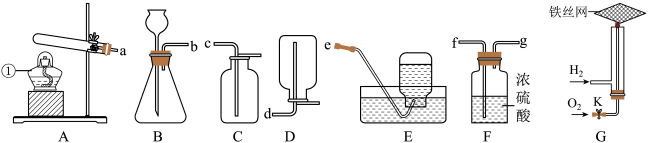
9 . 化学是一门以实验为基础的学科。请结合图示回答问题:___________ 。
(2)实验室用高锰酸钾制取氧气的化学方程式为___________ ,若利用该反应制取并收集一瓶干燥的氧气,所选装置的正确连接顺序是___________ (用装置导管口的字母填空)。
(3)用G装置模拟氢氧焰实验,关闭开关K,通入氢气并点燃。为保证安全,点燃氢气之前应先___________ ,将铁丝网放在火焰上灼烧,铁丝网只发红,不熔断,打开开关K,通入氧气,火焰更明亮,铁丝熔断,说明燃烧的剧烈程度与___________ 有关。
(4)实验室现有一包生锈的铜粉样品,其成分是铜粉、碱式碳酸铜(绿色)及少量水,为测定其中碱式碳酸铜的质量分数,某化学兴趣小组的同学利用如图所示装置进行实验。
主要实验步骤如下:
Ⅰ.将样品装入装置B的玻璃管中,连接好装置A、B,打开弹簧夹通空气一段时间。
Ⅱ.连接好以上整套装置,关闭弹簧夹,给样品加热,待样品完全反应后,再打开弹簧夹通入空气,然后关闭恒温电加热器,直到玻璃管冷却。
Ⅲ.实验完毕,测得装置C、D中的液体质量分别增加了m1、m2,根据实验所测数据计算该样品中碱式碳酸铜的质量分数。
①装置C中导气管口处的实验现象是___________ 。
②步骤Ⅱ中,先打开弹簧夹通入空气,再关闭恒温电加热器的目的是___________ 。
(2)实验室用高锰酸钾制取氧气的化学方程式为
(3)用G装置模拟氢氧焰实验,关闭开关K,通入氢气并点燃。为保证安全,点燃氢气之前应先
(4)实验室现有一包生锈的铜粉样品,其成分是铜粉、碱式碳酸铜(绿色)及少量水,为测定其中碱式碳酸铜的质量分数,某化学兴趣小组的同学利用如图所示装置进行实验。
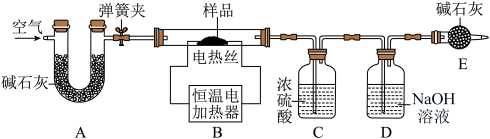
主要实验步骤如下:
Ⅰ.将样品装入装置B的玻璃管中,连接好装置A、B,打开弹簧夹通空气一段时间。
Ⅱ.连接好以上整套装置,关闭弹簧夹,给样品加热,待样品完全反应后,再打开弹簧夹通入空气,然后关闭恒温电加热器,直到玻璃管冷却。
Ⅲ.实验完毕,测得装置C、D中的液体质量分别增加了m1、m2,根据实验所测数据计算该样品中碱式碳酸铜的质量分数。
①装置C中导气管口处的实验现象是
②步骤Ⅱ中,先打开弹簧夹通入空气,再关闭恒温电加热器的目的是
您最近一年使用:0次
10 . 实验室学习化学的重要途径:
(一)实验室用下图所示装置制二氧化碳气体,并进行相关实验研究。
①锥形瓶内发生反应的化学方程式为___________ 。
②由实验现象可推知二氧化碳具有的物理性质为___________ 。
(2)若在装置A与二氧化碳收集装置之间增加装置C,其目的是___________ 。
(二)检验二氧化碳。图1是用大理石和盐酸制备的二氧化碳,并验证二氧化碳和澄清石灰水反应的装置。进行该实验时,同学们发现澄清石灰水中只看到出现气泡,但未见浑浊,于是猜想,可能是二氧化碳中混有氯化氢气体。
(3)甲同学用图2所示装置进行实验,结果观察到C中溶液变浑浊:为进一步验证,再取B中反应后的溶液,滴加___________ (填化学式)溶液,出现白色浑浊,则上述猜想成立。
(4)通过上述实验可知,用盐酸制取气体时,往往混有氯化氢气体,说明盐酸具有_______ 性。乙同学选择用饱和碳酸氢钠溶液除去二氧化碳中的氯化氢气体,发生反应的化学方程式为_______ 。
(5)丙同学不理解,混有氯化气体的二氧化碳为什么不能使澄清石灰水变浑浊。请你帮他解释一下:___________ (用化学方程式表示)。
(三)探究二氧化碳性质______ (填“Ⅰ”“Ⅱ”“Ⅲ”),实验①的结论是_______ 。
(7)实验②:证明氢氧化钠与盐酸发生了化学反应的现象是_______ 。
(8)实验③:向充满二氧化碳的锥形瓶中先注入氢氧化钠溶液,振荡,未观察到明显现象,再打开弹簧夹并注入_______ (填一种试剂名称),产生气泡,证明氢氧化钠与二氧化碳已发生反应。
(一)实验室用下图所示装置制二氧化碳气体,并进行相关实验研究。
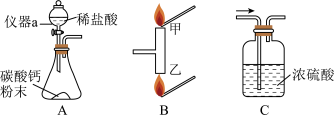
①锥形瓶内发生反应的化学方程式为
②由实验现象可推知二氧化碳具有的物理性质为
(2)若在装置A与二氧化碳收集装置之间增加装置C,其目的是
(二)检验二氧化碳。图1是用大理石和盐酸制备的二氧化碳,并验证二氧化碳和澄清石灰水反应的装置。进行该实验时,同学们发现澄清石灰水中只看到出现气泡,但未见浑浊,于是猜想,可能是二氧化碳中混有氯化氢气体。

(3)甲同学用图2所示装置进行实验,结果观察到C中溶液变浑浊:为进一步验证,再取B中反应后的溶液,滴加
(4)通过上述实验可知,用盐酸制取气体时,往往混有氯化氢气体,说明盐酸具有
(5)丙同学不理解,混有氯化气体的二氧化碳为什么不能使澄清石灰水变浑浊。请你帮他解释一下:
(三)探究二氧化碳性质

(7)实验②:证明氢氧化钠与盐酸发生了化学反应的现象是
(8)实验③:向充满二氧化碳的锥形瓶中先注入氢氧化钠溶液,振荡,未观察到明显现象,再打开弹簧夹并注入
您最近一年使用:0次



