解题方法
1 . 空气中体积分数为21%的气体是_______ ;最理想的清洁燃料是_______ 。
您最近一年使用:0次
解题方法
2 . 阅读下面材料。
2024年4月28日举行的中关村论坛上,氢能产业再次成为热点话题。
氢气的主要来源包括化石燃料制氢和电解水制氢。化石燃料制氢技术比较成熟,但也存在诸多问题。利用可再生能源电解水制氢是目前理想的制氢技术,其技术主要有三种,分别是光催化、光电催化和光-电催化耦合制氢,对应的氢能转化率如表1。
表1
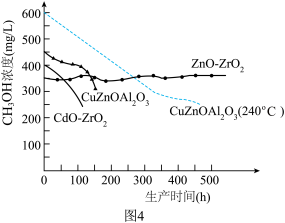
“液态阳光”关键技术之一是合成甲醇时催化剂的选择。工业生产选择催化剂时,催化剂的稳定性是重要参考条件之一。中国科学家突破了这一关键技术(部分研究成果如图4),推动了“液态阳光”生产从实验室走向应用。事实证明,这是切实可行的碳中和路径。
依据上述材料及所学化学知识,回答下列问题。
(1)氢能属于_______ 能源(填“可再生”或“不可再生”)。
(2)电解水制氢技术中,在电源的_______ 极产生氢气。
(3)如表1所示,光-电催化耦合技术优势之一是_______ 。
(4)氢气和二氧化碳在催化剂作用下转化为甲醇和水的化学方程式为_____ 。
(5)煤经过加工合成的甲醇,______ (填“能”或“不能”)称作“液态阳光”。
(6)甲醇可以直接使用现有的以汽油为主的燃料储存运输设施,原因是_______ 。
(7)根据图1信息,选出合成“液态阳光”最适合的催化剂_______(填序号)。
(8)“液态阳光”是理想的储氢材料,据此推测其不仅在合成的过程中能吸收氢气,还应具备的化学性质是_______ 。
(9)“液态阳光”的应用具有减碳、碳中和等作用,原因是_______ (写出一点即可)。
2024年4月28日举行的中关村论坛上,氢能产业再次成为热点话题。
氢气的主要来源包括化石燃料制氢和电解水制氢。化石燃料制氢技术比较成熟,但也存在诸多问题。利用可再生能源电解水制氢是目前理想的制氢技术,其技术主要有三种,分别是光催化、光电催化和光-电催化耦合制氢,对应的氢能转化率如表1。
表1
| 可再生能源制氢技术 | 氢能转化率 |
| 光催化 | 不足5% |
| 光电催化 | 不足5% |
| 光-电催化耦合 | 70%以上 |
“液态阳光”关键技术之一是合成甲醇时催化剂的选择。工业生产选择催化剂时,催化剂的稳定性是重要参考条件之一。中国科学家突破了这一关键技术(部分研究成果如图4),推动了“液态阳光”生产从实验室走向应用。事实证明,这是切实可行的碳中和路径。
依据上述材料及所学化学知识,回答下列问题。
(1)氢能属于
(2)电解水制氢技术中,在电源的
(3)如表1所示,光-电催化耦合技术优势之一是
(4)氢气和二氧化碳在催化剂作用下转化为甲醇和水的化学方程式为
(5)煤经过加工合成的甲醇,
(6)甲醇可以直接使用现有的以汽油为主的燃料储存运输设施,原因是
(7)根据图1信息,选出合成“液态阳光”最适合的催化剂_______(填序号)。
| A.ZnO-ZrO2 | B.CuZnOAl2O3 | C.CuZnOAl2O3(240℃) | D.CdO-ZrO2 |
(8)“液态阳光”是理想的储氢材料,据此推测其不仅在合成的过程中能吸收氢气,还应具备的化学性质是
(9)“液态阳光”的应用具有减碳、碳中和等作用,原因是
您最近一年使用:0次
3 . 氢能源被广泛应用的关键之一是要有大规模制氢的途径。现有工业制氢方式中,甲烷和二氧化碳重整制氢是一种重要工艺。在加热的条件下,甲烷和二氧化碳发生化学反应,生成一氧化碳和氢气,请写出该反应的化学方程式:______ 。氢能是未来最理想的能源,从环保角度分析,氢能最突出的优点是______ 。
您最近一年使用:0次
解题方法
4 . 请选择合适的物质,并用对应序号填空。
①氢气 ②赤铁矿 ③熟石灰 ④氯离子
(1)最清洁的燃料是_______ 。
(2)可改良酸性土壤的是_______ 。
(3)用于高炉炼铁的物质是_______ 。
(4)人体胃液中含有的阴离子是_______ 。
①氢气 ②赤铁矿 ③熟石灰 ④氯离子
(1)最清洁的燃料是
(2)可改良酸性土壤的是
(3)用于高炉炼铁的物质是
(4)人体胃液中含有的阴离子是
您最近一年使用:0次
解题方法
5 . 资源的合理利用和环境保护是人类共同关注的问题。
(1)氢气是一种理想能源,氢气燃烧的化学方程式为_________ ;与石油等化石燃料相比,氢能源的优点是_________ 。(写出一条即可)
(2)甲醇(CH3OH)不完全燃烧生成CO2、H2O和污染气体CO。若一定质量的甲醇燃烧生成CO和CO2的质量比为7:11,则参加反应的氧气与生成的一氧化碳分子个数比为_________ 。
(1)氢气是一种理想能源,氢气燃烧的化学方程式为
(2)甲醇(CH3OH)不完全燃烧生成CO2、H2O和污染气体CO。若一定质量的甲醇燃烧生成CO和CO2的质量比为7:11,则参加反应的氧气与生成的一氧化碳分子个数比为
您最近一年使用:0次
解题方法
6 . 中国新能源汽车远销世界各国。问界M9、小米SU7等一经上市,受到广大市民的追捧。
(1)新能源汽车的发展对缓解环境污染、实现“碳中和”有着重要的意义。中国自制氢能源汽车实现交通“零排放”的原因是_______ 。
(2)传统的燃油汽车使用的汽油是三大化石燃料中_______ 的综合利用的产物。
(3)电动汽车中电池的原理之一为高铁酸钾 和锌反应,生成锌酸钾
和锌反应,生成锌酸钾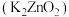 、氧化铁及氧化锌,同时释放出电能,标出高铁酸钾
、氧化铁及氧化锌,同时释放出电能,标出高铁酸钾 中
中 的化合价:
的化合价:_______ 。
(1)新能源汽车的发展对缓解环境污染、实现“碳中和”有着重要的意义。中国自制氢能源汽车实现交通“零排放”的原因是
(2)传统的燃油汽车使用的汽油是三大化石燃料中
(3)电动汽车中电池的原理之一为高铁酸钾
 和锌反应,生成锌酸钾
和锌反应,生成锌酸钾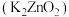 、氧化铁及氧化锌,同时释放出电能,标出高铁酸钾
、氧化铁及氧化锌,同时释放出电能,标出高铁酸钾 中
中 的化合价:
的化合价:
您最近一年使用:0次
解题方法
7 . 某研究所利用太阳能聚光器获得的高能量进行热化学循环反应制取 ,其流程如图所示,下列有关说法不正确的是
,其流程如图所示,下列有关说法不正确的是
 ,其流程如图所示,下列有关说法不正确的是
,其流程如图所示,下列有关说法不正确的是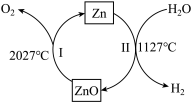
| A.反应Ⅰ属于分解反应 |
| B.反应Ⅱ中锌元素的化合价升高 |
C. 燃烧热值高,是一种理想的清洁能源 燃烧热值高,是一种理想的清洁能源 |
| D.该循环过程中,锌的质量不断减少 |
您最近一年使用:0次
2024九年级下·上海·专题练习
解题方法
8 . 根据下列实验装置图,回答有关问题。______ 该装置的优点是______ 。若在装置E中连接压强传感器(如图F),测定实验中试管内气体压强变化的情况(如下图)。压强变化与实验现象或操作相对应的是______ (填序号)。
(2)实验室以锌和稀硫酸为原料,______ (填“能”或“不能”)用E装置制氢气,若要制取0.1mol的氢气,需要9.8%的稀硫酸多少克?______ (根据化学方程式计算)
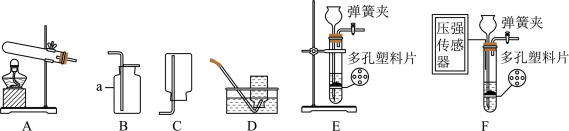
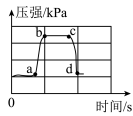
序号 | 图像 | 实验现象或操作 |
Ⅰ | a-b | 试管中液面逐渐上升 |
Ⅱ | b-c | 大理石与稀盐酸脱离接触 |
Ⅲ | c-d | 打开弹簧夹 |
(2)实验室以锌和稀硫酸为原料,
您最近一年使用:0次
9 . 如图是实验室制取气体的常用装置。
(2)实验室用锌粒和稀硫酸反应制取较纯净的氢气,可选用的发生装置和收集装置分别是什么?
(3)用E装置制取气体,可随时控制反应的发生和停止,请写出控制反应停止的原理。
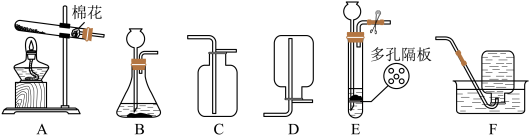
(2)实验室用锌粒和稀硫酸反应制取较纯净的氢气,可选用的发生装置和收集装置分别是什么?
(3)用E装置制取气体,可随时控制反应的发生和停止,请写出控制反应停止的原理。
您最近一年使用:0次
解题方法
10 . 根据图回答问题:______ (字母),用该装置制取氧气所需的药品是______ 。
(2)若要用装置G收集氧气,空气应从______ (填“a”或“b”)端排出。
(3)若用金属锌和稀硫酸反应制取并收集干燥的氢气,从A~F中选用装置的连接顺序为______ (填字母)。
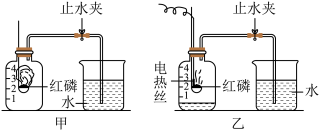
(4)图中乙装置是测定空气中氧气含量的改进装置(电热丝通电引燃红磷),与甲装置相比,改进后的优点是______ 。实验结束后观察到从烧杯中进入集气瓶内的水的体积仍明显小于瓶内原空气体积的1/5,请分析可能的原因______ (答出一点即可)
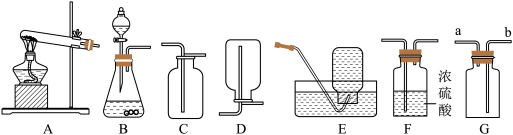
(2)若要用装置G收集氧气,空气应从
(3)若用金属锌和稀硫酸反应制取并收集干燥的氢气,从A~F中选用装置的连接顺序为
(4)图中乙装置是测定空气中氧气含量的改进装置(电热丝通电引燃红磷),与甲装置相比,改进后的优点是
您最近一年使用:0次



