2024九年级·湖北·专题练习
解题方法
1 . 根据如图实验装置,回答下列问题:_____________ 。
(2)写出实验室用 A 装置制取氧气的化学反应方程式_____________ 。
(3)实验室制取并收集一瓶较纯净的H2时,并想控制反应的速率,应选择的装置组合是_____________ 。
(4)若用 E装置收集 CO2,请设计实验检验 CO2已经收集满:_____________ 。

(2)写出实验室用 A 装置制取氧气的化学反应方程式
(3)实验室制取并收集一瓶较纯净的H2时,并想控制反应的速率,应选择的装置组合是
(4)若用 E装置收集 CO2,请设计实验检验 CO2已经收集满:
您最近一年使用:0次
2024九年级·江苏无锡·专题练习
解题方法
2 . 某化学兴趣小组同学学习了气体性质实验后,对氢气的性质开展以下学习。
【项目一:氢气的性质】
用自制的氢气通过软管吹泡泡液并用喷枪点燃,观察现象。
(1)吹出的泡泡液大多数都上升,但也有少数的泡泡液下降,可能的原因是_____ 。
【项目二:氢气点燃需验纯】
【查阅资料】三种常见可燃性气体的爆炸极限:
(2)点燃上面两袋气体,发现甲发生爆炸,原因是_____ 。
(3)根据上表可以得出,____ (填写气体名称)使用最安全,该气体可通过氢氧化钠和醋酸钠(CH3COONa)在加热条件下制得,同时得到碳酸钠,请写出该反应的化学方程式:____ 。
同学用温度传感器分别测定氢气(锌粒和稀硫酸反应装置导管中导出)和酒精灯燃烧后火焰温度的变化情况。
(4)结合甲图信息,可以得出氢气做燃料比酒精好,理由是______ 。
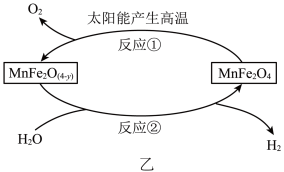
(5)科学家研究开发氢能源的脚步从未停止。如图乙为利用MnFe2O4热化学循环制氢的反应流程,反应前后Mn的化合价均为+2价。
①与传统电解法制取氢气相比,该流程的优点是____ 。
②若MnFe2O(4﹣y)中y=0.5,则MnFe2O(4﹣y)中Fe3+与Fe2+的个数比为____ 。
(6)氢气是一种清洁能源,但仍需要深度研究。请简述目前氢气的研究所面临的困难和问题:___ 、___ 。(写出两点即可)
(7)下列各组元素具有相似化学性质的是 (填字母)。
(8)保持液态氢的化学性质的最小粒子是___ 。
【项目一:氢气的性质】
用自制的氢气通过软管吹泡泡液并用喷枪点燃,观察现象。
(1)吹出的泡泡液大多数都上升,但也有少数的泡泡液下降,可能的原因是
【项目二:氢气点燃需验纯】


【查阅资料】三种常见可燃性气体的爆炸极限:
| 可燃气体 | 爆炸极限(体积分数) |
| H2 | 4.0%﹣74.2% |
| CH4 | 5%﹣15% |
| CO | 12.5%﹣74.2% |
(2)点燃上面两袋气体,发现甲发生爆炸,原因是
(3)根据上表可以得出,
同学用温度传感器分别测定氢气(锌粒和稀硫酸反应装置导管中导出)和酒精灯燃烧后火焰温度的变化情况。
(4)结合甲图信息,可以得出氢气做燃料比酒精好,理由是
(5)科学家研究开发氢能源的脚步从未停止。如图乙为利用MnFe2O4热化学循环制氢的反应流程,反应前后Mn的化合价均为+2价。
①与传统电解法制取氢气相比,该流程的优点是
②若MnFe2O(4﹣y)中y=0.5,则MnFe2O(4﹣y)中Fe3+与Fe2+的个数比为
(6)氢气是一种清洁能源,但仍需要深度研究。请简述目前氢气的研究所面临的困难和问题:
(7)下列各组元素具有相似化学性质的是 (填字母)。
| A.H和Ar | B.Li和Na | C.He和Be | D.F和Cl |
(8)保持液态氢的化学性质的最小粒子是
您最近一年使用:0次
3 . 2024年3月全国两会提出要加快发展新质生产力,新质生产力的底色是绿色低碳。下列说法与此理念不符的是
| A.维持以“煤炭为主”的能源结构,保障能源供给稳定 |
| B.用CO2人工合成淀粉,有利于实现碳中和 |
| C.氢气是一种高能环保新能源,应加快氢能的发展 |
| D.科学、合理地加快海洋资源的开发和利用 |
您最近一年使用:0次
4 . 下列叙述错误的是
| A.氢气被认为是理想的清洁、高能燃料 |
| B.冬季使用融雪剂清雪,虽然能减少交通事故,但会对土壤造成污染 |
| C.pH<6.5的雨水称为酸雨 |
| D.发生火灾时可用湿毛巾,捂住口鼻,低下身子沿墙壁跑出火灾区 |
您最近一年使用:0次
解题方法
5 . 阅读下面材料。
2024年4月28日举行的中关村论坛上,氢能产业再次成为热点话题。
氢气的主要来源包括化石燃料制氢和电解水制氢。化石燃料制氢技术比较成熟,但也存在诸多问题。利用可再生能源电解水制氢是目前理想的制氢技术,其技术主要有三种,分别是光催化、光电催化和光-电催化耦合制氢,对应的氢能转化率如表1。
表1
“液态阳光”关键技术之一是合成甲醇时催化剂的选择。工业生产选择催化剂时,催化剂的稳定性是重要参考条件之一。中国科学家突破了这一关键技术(部分研究成果如图4),推动了“液态阳光”生产从实验室走向应用。事实证明,这是切实可行的碳中和路径。
依据上述材料及所学化学知识,回答下列问题。
(1)氢能属于_______ 能源(填“可再生”或“不可再生”)。
(2)电解水制氢技术中,在电源的_______ 极产生氢气。
(3)如表1所示,光-电催化耦合技术优势之一是_______ 。
(4)氢气和二氧化碳在催化剂作用下转化为甲醇和水的化学方程式为_____ 。
(5)煤经过加工合成的甲醇,______ (填“能”或“不能”)称作“液态阳光”。
(6)甲醇可以直接使用现有的以汽油为主的燃料储存运输设施,原因是_______ 。
(7)根据图1信息,选出合成“液态阳光”最适合的催化剂_______(填序号)。
(8)“液态阳光”是理想的储氢材料,据此推测其不仅在合成的过程中能吸收氢气,还应具备的化学性质是_______ 。
(9)“液态阳光”的应用具有减碳、碳中和等作用,原因是_______ (写出一点即可)。
2024年4月28日举行的中关村论坛上,氢能产业再次成为热点话题。
氢气的主要来源包括化石燃料制氢和电解水制氢。化石燃料制氢技术比较成熟,但也存在诸多问题。利用可再生能源电解水制氢是目前理想的制氢技术,其技术主要有三种,分别是光催化、光电催化和光-电催化耦合制氢,对应的氢能转化率如表1。
表1
| 可再生能源制氢技术 | 氢能转化率 |
| 光催化 | 不足5% |
| 光电催化 | 不足5% |
| 光-电催化耦合 | 70%以上 |
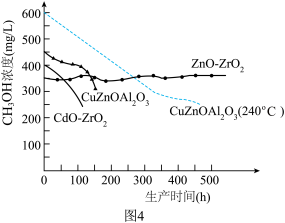
“液态阳光”关键技术之一是合成甲醇时催化剂的选择。工业生产选择催化剂时,催化剂的稳定性是重要参考条件之一。中国科学家突破了这一关键技术(部分研究成果如图4),推动了“液态阳光”生产从实验室走向应用。事实证明,这是切实可行的碳中和路径。
依据上述材料及所学化学知识,回答下列问题。
(1)氢能属于
(2)电解水制氢技术中,在电源的
(3)如表1所示,光-电催化耦合技术优势之一是
(4)氢气和二氧化碳在催化剂作用下转化为甲醇和水的化学方程式为
(5)煤经过加工合成的甲醇,
(6)甲醇可以直接使用现有的以汽油为主的燃料储存运输设施,原因是
(7)根据图1信息,选出合成“液态阳光”最适合的催化剂_______(填序号)。
| A.ZnO-ZrO2 | B.CuZnOAl2O3 | C.CuZnOAl2O3(240℃) | D.CdO-ZrO2 |
(8)“液态阳光”是理想的储氢材料,据此推测其不仅在合成的过程中能吸收氢气,还应具备的化学性质是
(9)“液态阳光”的应用具有减碳、碳中和等作用,原因是
您最近一年使用:0次
2024-06-17更新
|
200次组卷
|
4卷引用:2024年辽宁省沈阳市中考一模化学试题
6 . 回答问题
(1)实验室制取CO2和H2
ⅰ.仪器①的名称是___________ 。
ⅱ.小明用相同一套装置分别制取CO2和H2,应选用如图中发生装置___________ (填字母)。其中,制取CO2的化学方程式为___________ 。___________ g,量取体积时需用到如图的仪器有___________ (填字母);若在量取水的体积时仰视读数,则导致所配溶液溶质质量分数将___________ (填“偏大”或“偏小”或“不变”)。
ⅰ.第一代采用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)为推进剂,反应的化学方程式为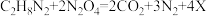 ,则X的化学式为
,则X的化学式为___________ 。
ⅱ.第二代以煤油作为推进剂,从石油中分离出航天煤油类似于实验操作中的___________ 。
ⅲ.第三代火箭推进剂常用到液氢和液氧组合,工业制取氧气利用分子筛可将氧分子从空气中“筛”出去,从而获得高浓度的氧气。其原理示意图如图所示,由此可知两种分子的大小:N2___________ (填“>”或“<”)O2。
(1)实验室制取CO2和H2
ⅰ.仪器①的名称是
ⅱ.小明用相同一套装置分别制取CO2和H2,应选用如图中发生装置


ⅰ.第一代采用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)为推进剂,反应的化学方程式为
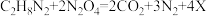 ,则X的化学式为
,则X的化学式为ⅱ.第二代以煤油作为推进剂,从石油中分离出航天煤油类似于实验操作中的
ⅲ.第三代火箭推进剂常用到液氢和液氧组合,工业制取氧气利用分子筛可将氧分子从空气中“筛”出去,从而获得高浓度的氧气。其原理示意图如图所示,由此可知两种分子的大小:N2

您最近一年使用:0次
解题方法
7 . 如图为实验室制取气体的部分装置,请按要求回答下列问题。_________ ;写出用改正后的装置制取氧气的化学方程式_____________ ;反应的基本类型是______ 。
(2)实验室制取二氧化碳的化学方程式是__________ ;以上装置可用于检验二氧化碳的是_____ (填序号),其装置内发生反应的化学方程式为____________ 。
(3)氢气是一种密度比空气小且难溶于水的气体,实验室用锌粒和稀硫酸反应制取并收集干燥的氢气,写出发生装置、收集装置导管口字母的连接顺序______ 。

(2)实验室制取二氧化碳的化学方程式是
(3)氢气是一种密度比空气小且难溶于水的气体,实验室用锌粒和稀硫酸反应制取并收集干燥的氢气,写出发生装置、收集装置导管口字母的连接顺序
您最近一年使用:0次
2024-06-17更新
|
38次组卷
|
3卷引用:贵州省贵阳市开阳县2024年5月中考模考·理综试题-初中化学
真题
解题方法
8 . 规范的操作是实验成功的保证。下列实验操作正确的是
A.读取液体体积 | B.点燃酒精灯 |
C.振荡试管 | D.收集氢气 |
您最近一年使用:0次
真题
解题方法
9 . 气体的制取和性质是初中化学核心知识之一,结合以下实验装置回答问题。_______ 。
(2)氢气是最理想的能源,实验室常用锌粒和稀硫酸制取。若制取并收集较干燥的氢气,应选择的装置组合是_______ (从图1的A~E中选择,填字母序号)。
(3)若选用F装置制氢气,其优点是______ 。
炭和水蒸气在高温条件下反应也会生成氢气,同时生成碳的氧化物。为探究该反应生成气体的成分,化学兴趣小组进行了如下实验(部分步骤及装置已省略)。
【猜想与假设】
同学们讨论得出,气体成分有H2,还有CO和CO2中的一种或两种。
【查阅资料】
①H2具有还原性。
②无水硫酸铜是一种白色固体,遇水会变成蓝色。
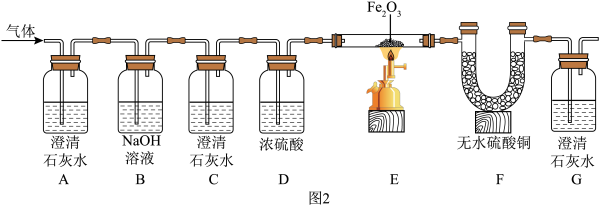
【设计并进行实验】将反应生成的气体按图2装置进行实验:________ 。
【实验现象与结论】
(5)A、C装置中无明显现象,E装置中固体由红色变为黑色,F装置中无水硫酸铜变蓝,G装置中澄清石灰水变浑浊。写出G装置中石灰水变浑浊的化学方程式:_________ 。
(6)由此得出:炭和水蒸气在高温条件下反应生成了H2和CO。写出CO与Fe2O3反应的化学方程式:_______ 。
【反思与评价】
(7)从环保角度考虑,该实验存在的不足是______ 。

(2)氢气是最理想的能源,实验室常用锌粒和稀硫酸制取。若制取并收集较干燥的氢气,应选择的装置组合是
(3)若选用F装置制氢气,其优点是
炭和水蒸气在高温条件下反应也会生成氢气,同时生成碳的氧化物。为探究该反应生成气体的成分,化学兴趣小组进行了如下实验(部分步骤及装置已省略)。
【猜想与假设】
同学们讨论得出,气体成分有H2,还有CO和CO2中的一种或两种。
【查阅资料】
①H2具有还原性。
②无水硫酸铜是一种白色固体,遇水会变成蓝色。
【设计并进行实验】将反应生成的气体按图2装置进行实验:
【实验现象与结论】
(5)A、C装置中无明显现象,E装置中固体由红色变为黑色,F装置中无水硫酸铜变蓝,G装置中澄清石灰水变浑浊。写出G装置中石灰水变浑浊的化学方程式:
(6)由此得出:炭和水蒸气在高温条件下反应生成了H2和CO。写出CO与Fe2O3反应的化学方程式:
【反思与评价】
(7)从环保角度考虑,该实验存在的不足是
您最近一年使用:0次
10 . 为完成“了解家用制氧机”,学习小组开展如下探究活动了解实验室制氧原理。______ 。
(2)实验室制取氧气用发生装置A的反应的化学方程式为______ 。如果用D装置收集氧气,气体应从管______ (填“a”或“b”)进入,验满的操作是______ 。
(3)某品牌家用“便携式制氧机”的制氧原理如图所示(内部结构透明)。
①将过碳酸钠和二氧化锰加入水中,过碳酸钠先分解,生成的H2O2再分解产生氧气。H2O2分解的化学方程式为______ 。
②反应仓相当于是图甲中的______ 装置,该装置更换药品后也能用来制取二氧化碳或氢气,请分析理由______ 。
③制取氧气时,观察孔可以看到加湿过滤仓里的情况,从化学的角度来看,你认为加湿过滤仓可能有的作用是______ 。

(2)实验室制取氧气用发生装置A的反应的化学方程式为
(3)某品牌家用“便携式制氧机”的制氧原理如图所示(内部结构透明)。
①将过碳酸钠和二氧化锰加入水中,过碳酸钠先分解,生成的H2O2再分解产生氧气。H2O2分解的化学方程式为
②反应仓相当于是图甲中的
③制取氧气时,观察孔可以看到加湿过滤仓里的情况,从化学的角度来看,你认为加湿过滤仓可能有的作用是
您最近一年使用:0次



