解题方法
1 . 化合反应可表示为:a+b+…→x。下列说法中正确的个数有
①x可能为氧化物、酸、碱或盐
②a、b、x可能含有同一种元素
③a、b可能都是单质,但不可能都是化合物
④化合反应一定是放热反应
①x可能为氧化物、酸、碱或盐
②a、b、x可能含有同一种元素
③a、b可能都是单质,但不可能都是化合物
④化合反应一定是放热反应
| A.0个 | B.1个 | C.2个 | D.3个 |
您最近一年使用:0次
解题方法
2 . 为验证镁片与稀盐酸反应放热,同学们设计了以下实验方案,请根据下列提示,补全实验内容:
【实验方法】
(1)按照如图所示进行实验,实验过程中取用镁片的操作:用______ 将镁片放在横放的试管口,再将试管慢慢竖立起来。
(2)试管中发生反应的化学方程式为_______ 。
(3)【实验现象】_______ 。
【实验结论】镁片与稀盐酸反应放热。
【问题与交流】
(4)①该实验成功的关键是______ (写一条)。
②实验后,对剩余药品的处理办法是_______ 。
【实验方法】
(1)按照如图所示进行实验,实验过程中取用镁片的操作:用
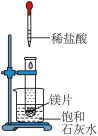
(2)试管中发生反应的化学方程式为
(3)【实验现象】
【实验结论】镁片与稀盐酸反应放热。
【问题与交流】
(4)①该实验成功的关键是
②实验后,对剩余药品的处理办法是
您最近一年使用:0次
解题方法
3 . 松花蛋是我国特有的一种传统美食。化学兴趣小组同学进行了“松花蛋制作”的项目研究,请结合任务回答问题。
【任务一】初识松花蛋,查阅营养成分
(1)松花蛋,又称皮蛋,制作原料为鸡蛋(或鸭蛋),鸡蛋中富含的营养素为________ ,除此之外,还含有油脂、维生素及无机盐等多种营养素,具有较高的营养价值。
【任务二】
(2)品尝松花蛋,感受松花蛋的酸碱性同学们品尝松花蛋时,发现松花蛋略有涩味,他联想到碱性物质通常有涩味,推测松花蛋中含有碱性物质,生活中食用时可加入________ 来中和涩味。(选填“料酒、食醋或酱油”)
【任务三】浸松花蛋粉,寻找涩味缘由
取适量松花蛋粉(用于制作松花蛋泥的原料),加入足量水,搅拌、过滤。测得滤液pH=12,证明滤液中含有碱性物质。
【提出问题】滤液中的碱性物质是什么?
【查阅资料】
(3)松花蛋粉中主要含有生石灰、食盐、纯碱(Na2CO3)等,其中碳酸钠属于________ (填物质类别),它的水溶液显_________ 性。
【分析推理】
松花蛋粉加水调和时发生如下反应:
(4)① 是
是__________ (填“吸热”或“放热”)反应。
②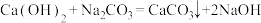
【提出猜想】
(5)猜想一:只有NaOH;
猜想二:有NaOH和__________ (填化学式);
猜想三:有NaOH和Na2CO3。
【实验探究】
(6)
通过以上探究,同学们找到了松花蛋粉加水后滤液显碱性的原因,寻到了涩味的缘由。
【任务一】初识松花蛋,查阅营养成分
(1)松花蛋,又称皮蛋,制作原料为鸡蛋(或鸭蛋),鸡蛋中富含的营养素为
【任务二】
(2)品尝松花蛋,感受松花蛋的酸碱性同学们品尝松花蛋时,发现松花蛋略有涩味,他联想到碱性物质通常有涩味,推测松花蛋中含有碱性物质,生活中食用时可加入
【任务三】浸松花蛋粉,寻找涩味缘由
取适量松花蛋粉(用于制作松花蛋泥的原料),加入足量水,搅拌、过滤。测得滤液pH=12,证明滤液中含有碱性物质。
【提出问题】滤液中的碱性物质是什么?
【查阅资料】
(3)松花蛋粉中主要含有生石灰、食盐、纯碱(Na2CO3)等,其中碳酸钠属于
【分析推理】
松花蛋粉加水调和时发生如下反应:
(4)①
 是
是②
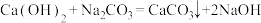
【提出猜想】
(5)猜想一:只有NaOH;
猜想二:有NaOH和
猜想三:有NaOH和Na2CO3。
【实验探究】
(6)
| 操作 | 现象 | 结论 |
| 取滤液少许,向其中加入过量的稀盐酸 | 无明显现象 | 滤液中不含 |
| 另取滤液少许,向其中加入碳酸钠溶液 | 猜想二成立 |
您最近一年使用:0次
名校
解题方法
4 . 附加题:空气中 含量的控制和
含量的控制和 资源利用具有重要意义。
资源利用具有重要意义。
(1)燃煤烟气中 的捕集可通过如图所示的物质转化实现。
的捕集可通过如图所示的物质转化实现。______ 。
②“吸收”后所得的 溶液与石灰乳反应的生成物有水、
溶液与石灰乳反应的生成物有水、______ 、______ ;载人航天器内,常用LiOH固体而很少用KOH固体吸收空气中的 ,其原因是
,其原因是______ 。
(2)合成尿素 是利用
是利用 的途径之一。尿素
的途径之一。尿素 合成主要通过下列反应实现:
合成主要通过下列反应实现: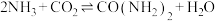 ,反应中,除尿素为液态,其余物质均为气态。已知:平衡常数
,反应中,除尿素为液态,其余物质均为气态。已知:平衡常数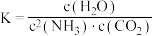 ,其中,c为物质的量浓度,单位为mol/L,K的大小反映了化学反应进行的程度,K值越大,表示反应进行得越完全。
,其中,c为物质的量浓度,单位为mol/L,K的大小反映了化学反应进行的程度,K值越大,表示反应进行得越完全。______ 反应(填“放热”或“吸热”)。
②某温度下,向容积为100L的密闭容器中通入 和
和 ,该反应进行到40s时达到平衡,此时
,该反应进行到40s时达到平衡,此时 的转化率为50%。该温度下此反应平衡常数K的值为
的转化率为50%。该温度下此反应平衡常数K的值为______ (只写数字)。
(3)催化电解吸收 的KOH溶液可将
的KOH溶液可将 还原为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图乙所示。(电解池中,电源负极与阴极相连。)
还原为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图乙所示。(电解池中,电源负极与阴极相连。)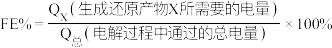 。其中,
。其中, ,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
①当电解电压为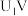 时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物为
时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物为______ (填化学式)。
②当电解电压为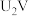 时,阴极由
时,阴极由 生成
生成 时,转移的电子的物质的量为
时,转移的电子的物质的量为______ mol。
③当电解电压为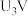 时,电解生成的
时,电解生成的 和
和 的物质的量之比为
的物质的量之比为______ (只写结果)。
 含量的控制和
含量的控制和 资源利用具有重要意义。
资源利用具有重要意义。(1)燃煤烟气中
 的捕集可通过如图所示的物质转化实现。
的捕集可通过如图所示的物质转化实现。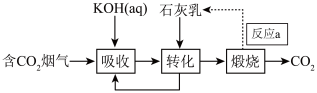
②“吸收”后所得的
 溶液与石灰乳反应的生成物有水、
溶液与石灰乳反应的生成物有水、 ,其原因是
,其原因是(2)合成尿素
 是利用
是利用 的途径之一。尿素
的途径之一。尿素 合成主要通过下列反应实现:
合成主要通过下列反应实现: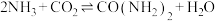 ,反应中,除尿素为液态,其余物质均为气态。已知:平衡常数
,反应中,除尿素为液态,其余物质均为气态。已知:平衡常数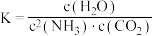 ,其中,c为物质的量浓度,单位为mol/L,K的大小反映了化学反应进行的程度,K值越大,表示反应进行得越完全。
,其中,c为物质的量浓度,单位为mol/L,K的大小反映了化学反应进行的程度,K值越大,表示反应进行得越完全。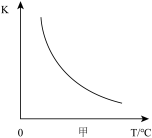
②某温度下,向容积为100L的密闭容器中通入
 和
和 ,该反应进行到40s时达到平衡,此时
,该反应进行到40s时达到平衡,此时 的转化率为50%。该温度下此反应平衡常数K的值为
的转化率为50%。该温度下此反应平衡常数K的值为(3)催化电解吸收
 的KOH溶液可将
的KOH溶液可将 还原为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图乙所示。(电解池中,电源负极与阴极相连。)
还原为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图乙所示。(电解池中,电源负极与阴极相连。)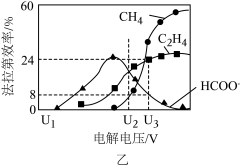
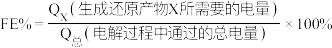 。其中,
。其中, ,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。①当电解电压为
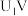 时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物为
时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物为②当电解电压为
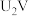 时,阴极由
时,阴极由 生成
生成 时,转移的电子的物质的量为
时,转移的电子的物质的量为③当电解电压为
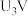 时,电解生成的
时,电解生成的 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
2024-06-08更新
|
32次组卷
|
2卷引用:山东省青岛大学附属中学2023-2024学年九年级下学期阶段性检测化学试卷
解题方法
5 . 某化学小组将等质量的锌、铁、铜三种金属粉末分别加入等质量、相同质量分数的稀硫酸中,观察到铜与稀硫酸无反应,测得锌、铁与稀硫酸反应产生气体体积与时间的关系如图所示,关于该小组的实验有下列说法,其中错误的是
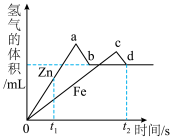
A.从 时间就可以得出金属活动性: 时间就可以得出金属活动性: |
| B.一定时间内气体体积从a降到b说明装置气密性不好 |
C.反应结束后 一定剩余, 一定剩余, 可能剩余 可能剩余 |
D. 是说明 是说明 生成的氢气比 生成的氢气比 多 多 |
您最近一年使用:0次
解题方法
6 . 我国是茶文化的发源地。唐代陆羽《茶经》中记载;“风炉以铜铁铸之……底一窗以为通飚漏烬之所……风能兴火,火能熟水。“漉水囊……其格以生铜铸之。”___________ (填“金属”或“合成”)材料。
(2)“飚”(即风)提供燃烧所需的___________ 。
(3)“火能熟水”说明燃烧___________ (填“吸收”或“放出”)热量。
(4)“漉水囊”可将茶叶与茶水分离,类似于基本实验操作中的___________ 。

(2)“飚”(即风)提供燃烧所需的
(3)“火能熟水”说明燃烧
(4)“漉水囊”可将茶叶与茶水分离,类似于基本实验操作中的
您最近一年使用:0次
7 . 如图1为氯化钠、碳酸钠在水中的溶解度曲线。请回答下列问题: 时,向两只盛有
时,向两只盛有 水的烧杯中,分别加入氯化钠、碳酸钠两种物质,至不再溶解为止,所得溶液的溶质质量分数大的是
水的烧杯中,分别加入氯化钠、碳酸钠两种物质,至不再溶解为止,所得溶液的溶质质量分数大的是_______ 溶液。
(2) 时,向
时,向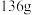 氯化钠的饱和溶液中加一定质量的水,配成
氯化钠的饱和溶液中加一定质量的水,配成 的氯化钠溶液用于农业生产中的选种,请计算加入水的质量
的氯化钠溶液用于农业生产中的选种,请计算加入水的质量_______ g。
(3)将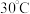 时相同质量的两种物质的饱和溶液,分别降温到
时相同质量的两种物质的饱和溶液,分别降温到 ,晶体析出较多的是
,晶体析出较多的是_______ 。
(4)如图2所示, 时,将盛有饱和碳酸钠溶液的小试管放入盛有液体甲的烧杯中,向甲中加入某固体乙后,试管中有晶体析出。甲、乙物质的组合可能是_______(填字母序号)。
时,将盛有饱和碳酸钠溶液的小试管放入盛有液体甲的烧杯中,向甲中加入某固体乙后,试管中有晶体析出。甲、乙物质的组合可能是_______(填字母序号)。
(5)当碳酸钠的饱和溶液中含有少量氯化钠时,可选用_______ 方法获得碳酸钠晶体。(填“蒸发结晶”或“降温结晶”)
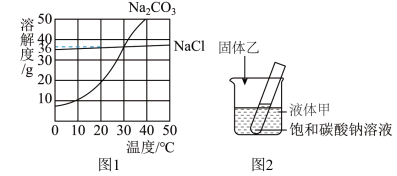
 时,向两只盛有
时,向两只盛有 水的烧杯中,分别加入氯化钠、碳酸钠两种物质,至不再溶解为止,所得溶液的溶质质量分数大的是
水的烧杯中,分别加入氯化钠、碳酸钠两种物质,至不再溶解为止,所得溶液的溶质质量分数大的是(2)
 时,向
时,向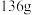 氯化钠的饱和溶液中加一定质量的水,配成
氯化钠的饱和溶液中加一定质量的水,配成 的氯化钠溶液用于农业生产中的选种,请计算加入水的质量
的氯化钠溶液用于农业生产中的选种,请计算加入水的质量(3)将
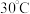 时相同质量的两种物质的饱和溶液,分别降温到
时相同质量的两种物质的饱和溶液,分别降温到 ,晶体析出较多的是
,晶体析出较多的是(4)如图2所示,
 时,将盛有饱和碳酸钠溶液的小试管放入盛有液体甲的烧杯中,向甲中加入某固体乙后,试管中有晶体析出。甲、乙物质的组合可能是_______(填字母序号)。
时,将盛有饱和碳酸钠溶液的小试管放入盛有液体甲的烧杯中,向甲中加入某固体乙后,试管中有晶体析出。甲、乙物质的组合可能是_______(填字母序号)。| A.水和氢氧化钠 | B.稀盐酸和镁 | C.水和硝酸铵 | D.水和冰 |
(5)当碳酸钠的饱和溶液中含有少量氯化钠时,可选用
您最近一年使用:0次
2024-06-06更新
|
38次组卷
|
2卷引用:2024年山东省日照市莒县中考二模化学试题
名校
解题方法
8 . 运用手持技术探究金属与酸的反应。向250mL的烧瓶内注入25mL质量分数为8.8%的稀盐酸,分别剪取长约4cm、宽约0.4cm的镁、铝、锌、铁、铜金属条,打磨后投入烧瓶中,迅速塞紧带有压强传感器的橡胶塞如图甲,点击采集,得到如图乙所示的气压变化曲线。______ ;你判断的依据是______ 。
(2)曲线c在18s左右达到最高点后又略微下降的原因是______ 。
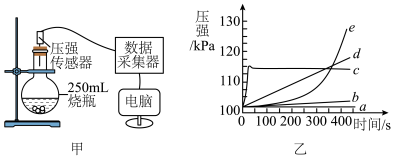
(2)曲线c在18s左右达到最高点后又略微下降的原因是
您最近一年使用:0次
解题方法
9 . 化学小组在“设计和制作简易供氧器”的实践活动中,探究影响供氧剂过碳酸钠产氧速率的因素。
【查阅资料】
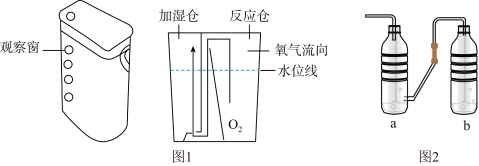
Ⅰ. 化学小组研究了图1所示的某品牌制氧机的装置原理后,利用身边物品自制了如图2所示的简易供氧器。
实验1:探究药品用量、温度对产氧速率的影响
【进行实验】在不同温度下,取一定质量的过碳酸钠和MnO2放入b瓶中,并加入相同体积的水,测得平均产氧速率数据如下表所示。
实验2:探究加水量对产氧速率的影响
【进行实验】20℃时,取一定质量的过碳酸钠和MnO2放入b瓶中,并加入不同体积的水,测得平均产氧速率及反应过程中温度变化数据如下表所示。
【解释与结论】
(1)实验中,过氧化氢分解生成氧气的化学方程式为_______ 。
(2)设计实验①②的目的是_______ 。
(3)由①③可以得到的结论是_______ 。
(4)⑤中x应为_______ 。
(5)依据实验2可知,该制氧过程中发生的化学反应属于_______ (填“吸热”或“放热”)反应。
【反思与评价】
(6)由上述实验可知,适当增加加水量可减缓产氧速率,其证据是_______ 。
(7)某同学欲进一步探究MnO2质量对产氧速率有影响,设计的实验方案是:20℃时,_______ 。
【查阅资料】
Ⅰ. 化学小组研究了图1所示的某品牌制氧机的装置原理后,利用身边物品自制了如图2所示的简易供氧器。
实验1:探究药品用量、温度对产氧速率的影响
【进行实验】在不同温度下,取一定质量的过碳酸钠和MnO2放入b瓶中,并加入相同体积的水,测得平均产氧速率数据如下表所示。
| 序号 | 过碳酸钠质量/g | MnO2质量/g | 温度/℃ | 平均产氧速率mL/s |
| ① | 10 | 0.3 | 26 | 2.73 |
| ② | 20 | 0.3 | 26 | 8.56 |
| ③ | 10 | 0.3 | 41 | 4.54 |
【进行实验】20℃时,取一定质量的过碳酸钠和MnO2放入b瓶中,并加入不同体积的水,测得平均产氧速率及反应过程中温度变化数据如下表所示。
| 序号 | 过碳酸钠质量/g | MnO2质量/g | 加水体积/mL | 反应液最高温度/℃ | 平均产氧速率mL/s |
| ④ | 240 | 2.5 | 350 | 98 | 33.3 |
| ⑤ | x | 2.5 | 500 | 74 | 15 |
| ⑥ | 240 | 2.5 | 800 | 53 | 10 |
(1)实验中,过氧化氢分解生成氧气的化学方程式为
(2)设计实验①②的目的是
(3)由①③可以得到的结论是
(4)⑤中x应为
(5)依据实验2可知,该制氧过程中发生的化学反应属于
【反思与评价】
(6)由上述实验可知,适当增加加水量可减缓产氧速率,其证据是
(7)某同学欲进一步探究MnO2质量对产氧速率有影响,设计的实验方案是:20℃时,
您最近一年使用:0次
名校
解题方法
10 . 以物质甲为原料合成化工产品丁的微观过程如图,下列说法正确的是
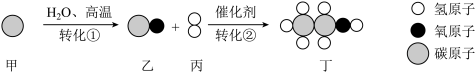
| A.转化①生成的物质乙,可使紫色石蕊溶液变成红色 |
| B.转化①是一个放热反应 |
| C.转化②中乙、丙分子个数比是1:3 |
| D.丁物质属于可再生能源 |
您最近一年使用:0次



