1 . 某兴趣小组的同学们在实验室用块状大理石和稀盐酸反应制取 的实验时,发现产生气泡的速率都不相同,并对这一现象展开了探究。
的实验时,发现产生气泡的速率都不相同,并对这一现象展开了探究。
【提出问题】影响产生二氧化碳气体速率的因素有哪些?
【作出猜想】猜想一:稀盐酸的浓度
猜想二:石块中碳酸钙的质量分数
猜想三:石块颗粒大小
【实验设计】为验证上述猜想,同学们设计了如图1所示的实验装置进行探究。将各试管生成的气体分别通入到足量相同体积、相同浓度的氢氧化钠溶液中,称量相同反应时间内各组氢氧化钠溶液增加的质量。
(1)对A组和B组实验:双察到A组产生气体使氢氧化钠溶液增加的质量小于B组;验证了猜想_____ 是正确的。
(2)对比B组和C组实验:观察到B组产生气体使氢氧化钠溶液增加的质量等于C组,说明产生二氧化碳的速率与石块中碳酸钙的质量分数无关。但有同学指出该组对比实验的结论不合理,写出可能的原因__________ 。
(3)对比C组和D组实验:观察到C组产生气体使氢氧化钠溶液增加的质量小于D组,说明石块颗粒越小,石块与稀盐酸的接触面积越大,产生二氧化碳的速率越快。
【反思提升】小明同学分别设计了下列3组实验,并通过数字化仪器测量实验中 质量随时间变化的关系如图2所示,其中符合曲线B的实验是
质量随时间变化的关系如图2所示,其中符合曲线B的实验是______ (填实验序号)
① 块状大理石+
块状大理石+ 溶质质量分数为10%的稀盐酸
溶质质量分数为10%的稀盐酸
② 块状大理石+
块状大理石+ 溶质质量分数为20%的稀盐酸
溶质质量分数为20%的稀盐酸
③ 粉末状大理石+
粉末状大理石+ 溶质质量分数为20%的稀盐酸
溶质质量分数为20%的稀盐酸
 的实验时,发现产生气泡的速率都不相同,并对这一现象展开了探究。
的实验时,发现产生气泡的速率都不相同,并对这一现象展开了探究。【提出问题】影响产生二氧化碳气体速率的因素有哪些?
【作出猜想】猜想一:稀盐酸的浓度
猜想二:石块中碳酸钙的质量分数
猜想三:石块颗粒大小
【实验设计】为验证上述猜想,同学们设计了如图1所示的实验装置进行探究。将各试管生成的气体分别通入到足量相同体积、相同浓度的氢氧化钠溶液中,称量相同反应时间内各组氢氧化钠溶液增加的质量。

(1)对A组和B组实验:双察到A组产生气体使氢氧化钠溶液增加的质量小于B组;验证了猜想
(2)对比B组和C组实验:观察到B组产生气体使氢氧化钠溶液增加的质量等于C组,说明产生二氧化碳的速率与石块中碳酸钙的质量分数无关。但有同学指出该组对比实验的结论不合理,写出可能的原因
(3)对比C组和D组实验:观察到C组产生气体使氢氧化钠溶液增加的质量小于D组,说明石块颗粒越小,石块与稀盐酸的接触面积越大,产生二氧化碳的速率越快。
【反思提升】小明同学分别设计了下列3组实验,并通过数字化仪器测量实验中
 质量随时间变化的关系如图2所示,其中符合曲线B的实验是
质量随时间变化的关系如图2所示,其中符合曲线B的实验是①
 块状大理石+
块状大理石+ 溶质质量分数为10%的稀盐酸
溶质质量分数为10%的稀盐酸②
 块状大理石+
块状大理石+ 溶质质量分数为20%的稀盐酸
溶质质量分数为20%的稀盐酸③
 粉末状大理石+
粉末状大理石+ 溶质质量分数为20%的稀盐酸
溶质质量分数为20%的稀盐酸
您最近一年使用:0次
2 . 已知胃酸的主要成分是盐酸,能与含有碳酸钙的补钙剂发生化学反应。如图2为某钙片的商品标签,为测定钙片中钙元素的质量分数(假设钙片中其他物质不含钙元素,且不溶于水,也不与任何物质发生反应),某化学兴趣小组取20片钙片,进行如下实验:
(1)实验过程中“研碎”和食用方法中“嚼食”都能加快化学反应速率,其原因是____________ 。
(2)计算上述实验过程中所得滤液的质量______ 。(写出计算过程)
(3)钙片中钙元素的质量分数为______ 。
(1)实验过程中“研碎”和食用方法中“嚼食”都能加快化学反应速率,其原因是
(2)计算上述实验过程中所得滤液的质量
(3)钙片中钙元素的质量分数为

您最近一年使用:0次
3 . 查阅资料得知:过氧化钠( )可与
)可与 或
或 反应生成
反应生成 ,反应原理为:
,反应原理为: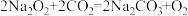 ,
, 。某科学兴趣小组同学设计了如图所示实验,说明
。某科学兴趣小组同学设计了如图所示实验,说明 可在呼吸面具和潜水艇中做供氧剂。
可在呼吸面具和潜水艇中做供氧剂。______ 。
(2)为了除去二氧化碳中混有的氯化氢气体,装置B中盛装的乙溶液是______ 。
(3)装置D用于除去末被装置C转化的(CO2,便于后续气体检验,则D中发生反应的化学方程式是____________ 。
(4)装置E的试管中收集到的气体来自于哪些物质相互反应?______ 。
 )可与
)可与 或
或 反应生成
反应生成 ,反应原理为:
,反应原理为: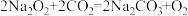 ,
, 。某科学兴趣小组同学设计了如图所示实验,说明
。某科学兴趣小组同学设计了如图所示实验,说明 可在呼吸面具和潜水艇中做供氧剂。
可在呼吸面具和潜水艇中做供氧剂。
(2)为了除去二氧化碳中混有的氯化氢气体,装置B中盛装的乙溶液是
(3)装置D用于除去末被装置C转化的(CO2,便于后续气体检验,则D中发生反应的化学方程式是
(4)装置E的试管中收集到的气体来自于哪些物质相互反应?
您最近一年使用:0次
4 . 化学实验是科学探究的重要手段,请根据下列装置图回答问题。______ 。
(2)用高锰酸钾制取较纯净的氧气,应选用装置______ ,反应的化学方程式为____________ ,实验过程中发现水槽中的水变红了原因可能是______ 。
(3)实验室制取 选用装置C的优点是
选用装置C的优点是______ ,化学反应方程式为______ 。
(4)长途运输鱼苗时,在水中加入少量过氧化钙 ,通过过氧化钙和水反应生成氧气溶解在水中,供鱼苗呼吸,请对其化学反应方程式配平:
,通过过氧化钙和水反应生成氧气溶解在水中,供鱼苗呼吸,请对其化学反应方程式配平:______ 
______ 
______ 
______ 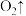 。
。

(2)用高锰酸钾制取较纯净的氧气,应选用装置
(3)实验室制取
 选用装置C的优点是
选用装置C的优点是(4)长途运输鱼苗时,在水中加入少量过氧化钙
 ,通过过氧化钙和水反应生成氧气溶解在水中,供鱼苗呼吸,请对其化学反应方程式配平:
,通过过氧化钙和水反应生成氧气溶解在水中,供鱼苗呼吸,请对其化学反应方程式配平:


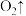 。
。
您最近一年使用:0次
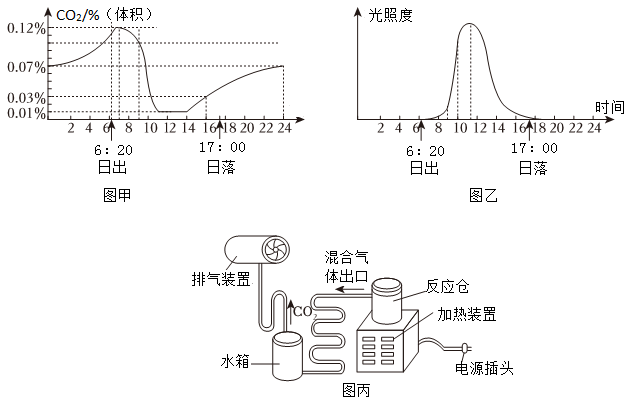
5 . 二氧化碳是光合作用的原料,当二氧化碳浓度太低时,植物的光合作用速率会减低甚至停止。图甲是自然状态下大棚内二氧化碳浓度随时间变化的曲线图,日出后随着光照的增强三氧化碳浓度不断降低。图乙为一天中光照强度随时间的变化曲线。为提高棚内蔬菜瓜果的产量,人们常常向大棚内补充二氧化碳,以增强光合作用的强度。________ (填结构)离开植物体内,进入大气。但是白天二氧化碳的浓度又会下降,结合图甲、图乙,分析从7:00到11·00大棚内二氧化碳浓度变化的原因________ 。
(2)图丙是一种“二氧化碳发生器”的装置图,在反应仓内放入原料碳酸氢铵(NH4HCO3),启动加热装置后发生化学反应:NH4HCO3→NH3↑+CO2↑+H20。反应生成的混合气体进入水箱,其中氨气(NH3)溶于水并留在水箱中,二氧化碳经过由气管由排气装置排放到大棚的空气中,为棚内蔬菜提供光合作用所需的原料。结合下表中氨气与二氧化碳在水中的溶解度,解释氨气留在水箱中而二氧化碳逸出的原因__________________________________________________ 。
(3)大棚内装有二氧化碳浓度及光感双控装置,当棚内二氧化碳浓度值低于0.1%时加热装置自动启动,分解NH4HCO3,产生二氧化碳,使大棚内二氧化碳维持在0.1%-0.12%;日落时光照减弱,加热装置自动关闭,停止产生二氧化碳。已知该二氧化碳发生器中碳酸氢铵的分解速率为0.79千克/小时,请结合图甲计算该二氧化碳发生器一天中产生二氧化碳的质量为________ 千克。
(2)图丙是一种“二氧化碳发生器”的装置图,在反应仓内放入原料碳酸氢铵(NH4HCO3),启动加热装置后发生化学反应:NH4HCO3→NH3↑+CO2↑+H20。反应生成的混合气体进入水箱,其中氨气(NH3)溶于水并留在水箱中,二氧化碳经过由气管由排气装置排放到大棚的空气中,为棚内蔬菜提供光合作用所需的原料。结合下表中氨气与二氧化碳在水中的溶解度,解释氨气留在水箱中而二氧化碳逸出的原因
| 溶解物质/温度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| NH₃ | 89.9 | 68.3 | 52.9 | 40.9 | 31.6 |
| CO₂ | 0.33 | 0.23 | 0.17 | 0.13 | 0.1 |
您最近一年使用:0次
6 . 小科组装了如下装置来制取二氧化碳气体,该装置的优点是能使反应随时进行或停止。为了解装置具有该优点的原因,他在装置中连接了压强传感器,从而测定实验中试管内气体压强变化的情况(如图),回答下列问题:________ ;
(2)图中曲线的a点对应的操作是________ ;
(3)曲线中bc段压强保持不变的原因________ 。

(2)图中曲线的a点对应的操作是
(3)曲线中bc段压强保持不变的原因
您最近一年使用:0次
7 . 如图所示为科学实验中的“多功能”装置:__________ 端通入;
(2)若要用来检验二氧化碳气体,则瓶中所盛放液体的化学式是__________
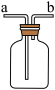
(2)若要用来检验二氧化碳气体,则瓶中所盛放液体的化学式是
您最近一年使用:0次
8 . 海洋封存是实现“碳中和”的途径之一,其原理是利用水等液体吸收CO2实现减碳目标。某科学小组对“二氧化碳气体的收集”这一课题开展了探究。
【提出问题】二氧化碳气体在水和食盐水中溶解能力相同吗?
【建立建设】二氧化碳气体在食盐水中溶解能力更强。
【实验设计与操作】
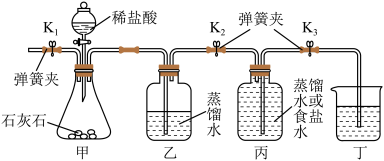
(1)实验时,需先将甲装置中的空气排尽。其操作是:打开弹簧夹K1,关闭弹簧夹K2,打开活塞,滴加稀盐酸至空气排尽。检验空气已排尽的方法是__________ 。
(2)关闭K1,打开K2、K3,分别用排水法、排食盐水法收集CO2,且每隔一段时间测出丁烧杯中液体的体积,测得数据如下:
根据以上数据分析,能用排水法收集CO2的理由是_________ 。
【实验结论】相同条件下,二氧化碳在_________ 中溶解能力更强。
(3)小组同学想了解水吸收CO2后溶液的酸碱性情况,在实验中做了以下操作,待丙装置中收集半瓶气体时,关闭活塞K2和K3,充分振荡丙装置。然后用pH计测得如下数据:
分析可知,在丙和丁装置中所溶解二氧化碳的体积___________ (选填“大于”、“小于”或“等于”)丙和丁装置中溶液的总体积。
【实验反思】海洋封存CO2后可能会带来哪些危害?_________ (写出一点即可)
【提出问题】二氧化碳气体在水和食盐水中溶解能力相同吗?
【建立建设】二氧化碳气体在食盐水中溶解能力更强。
【实验设计与操作】
(1)实验时,需先将甲装置中的空气排尽。其操作是:打开弹簧夹K1,关闭弹簧夹K2,打开活塞,滴加稀盐酸至空气排尽。检验空气已排尽的方法是
(2)关闭K1,打开K2、K3,分别用排水法、排食盐水法收集CO2,且每隔一段时间测出丁烧杯中液体的体积,测得数据如下:
| 时间/min | 0 | 0.5 | 6 | 12 | 24 | 48 |
| 排水法时丁中水的体积/mL | 0 | 2.5 | 14.5 | 23 | 34 | 41 |
| 排盐水法时丁中盐水的体积/mL | 0 | 1 | 7 | 9.5 | 11 | 12 |
【实验结论】相同条件下,二氧化碳在
(3)小组同学想了解水吸收CO2后溶液的酸碱性情况,在实验中做了以下操作,待丙装置中收集半瓶气体时,关闭活塞K2和K3,充分振荡丙装置。然后用pH计测得如下数据:
| 物质 | 丁装置中溶液 | 丙装置中溶液 |
| pH | 6.50 | 5.60 |
【实验反思】海洋封存CO2后可能会带来哪些危害?
您最近一年使用:0次
9 . 在探究二氧化碳性质时,用空矿泉水瓶采用排空气法收集一瓶CO2气体,再倒入一定量的水,盖紧瓶盖,振荡一段时间后瓶子并未出现明显压瘪的现象。该实验引发了同学们对排空气法收集CO2的纯度及CO2收集方法的思考,为此他们开展了实验。
小组同学用如图所示的装置制取CO2,分别用排空气法和排水法收集1瓶CO2气体(集气瓶容积相同),记录所需时间,并用氧气传感器测出两瓶气体中氧气的体积分数,结果如表格所示。
(1)每次收集气体时,需要反应一段时间后再开始收集,其原因是________ 。
(2)若空气中氧气体积分数以20%计算,则排水法收集的气体中CO2体积分数约为________ 。
(3)通过实验数据分析,同学们发现实验室也可以采用排水法收集CO2,其依据是________ 。
小组同学用如图所示的装置制取CO2,分别用排空气法和排水法收集1瓶CO2气体(集气瓶容积相同),记录所需时间,并用氧气传感器测出两瓶气体中氧气的体积分数,结果如表格所示。
收集方法 | 排空气法 | 排水法 |
收集时间 | 1分57秒 | 43秒 |
气体中氧气的体积分数 | 5.8% | 2.5% |
(2)若空气中氧气体积分数以20%计算,则排水法收集的气体中CO2体积分数约为
(3)通过实验数据分析,同学们发现实验室也可以采用排水法收集CO2,其依据是

您最近一年使用:0次
10 . 化验员对某市售补钙剂进行检验,想测定其含量是否达标,如图是某补钙药品的部分说明书。在实验室中取10片钙片研碎后放于烧杯中,将100g稀盐酸分五次依次加入烧杯中,并不断搅拌,称量,将得到的有关数据记录如下(钙片中其它成分不与稀盐酸反应):
(1)完全反应后,产生二氧化碳的质量为______ g。
(2)试通过计算说明(写出具体计算过程)①该品牌钙片含量是否达标_______
(3)如果按用量服用,服用者每天通过该补钙剂摄入钙元素的质量为______ g。
稀盐酸的质量/g | 0 | 20 | 40 | 60 | 80 | 100 |
烧杯中剩余物质质量/g | 10 | 29.12 | 48.24 | 67.36 | 86.48 | 106.48 |

(1)完全反应后,产生二氧化碳的质量为
(2)试通过计算说明(写出具体计算过程)①该品牌钙片含量是否达标
(3)如果按用量服用,服用者每天通过该补钙剂摄入钙元素的质量为
您最近一年使用:0次



