名校
1 . 浓差电池是一种利用电解质溶液浓度差产生电势差而形成的电池,理论上当电解质溶液的浓度相等时停止放电。图1为浓差电池,图2为电渗析法制备磷酸二氢钠,用浓差电池为电源完成电渗析法制备磷酸二氢钠。下列说法正确的是
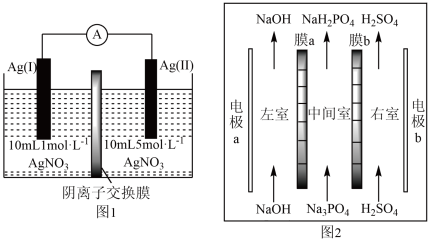
| A.电极Ag(II)的电极反应式为:Ag-e-=Ag+ |
| B.电渗析装置中膜a、b均为阳离子交换膜 |
| C.电渗析过程中左室中NaOH浓度增大,右室H2SO4的浓度减小 |
| D.电池从开始到停止放电,理论上可制备2.4gNaH2PO4 |
您最近半年使用:0次
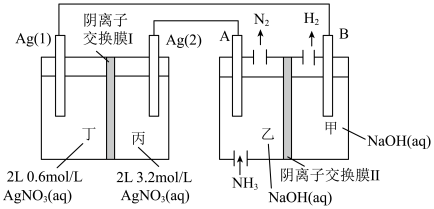
2 . 以 浓差电池(电解质溶液浓度不同形成的电池)为电源,以石墨为电极将
浓差电池(电解质溶液浓度不同形成的电池)为电源,以石墨为电极将 转化为较高纯度的
转化为较高纯度的 装置如图所示。下列说法正确的是
装置如图所示。下列说法正确的是
 浓差电池(电解质溶液浓度不同形成的电池)为电源,以石墨为电极将
浓差电池(电解质溶液浓度不同形成的电池)为电源,以石墨为电极将 转化为较高纯度的
转化为较高纯度的 装置如图所示。下列说法正确的是
装置如图所示。下列说法正确的是
A.电极A上的反应为 |
| B.由于存在阴离子交换膜,电解过程中乙池溶液pH不变 |
C.当产生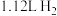 (标况)时,丙室中电解质溶液质量减少17g (标况)时,丙室中电解质溶液质量减少17g |
D.电池停止工作后,若要使电池恢复到初始状态,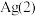 连接的是电源负极 连接的是电源负极 |
您最近半年使用:0次
名校
3 . 用一种具有“卯榫”结构的双极膜组装电解池(下图),可实现大电流催化电解KNO3溶液制氨。工作时H2O在双极膜界面处被催化解离成H+和OH-,有利于电解反应顺利进行。下列说法错误的是
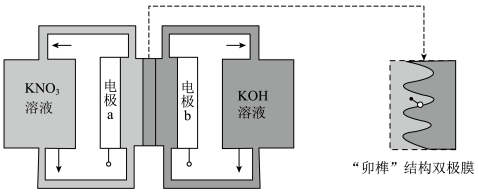

| A.相比于平面结构双极膜,“卯榫”结构可提高氮生成速率 |
B.阴极反应式为 +7H2O+8e-=NH3·H2O+9OH- +7H2O+8e-=NH3·H2O+9OH- |
| C.每生成1molNH3·H2O,双极膜界面处产生9mol的H+移向电极a |
| D.电解过程中,阳极室中KOH的物质的量不因反应而改变 |
您最近半年使用:0次
名校
4 . 由于存在同种电解质溶液的浓度差而产生电动势的电池称为浓差电池。利用浓差电池电解硫酸钠溶液可以制得氧气、氢气、硫酸和氢氧化钠,其装置如图所示(a、b电极均为石墨电极,已知:溶液A为1L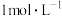
 溶液;溶液B为1L
溶液;溶液B为1L 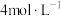
 溶液)。下列说法不正确的是
溶液)。下列说法不正确的是

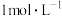
 溶液;溶液B为1L
溶液;溶液B为1L 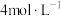
 溶液)。下列说法不正确的是
溶液)。下列说法不正确的是
A.电池放电过程中Ag(2)为正极,电极反应为 |
B.b电极为电解池阴极,电极反应式为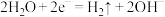 |
| C.c、d离子交换膜依次为阴离子交换膜、阳离子交换膜 |
D.电池从开始工作到停止放电,电解池理论上可制得80g  |
您最近半年使用:0次
2024-01-21更新
|
617次组卷
|
2卷引用:山西省吕梁市孝义市2023-2024学年高二上学期12月月考化学试题
名校
5 . 科学家通过自由基电解法合成羧酸,如 先在涂有活性银纳米颗粒和特殊配体的阴极断裂成自由基
先在涂有活性银纳米颗粒和特殊配体的阴极断裂成自由基 和
和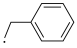 ,再与
,再与 反应转化为相应的羧酸,装置如图所示。下列说法不正确的是
反应转化为相应的羧酸,装置如图所示。下列说法不正确的是
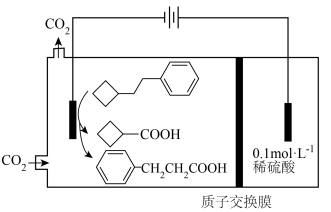
 先在涂有活性银纳米颗粒和特殊配体的阴极断裂成自由基
先在涂有活性银纳米颗粒和特殊配体的阴极断裂成自由基 和
和 ,再与
,再与 反应转化为相应的羧酸,装置如图所示。下列说法不正确的是
反应转化为相应的羧酸,装置如图所示。下列说法不正确的是
A.电压不变,用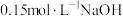 溶液替换阳极室的稀硫酸,生产效率不变 溶液替换阳极室的稀硫酸,生产效率不变 |
B.活性银纳米颗粒和特殊配体阻止了 得电子生成 得电子生成 |
C.阴极电极反应有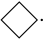 +CO2+e-+H+= +CO2+e-+H+=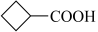 |
| D.同温同压下,阴、阳两极涉及的气体的体积之比为4:1 |
您最近半年使用:0次
名校
解题方法
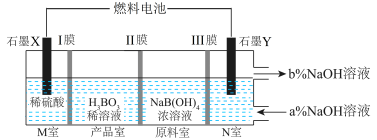
6 . 以甲烷燃料电池为电源电解 溶液制备
溶液制备 工作原理如图所示。下列说法正确的是
工作原理如图所示。下列说法正确的是
 溶液制备
溶液制备 工作原理如图所示。下列说法正确的是
工作原理如图所示。下列说法正确的是
A.N室中: |
| B.燃料电池通入氧气的电极接电解池的Y电极 |
| C.I、Ⅲ膜为阴离子交换膜,Ⅱ膜为阳离子交换膜 |
D.理论上每生成 产品,需消耗甲烷的体积为 产品,需消耗甲烷的体积为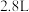 (标准状况) (标准状况) |
您最近半年使用:0次
2023-11-16更新
|
683次组卷
|
3卷引用:江苏省苏州市实验中学2023-2024学年高二上学期10月月考化学试题
名校
7 . 电解硫酸钠溶液制取电池正极材料 的前驱体
的前驱体 ,其工作原理如图所示:
,其工作原理如图所示:
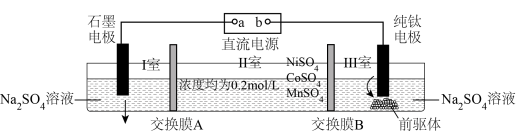
下列说法不正确 的是
 的前驱体
的前驱体 ,其工作原理如图所示:
,其工作原理如图所示:
下列说法
| A.a是直流电源的正极,石墨电极发生氧化反应 |
| B.交换膜A是阴离子交换膜,通电一段时间,Ⅰ室pH降低 |
C.当产生 的 的 时,标准状况下纯钛电极上至少产生 时,标准状况下纯钛电极上至少产生 气体 气体 |
| D.若将纯钛电极直接放入Ⅱ室,则纯钛电极上会有金属与前驱体附着而使产率降低 |
您最近半年使用:0次
2023-11-15更新
|
2311次组卷
|
6卷引用:浙江省宁波市2023-2024学年高三上学期选考模拟考试化学试题
浙江省宁波市2023-2024学年高三上学期选考模拟考试化学试题化学02(15+4模式)2024年1月“九省联考”考前化学猜想卷湖南省衡阳市第八中学2023-2024学年高三上学期1月月考化学(已下线)热点14 电化学及其应用(已下线)专题05 化学反应与能量(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)2024届湖南省长沙市第一中高三下学期高考适应性演练(一)化学试题
8 . 以四甲基氯化铵[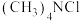 ]水溶液为原料,利用光伏并网发电装置制备四甲基氢氧化铵[
]水溶液为原料,利用光伏并网发电装置制备四甲基氢氧化铵[ ],下列叙述不正确的是
],下列叙述不正确的是

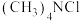 ]水溶液为原料,利用光伏并网发电装置制备四甲基氢氧化铵[
]水溶液为原料,利用光伏并网发电装置制备四甲基氢氧化铵[ ],下列叙述不正确的是
],下列叙述不正确的是
| A.a极电极发生还原反应 |
B.保持电流恒定,增大NaCl稀溶液浓度,制备 的反应速率增大 的反应速率增大 |
| C.c为阳离子交换膜,d为阴离子交换膜 |
| D.b极收集2.24L(标况)气体时,溶液中有0.4mol离子透过交换膜 |
您最近半年使用:0次
名校
解题方法
9 . 设计如图所示装置回收金属钴。保持细菌所在环境pH稳定,借助其降解乙酸盐生成CO2,将废旧锂离子电池的正极材料LiCoO2(s)转化为Co2+,工作时保持厌氧环境,并定时将乙室溶液转移至甲室。已知电极材料均为石墨材质,右侧装置为原电池。下列说法错误的是
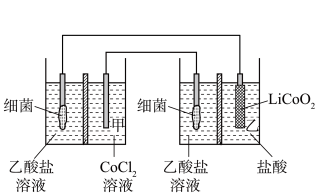

| A.为了保持细菌所在环境pH稳定,两侧都应选择质子交换膜 |
| B.乙室电极反应式为LiCoO2+e-+4H+=Co2++Li++2H2O |
| C.装置工作一段时间后,乙室的pH在减小 |
| D.若甲室Co2+减少150mg,乙室Co2+增加200mg,则此时已进行过溶液转移 |
您最近半年使用:0次
名校
10 . 电化学原理在工业生产及生活中发挥着巨大的作用。
Ⅰ.利用微电解技术可以处理工业废水,如酸性含铬废水(主要含有Cr2O )。原理是利用电极反应物与某些污染物反应,从而达到去除污物的作用。
)。原理是利用电极反应物与某些污染物反应,从而达到去除污物的作用。
(1)通常以铁板和石墨作为电极材料,应选________ 作阴极。
(2)废水中的Cr2O 通过反应转化为Cr3+,此过程的离子反应方程式为
通过反应转化为Cr3+,此过程的离子反应方程式为________ ,最终Cr3+以Cr(OH)3形式除去。
(3)当电路中每转移1.2mol电子,最多有________ mol Cr2O 参加反应。
参加反应。
Ⅱ.红矾钠(Na2Cr2O7•2H2O)是一种重要的化工原料。利用膜电解技术(装置如图所示),以Na2CrO4为主要原料制备Na2Cr2O7的总反应方程式为:4Na2CrO4+4H2O 2Na2Cr2O7+4NaOH+2H2↑+O2↑。
2Na2Cr2O7+4NaOH+2H2↑+O2↑。
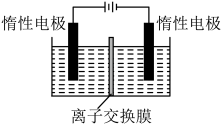
(4)电解时应选择________ (填“阴”“阳”)离子交换膜。阳极区的反应有________ ,NaOH在________ (填“阴”或“阳”)极室制得。
Ⅲ.用C3H8、O2和熔融Na2CO3组成的燃料电池作电源,电解饱和的K2S溶液和2mol•L-1AgNO3溶液制备某些单质,盐桥中充有饱和的KNO3溶液。
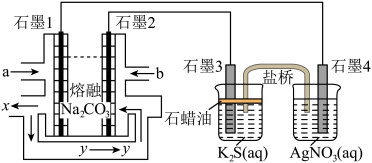
(5)石墨1电极反应式为________ ,物质y为________ 。
(6)若此装置通入C3H8的体积为2.24L(标准状况下),则可以制取单质硫的质量为________ 。
Ⅰ.利用微电解技术可以处理工业废水,如酸性含铬废水(主要含有Cr2O
 )。原理是利用电极反应物与某些污染物反应,从而达到去除污物的作用。
)。原理是利用电极反应物与某些污染物反应,从而达到去除污物的作用。(1)通常以铁板和石墨作为电极材料,应选
(2)废水中的Cr2O
 通过反应转化为Cr3+,此过程的离子反应方程式为
通过反应转化为Cr3+,此过程的离子反应方程式为(3)当电路中每转移1.2mol电子,最多有
 参加反应。
参加反应。Ⅱ.红矾钠(Na2Cr2O7•2H2O)是一种重要的化工原料。利用膜电解技术(装置如图所示),以Na2CrO4为主要原料制备Na2Cr2O7的总反应方程式为:4Na2CrO4+4H2O
 2Na2Cr2O7+4NaOH+2H2↑+O2↑。
2Na2Cr2O7+4NaOH+2H2↑+O2↑。
(4)电解时应选择
Ⅲ.用C3H8、O2和熔融Na2CO3组成的燃料电池作电源,电解饱和的K2S溶液和2mol•L-1AgNO3溶液制备某些单质,盐桥中充有饱和的KNO3溶液。

(5)石墨1电极反应式为
(6)若此装置通入C3H8的体积为2.24L(标准状况下),则可以制取单质硫的质量为
您最近半年使用:0次



