解题方法
1 . 高锰酸钾是一种常用的强氧化剂,在临床医学上可以用作消毒剂,可以杀菌止痛。如图是电化学法制备高锰酸钾的装置图。下列说法正确的是


| A.中间的离子交换膜是阴离子交换膜 |
| B.每转移1mol电子,Y极放出112mL气体 |
C.X极的电极反应式为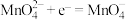 |
D.当有2mol电子转移时,氧化产物与还原产物的比值为 |
您最近半年使用:0次
2 .  是一种高效、安全的消毒用品。某电解法制备
是一种高效、安全的消毒用品。某电解法制备 的装置如图,有关说法错误的是
的装置如图,有关说法错误的是
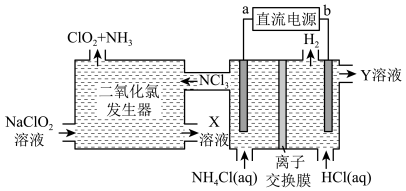
| A.与a相连的电极上发生氧化反应 |
B.电解过程中转移 电子时,有 电子时,有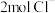 通过离子交换膜进入阳极区 通过离子交换膜进入阳极区 |
C.整个生产过程中,理论上得到两种气体产物 和 和 的体积比为 的体积比为 |
D.“二氧化氯发生器”中生成的X溶液的主要溶质为 和 和 |
您最近半年使用:0次
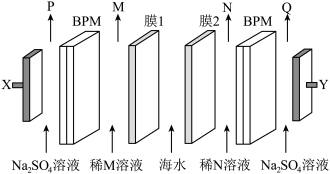
3 . 某海水淡化装置如图所示,获得淡水的同时可生产盐酸、 等基本化工原料。已知相同时间内产生气体P、Q物质的量之比为2:1(BPM为双极膜,在直流电场的作用下,可作为
等基本化工原料。已知相同时间内产生气体P、Q物质的量之比为2:1(BPM为双极膜,在直流电场的作用下,可作为 和
和 离子源)。下列说法正确的是
离子源)。下列说法正确的是
 等基本化工原料。已知相同时间内产生气体P、Q物质的量之比为2:1(BPM为双极膜,在直流电场的作用下,可作为
等基本化工原料。已知相同时间内产生气体P、Q物质的量之比为2:1(BPM为双极膜,在直流电场的作用下,可作为 和
和 离子源)。下列说法正确的是
离子源)。下列说法正确的是
| A.若装置与外接电源正负极反接,可同样起到海水淡化的作用 |
| B.膜1、膜2分别为阳离子交换膜、阴离子交换膜 |
C.每生成2.24LQ气体,理论上除盐(以 计)23.4g 计)23.4g |
D.阳极发生的电极反应为 |
您最近半年使用:0次
4 . 一种以钒基氧化物(V6O13)为正极材料的水系锌离子电池的工作原理如图所示。通过使用孔径大小合适且分布均匀的新型离子交换膜,可提高离子传输通量的均匀性,从而保持电池的稳定性。下列说法正确的是
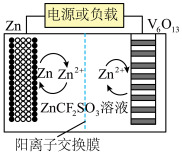
A.放电过程中,Zn2+向 极一侧移动 极一侧移动 |
B.放电过程中,电子由 极经电解质溶液向V6O13极移动 极经电解质溶液向V6O13极移动 |
| C.充电时,V6O13极与外接直流电源正极相连 |
D.充电时,阳极发生的电极反应可能为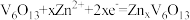 |
您最近半年使用:0次
5 . 一氯甲烷主要用于生产甲基氯硅烷,一氯乙烯主要用于生产聚氯乙烯等高聚物,1,2-二氯乙烷常用作有机溶剂和化工原料。回答下列问题:
I.在加热或光照条件下,“甲烷一氯气”法得到一氯甲烷是按自由基机理进行的,即CH4(g)+Cl2(g) CH3Cl(g)+HCl(g) △H。该反应涉及两个基元步骤①②,其相对能量一反应历程图如图:
CH3Cl(g)+HCl(g) △H。该反应涉及两个基元步骤①②,其相对能量一反应历程图如图:
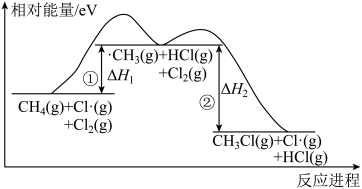
(1)已知H3C-H键能为4.56eV,H-Cl键能为4.46eV,1eV相当于96.5kJ/mol。则步骤①的焓变△H1=_______ kJ/mol;一氯取代反应的总焓变△H=______ (用△H1、△H2表示)。
Ⅱ.一氯乙烯(CH2=CHC1)的工业生产方法之一是乙烯氯化裂解法,该方法分以下两个过程进行:
乙烯氯化加成:CH2=CH2(g)+Cl2(g) ClCH2CH2Cl(g) △H1=-171.7kJ/mol
ClCH2CH2Cl(g) △H1=-171.7kJ/mol
1,2-二氯乙烷裂解:ClCH2CH2Cl(g) CH2=CHCl(g)+HCl(g) △H2=+73.4kJ/mol
CH2=CHCl(g)+HCl(g) △H2=+73.4kJ/mol
(2)乙烯氯化加成反应在热力学上进行的趋势很大,原因是______ 。1,2-二氯乙烷裂解反应的△S=+145.7J mol/K,则该裂解反应能自发进行的最低温度约为
mol/K,则该裂解反应能自发进行的最低温度约为______ K(保留整数)。
(3)在某恒压密闭容器中通入一定量的ClCH2CH2Cl(g),仅发生1,2-二氯乙烷裂解生成氯乙烯和氯化氢,实验测得ClCH2CH2Cl(g)的转化率随温度和反应时间的关系如图所示。

①T1、T2、T3的大小关系为_______ ,原因是_______ 。
②若M点刚好达到平衡状态,则N点的v正_____ v逆(填“大于”“小于”或“等于”)。Ka是以物质的量分数表示的平衡常数,则T2温度下1,2-二氯乙烷裂解生成氯乙烯和氯化氢的反应的Kx=_____ 保留2位小数)。
Ⅲ.一种电化学合成1,2-二氯乙婉的实验装置如图所示
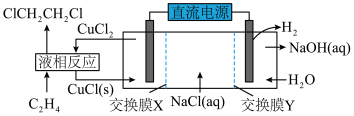
(4)交换膜X是______ 离子交换膜(填“阴”或“阳”),该实验装置合成1,2-二氯乙烷的总反应的化学方程式为______ 。
I.在加热或光照条件下,“甲烷一氯气”法得到一氯甲烷是按自由基机理进行的,即CH4(g)+Cl2(g)
 CH3Cl(g)+HCl(g) △H。该反应涉及两个基元步骤①②,其相对能量一反应历程图如图:
CH3Cl(g)+HCl(g) △H。该反应涉及两个基元步骤①②,其相对能量一反应历程图如图:
(1)已知H3C-H键能为4.56eV,H-Cl键能为4.46eV,1eV相当于96.5kJ/mol。则步骤①的焓变△H1=
Ⅱ.一氯乙烯(CH2=CHC1)的工业生产方法之一是乙烯氯化裂解法,该方法分以下两个过程进行:
乙烯氯化加成:CH2=CH2(g)+Cl2(g)
 ClCH2CH2Cl(g) △H1=-171.7kJ/mol
ClCH2CH2Cl(g) △H1=-171.7kJ/mol1,2-二氯乙烷裂解:ClCH2CH2Cl(g)
 CH2=CHCl(g)+HCl(g) △H2=+73.4kJ/mol
CH2=CHCl(g)+HCl(g) △H2=+73.4kJ/mol(2)乙烯氯化加成反应在热力学上进行的趋势很大,原因是
 mol/K,则该裂解反应能自发进行的最低温度约为
mol/K,则该裂解反应能自发进行的最低温度约为(3)在某恒压密闭容器中通入一定量的ClCH2CH2Cl(g),仅发生1,2-二氯乙烷裂解生成氯乙烯和氯化氢,实验测得ClCH2CH2Cl(g)的转化率随温度和反应时间的关系如图所示。

①T1、T2、T3的大小关系为
②若M点刚好达到平衡状态,则N点的v正
Ⅲ.一种电化学合成1,2-二氯乙婉的实验装置如图所示

(4)交换膜X是
您最近半年使用:0次
2024-03-18更新
|
115次组卷
|
2卷引用:河北省石家庄市辛集中学、衡水中学2023-2024高三上学期期末联考化学试题
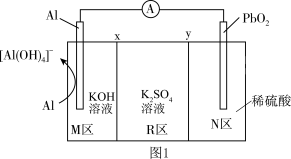
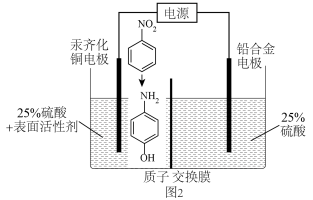
6 . 对氨基苯酚可用作农药、医药、染料等精细化学品的中间体,利用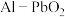 电池(其装置如图1所示)作为电源电解硝基苯制备对氨基苯酚,其装置如图2所示。已知反应过程中
电池(其装置如图1所示)作为电源电解硝基苯制备对氨基苯酚,其装置如图2所示。已知反应过程中 溶液浓度增大,下列说法错误的是
溶液浓度增大,下列说法错误的是
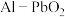 电池(其装置如图1所示)作为电源电解硝基苯制备对氨基苯酚,其装置如图2所示。已知反应过程中
电池(其装置如图1所示)作为电源电解硝基苯制备对氨基苯酚,其装置如图2所示。已知反应过程中 溶液浓度增大,下列说法错误的是
溶液浓度增大,下列说法错误的是

A. 通过 通过 膜移向 膜移向 区 区 |
B.铅合金电极应与 电极相连 电极相连 |
C.消耗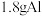 时, 时, 区域电解质溶液质量减少 区域电解质溶液质量减少 |
D.汞齐化铜电极的反应式为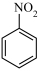 +4H++4e- +4H++4e- 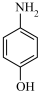 +H2O +H2O |
您最近半年使用:0次
名校
7 . 利用如图装置处理碱性含CN-的废水,同时淡化海水(用NaCl溶液模拟海水),a电极和b电极均为惰性电极。下列说法错误的是
已知:阳极区溶液中离子放电顺序为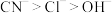 ,(未配平)。
,(未配平)。

已知:阳极区溶液中离子放电顺序为
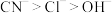 ,(未配平)。
,(未配平)。
A.CN-在阳极发生的电极反应为 |
| B.通电过程中阴极区溶液pH不断增大 |
| C.隔膜1为阴离子交换膜,隔膜2为阳离子交换膜 |
| D.将1molCN-完全转化成无污染物质时,外电路中至少需要转移4mol电子 |
您最近半年使用:0次
名校
8 . 氯碱工业是一种高耗能产业,一种将燃料电池与电解池组合的新工艺可节能30%以上,下图是该工艺图示(电极未标出),下列说法正确的是
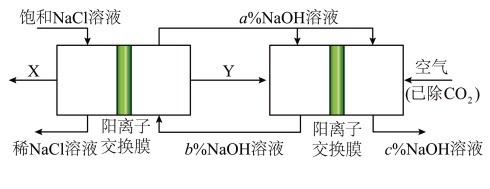
| A.右池为电解池,Y为H2 |
B.通入空气的电极反应式为: |
| C.a>b>c |
| D.两池的钠离子均从左往右侧移动 |
您最近半年使用:0次
名校
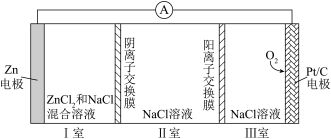
9 . 一种可充电锌—空气电池放电时的工作原理如下图所示、已知:I室溶液中,锌主要以[Zn(H2O)6]2+的形式存在,并存在电离平衡[Zn(H2O)6]2+ [Zn(H2O)5OH]++4H+。下列说法错误的是
[Zn(H2O)5OH]++4H+。下列说法错误的是
 [Zn(H2O)5OH]++4H+。下列说法错误的是
[Zn(H2O)5OH]++4H+。下列说法错误的是
| A.放电时,I室溶液中[Zn(H2O)5OH]+浓度增大 |
| B.放电时,Ⅱ室中的Cl-通过阴离子交换膜进入I室 |
| C.充放电时,Zn电极的电势均低于Pt/C电极的电势 |
| D.充电时,每生成0.2molO2,Ⅲ室溶液质量理论上减少6.4g |
您最近半年使用:0次
名校
10 . 硼氢化钠( )广泛用于化工生产,常温下能与水反应,易溶于异丙胺(沸点为
)广泛用于化工生产,常温下能与水反应,易溶于异丙胺(沸点为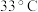 )。工业上可用硼镁矿(主要成分为
)。工业上可用硼镁矿(主要成分为 ,含少量杂质
,含少量杂质 )制取
)制取 ,其工艺流程如下:
,其工艺流程如下:
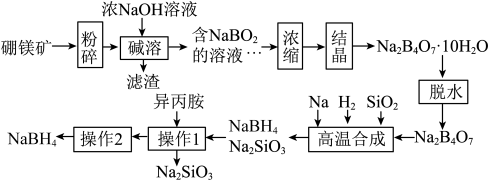
回答下列问题:
(1)粉碎的目的是___________ 。
(2) 的空间结构为
的空间结构为___________ 。
(3)滤渣的成分是___________ 。
(4)高温合成发生的化学反应方程式为___________ ,操作2的名称为___________ ,流程中可循环利用的物质是___________ 。
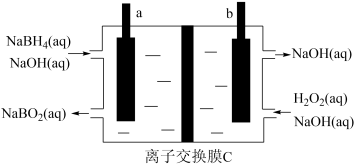
(5)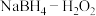 燃料电池有望成为低温环境下工作的便携式燃料电池,其工作原理如图所示。离子交换膜C为
燃料电池有望成为低温环境下工作的便携式燃料电池,其工作原理如图所示。离子交换膜C为___________ 交换膜(填“阳离子”或“阴离子”),a极发生的电极方程式为___________ 。
 )广泛用于化工生产,常温下能与水反应,易溶于异丙胺(沸点为
)广泛用于化工生产,常温下能与水反应,易溶于异丙胺(沸点为 )。工业上可用硼镁矿(主要成分为
)。工业上可用硼镁矿(主要成分为 ,含少量杂质
,含少量杂质 )制取
)制取 ,其工艺流程如下:
,其工艺流程如下:
回答下列问题:
(1)粉碎的目的是
(2)
 的空间结构为
的空间结构为(3)滤渣的成分是
(4)高温合成发生的化学反应方程式为
(5)
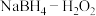 燃料电池有望成为低温环境下工作的便携式燃料电池,其工作原理如图所示。离子交换膜C为
燃料电池有望成为低温环境下工作的便携式燃料电池,其工作原理如图所示。离子交换膜C为
您最近半年使用:0次



