解题方法
1 . 《环境科学》刊发了我国科研部门采用零价铁活化过二硫酸钠(Na2S2O8) 去除废水中的正五价砷[As(V)]的研究成果,其反应机制模型如图所示。下列叙述不正确的是
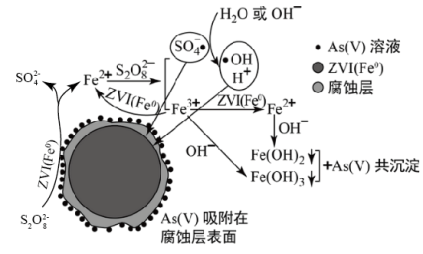

A.56gFe参加反应,消耗的S2O 大于1 mol 大于1 mol |
| B.过二硫酸钠(Na2S2O8) 中S的化合价为+6 |
| C.pH越大,越有利于去除废水中的正五价砷 |
D.碱性条件下,硫酸根自由基发生反应的方程式为:  +H2O= SO +H2O= SO + + +H+ +H+ |
您最近一年使用:0次
名校
2 . 取某固体样品,进行如下实验:
①取一定量的样品,加足量水充分溶解,过滤得到白色滤渣和无色溶液
②取白色滤渣,加入稀盐酸,滤渣全部溶解,同时有气体产生
③取①中无色溶液,通入适量 ,产生白色沉淀
,产生白色沉淀
根据上述实验现象,该固体样品的成分可能是
①取一定量的样品,加足量水充分溶解,过滤得到白色滤渣和无色溶液
②取白色滤渣,加入稀盐酸,滤渣全部溶解,同时有气体产生
③取①中无色溶液,通入适量
 ,产生白色沉淀
,产生白色沉淀根据上述实验现象,该固体样品的成分可能是
A. 、 、 、KOH 、KOH | B. 、 、 、NaCl 、NaCl |
C. 、 、 、NaOH 、NaOH | D. 、 、 、NaOH 、NaOH |
您最近一年使用:0次
2022-01-15更新
|
1134次组卷
|
8卷引用:湖南省祁东县育贤中学2022-2023学年高一上学期第一次月考化学试题
名校
解题方法
3 . Cl2O又称为次氯酸酐,是强氧化剂,易溶于水且与水反应,受热时容易燃烧、高浓度时容易爆炸。其熔沸点分别为-116℃和3.8℃;Cl2的沸点是-34.6℃。现利用HgO和Cl2以及以下装置制备Cl2O:

回答下列问题:
(1)仪器A的名称:___________ 。用酸性高锰酸钾制备Cl2应采用气体发生装置:___________ (填“甲”或“乙”)
(2)②、③中盛放的试剂分别是___________ 、___________ 。
(3)写出HgO和Cl2制备Cl2O的化学方程式:___________ 。
(4)通入干燥空气的目的是___________ 。
(5)实验装置存在一些不足,请指出___________ 。
(6)要想进一步分离得到Cl2O,采用的操作方法是:___________ 。

回答下列问题:
(1)仪器A的名称:
(2)②、③中盛放的试剂分别是
(3)写出HgO和Cl2制备Cl2O的化学方程式:
(4)通入干燥空气的目的是
(5)实验装置存在一些不足,请指出
(6)要想进一步分离得到Cl2O,采用的操作方法是:
您最近一年使用:0次
2021-07-14更新
|
811次组卷
|
7卷引用:湖南省衡阳市第八中学2020-2021学年高一下学期期末考试化学试题
解题方法
4 . 硫酸铁铵[aFe2(SO4) 3·b(NH4) 2SO4·cH2O]广泛用于城镇生活饮用水、工业循环水的净化处理等。某化工厂以硫酸亚铁(含少量硝酸钙)和硫酸铵为原料,设计了如下工艺流程制取硫酸铁铵。

请回答下列问题:
(1)下列物质中最适合的氧化剂B是____________________ ;
a.NaClO b.H2O2c.KMnO4d.K2Cr2O7
反应的离子方程式____________________ 。
(2)上述流程中,用足量最适合的氧化剂B氧化之后和加热蒸发之前,需取少量检验Fe2+是否已全部被氧化,能否用酸性的KMnO4溶液?并说明理由____________________ 。(可用文字或方程式说明)
(3)检验硫酸铁铵中NH 的方法是
的方法是____________________ 。
(4)称取14.00 g所得样品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14 g沉淀;向另一份溶液中加入含0.05 mol Ba (NO3)2的溶液,恰好完全反应。则该硫酸铁铵的化学式为____________________ 。

请回答下列问题:
(1)下列物质中最适合的氧化剂B是
a.NaClO b.H2O2c.KMnO4d.K2Cr2O7
反应的离子方程式
(2)上述流程中,用足量最适合的氧化剂B氧化之后和加热蒸发之前,需取少量检验Fe2+是否已全部被氧化,能否用酸性的KMnO4溶液?并说明理由
(3)检验硫酸铁铵中NH
 的方法是
的方法是(4)称取14.00 g所得样品,将其溶于水配制成100 mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14 g沉淀;向另一份溶液中加入含0.05 mol Ba (NO3)2的溶液,恰好完全反应。则该硫酸铁铵的化学式为
您最近一年使用:0次
2016-12-09更新
|
279次组卷
|
3卷引用:2015届湖南省衡阳市八中高三上学期月考理综化学试卷



