名校
1 . 1869年俄国化学家门捷列夫制出第一张元素周期表。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。回答下列问题:
(1)元素Se在元素周期表中的位置为____________ (写明周期数和族序数),汞是80号元素,原子结构示意图如图,汞在第________________ 周期。

(2)Ge的最高正价为____________ ,Bi的最高价氧化物为____________ (填化学式)。
(3)根据元素周期律推断:
①氢化物稳定性最强的卤族元素是____________ (填元素符号)。
② 、
、 的酸性强弱:
的酸性强弱:
____________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③氢化物的还原性:
____________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4)过渡元素中可以寻找到 (填序号)。
(5)① 常用作溶剂,其电子式为
常用作溶剂,其电子式为____________ ,分子空间构型为____________ 。
②镓( )的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列说法正确的是
)的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列说法正确的是____________ (填序号)。
A.原子半径: B.N的非金属性比O强 C.Ga的金属性比Al弱 D.As和Sb的氧化物可能是两性氧化物
B.N的非金属性比O强 C.Ga的金属性比Al弱 D.As和Sb的氧化物可能是两性氧化物
(6)甲烷可直接应用于燃料电池,该电池采用可传导 的固体氧化物为电解质,其工作原理如图所示:
的固体氧化物为电解质,其工作原理如图所示:
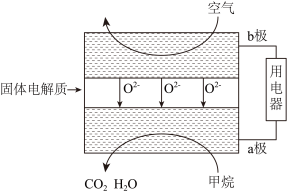
①外电路电子移动方向:__________________ (填“a极到b极”或“b极到a极”)。
②若燃料电池消耗的空气在标准状况下的体积是5.6L(假设空气中 体积分数为20%),则理论上消耗甲烷
体积分数为20%),则理论上消耗甲烷________ mol。
(1)元素Se在元素周期表中的位置为

(2)Ge的最高正价为
(3)根据元素周期律推断:
①氢化物稳定性最强的卤族元素是
②
 、
、 的酸性强弱:
的酸性强弱:
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③氢化物的还原性:

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(4)过渡元素中可以寻找到 (填序号)。
| A.农药 | B.黑色金属 | C.半导体材料 | D.优良的催化剂 |
 常用作溶剂,其电子式为
常用作溶剂,其电子式为②镓(
 )的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列说法正确的是
)的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列说法正确的是A.原子半径:
 B.N的非金属性比O强 C.Ga的金属性比Al弱 D.As和Sb的氧化物可能是两性氧化物
B.N的非金属性比O强 C.Ga的金属性比Al弱 D.As和Sb的氧化物可能是两性氧化物(6)甲烷可直接应用于燃料电池,该电池采用可传导
 的固体氧化物为电解质,其工作原理如图所示:
的固体氧化物为电解质,其工作原理如图所示:
①外电路电子移动方向:
②若燃料电池消耗的空气在标准状况下的体积是5.6L(假设空气中
 体积分数为20%),则理论上消耗甲烷
体积分数为20%),则理论上消耗甲烷
您最近一年使用:0次
名校
2 . 元素周期表体现了元素“位-构-性”的关系,下图是元素周期表的一部分,回答下列问题:
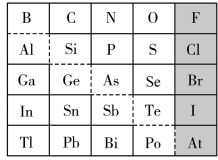
(1)Ga元素的原子结构示意图如图所示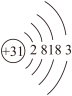 ,则其在元素周期表中的位置为
,则其在元素周期表中的位置为___________ 。
(2)Ge元素位于中金属元素和非金属元素的分界处,其最高正价为___________ ,可作___________ 材料使用;Bi元素的最高价氧化物为___________ (填化学式,下同);I元素的最高价氧化物对应的水化物为___________ 。
(3)以上元素中,失电子能力最强的元素是___________ ,非金属性最强的元素是___________ 。
(4)根据元素周期律等有关知识,推断:
①阴影部分元素对应的氢化物中最稳定的是___________ 。
② 、
、 、
、 、
、 ,四种离子半径由大到小的顺序:
,四种离子半径由大到小的顺序:___________ (用离子符号排序)。
③ 、
、 、
、 的酸性由强到弱的顺序:
的酸性由强到弱的顺序:___________ 。

(1)Ga元素的原子结构示意图如图所示
 ,则其在元素周期表中的位置为
,则其在元素周期表中的位置为(2)Ge元素位于中金属元素和非金属元素的分界处,其最高正价为
(3)以上元素中,失电子能力最强的元素是
(4)根据元素周期律等有关知识,推断:
①阴影部分元素对应的氢化物中最稳定的是
②
 、
、 、
、 、
、 ,四种离子半径由大到小的顺序:
,四种离子半径由大到小的顺序:③
 、
、 、
、 的酸性由强到弱的顺序:
的酸性由强到弱的顺序:
您最近一年使用:0次
名校
3 . 镓是一种低熔点、高沸点的稀有金属,有“电子工业脊梁”的美誉,被广泛应用到光电子工业和微波通信工业.回答下列问题:
(1)镓 的原子结构示意图为
的原子结构示意图为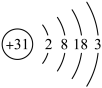 ,镓元素在元素周期表中的位置是
,镓元素在元素周期表中的位置是_________ .
(2) 的熔点为1238℃,且熔融状态不导电,据此判断,该化合物是
的熔点为1238℃,且熔融状态不导电,据此判断,该化合物是_____________ (填“共价化合物”或“离子化合物”).
(3)已知 与
与 同周期,
同周期, 与N同主族.
与N同主族.
①用原子结构理论推测, 中
中 元素的化合价为
元素的化合价为____________ ;
②下列事实不能用元素周期律解释的是___________ (填标序号);
a.原子半径: b.热稳定性:
b.热稳定性: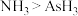
c.碱性: d.酸性:
d.酸性: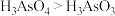
(4) 是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中.一种镍催化法生产
是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中.一种镍催化法生产 的工艺如图.
的工艺如图.
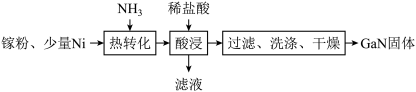
①“热转化”时 转化为
转化为 的化学方程式是
的化学方程式是______________ ;
②“酸浸”操作的目的是_______________ ;
③某学校化学兴趣小组在实验室利用如图装置模拟制备氮化镓:
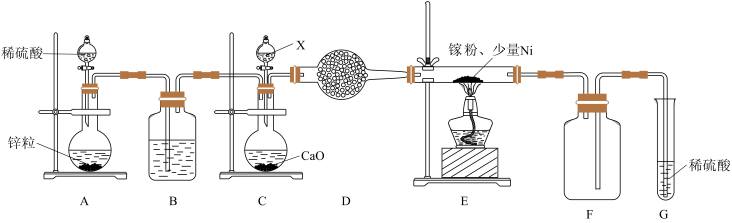
仪器X中的试剂是____________ ;加热前需先通入一段时间的 ,原因是
,原因是____________ ;装置G的作用是___________ .
(1)镓
 的原子结构示意图为
的原子结构示意图为 ,镓元素在元素周期表中的位置是
,镓元素在元素周期表中的位置是(2)
 的熔点为1238℃,且熔融状态不导电,据此判断,该化合物是
的熔点为1238℃,且熔融状态不导电,据此判断,该化合物是(3)已知
 与
与 同周期,
同周期, 与N同主族.
与N同主族.①用原子结构理论推测,
 中
中 元素的化合价为
元素的化合价为②下列事实不能用元素周期律解释的是
a.原子半径:
 b.热稳定性:
b.热稳定性: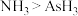
c.碱性:
 d.酸性:
d.酸性: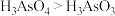
(4)
 是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中.一种镍催化法生产
是一种直接能隙(directbandgap)的半导体,自1990年起常用在发光二极管中.一种镍催化法生产 的工艺如图.
的工艺如图.
①“热转化”时
 转化为
转化为 的化学方程式是
的化学方程式是②“酸浸”操作的目的是
③某学校化学兴趣小组在实验室利用如图装置模拟制备氮化镓:

仪器X中的试剂是
 ,原因是
,原因是
您最近一年使用:0次
2021-06-11更新
|
492次组卷
|
3卷引用:福建省厦门第二中学2022-2023学年高一下学期4月月考化学试题
名校
4 . 如图是部分短周期主族元素原子半径与原子序数的关系图。

回答下列问题(对应的微粒均用相应的元素符号表示):
(1)写出A在元素周期表中的位置_______ 。比较Z、Q两种元素的简单离子半径大小_______ ;M的原子结构示意图为_______ 。
(2)图中最活泼的金属是_______ ,将其单质在氧气中加热,生成的产物为_______ 。该元素的最高价氧化物对应的水化物与L的最高价氧化物对应的水化物发生反应的离子方程式为_______ 。
(3)比较X、R两种元素的简单气态氢化物的沸点高低_______ ;B的氢化物在常温下跟R的氢化物混合发生反应的化学方程式为_______ ;现象为_______ 。
(4)最高价氧化物的水化物中酸性最强的是_______ 。
(5)设计一个实验方案,比较X、Q单质氧化性的强弱:_______ (注明操作、现象及结论)。

回答下列问题(对应的微粒均用相应的元素符号表示):
(1)写出A在元素周期表中的位置
(2)图中最活泼的金属是
(3)比较X、R两种元素的简单气态氢化物的沸点高低
(4)最高价氧化物的水化物中酸性最强的是
(5)设计一个实验方案,比较X、Q单质氧化性的强弱:
您最近一年使用:0次



