1 . (I)俄美科学家联合小组宣布合成出114号元素(Fl)的一种同位素,该原子的质量数是289,试回答下列问题:
(1)该元素在周期表中的位置为:___________ ,属于___________ 元素(填“金属”或“非金属”)。
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,回答下列问题:
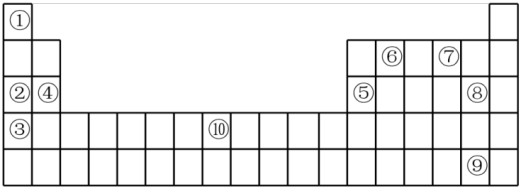
(2)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是___________ (填化学式)。
(3)元素⑦的简单氢化物与③的单质反应的离子方程式为___________ ;
(4)元素②和⑤的最高价氧化物的水化物反应的离子方程式为___________ ;
(5)元素⑩为铁,其单质与⑧的单质反应的化学方程式为___________ ;
(6)部分短周期元素的原子半径及主要化合价如下表,判断以下叙述不正确的是___________
(1)该元素在周期表中的位置为:
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,回答下列问题:

(2)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是
(3)元素⑦的简单氢化物与③的单质反应的离子方程式为
(4)元素②和⑤的最高价氧化物的水化物反应的离子方程式为
(5)元素⑩为铁,其单质与⑧的单质反应的化学方程式为
(6)部分短周期元素的原子半径及主要化合价如下表,判断以下叙述不正确的是___________
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A.L2+、R2-的核外电子数相等 |
| B.单质与稀盐酸反应的速率L<Q |
| C.M与T形成的化合物具有两性 |
| D.T与R可形成的化合物TR2、TR3 |
您最近一年使用:0次
名校
2 . 1869年俄国化学家门捷列夫制出第一张元素周期表,元素周期表体现了元素位置、结构和性质的关系。短周期元素A、B、C、D、E原子序数递增,由它们组成的新型化合物CA4B5D8·4A2D可用于电讯器材、高级玻璃的制造,其受热分解产物中有两种常见的10电子分子,二者反应生成一种弱碱,B、E同主族,E是同周期离子半径最小的。
(1)画出E的离子结构示意图______ ,在元素周期表中的位置为______ 。
(2)100—200℃时只生成一种气体,该气体电子式为______ 。
(3)试比较B、C、E元素所形成最高价氧化物对应水化物的酸性由强到弱的顺序为(写化学式)______ ,并从原子结构角度解释其原因__ 。
(4)请依据推断比较D、E两种元素离子半径的大小______ 。
(5)C的最高价氧化物对应的水化物与E的最高价氧化物对应的水化物反应的离子方程式为______ 。
(6)该化合物500℃热分解后生成的固体氧化物可与Mg单质发生置换反应,写出化学方程式______ 。
(1)画出E的离子结构示意图
(2)100—200℃时只生成一种气体,该气体电子式为
(3)试比较B、C、E元素所形成最高价氧化物对应水化物的酸性由强到弱的顺序为(写化学式)
(4)请依据推断比较D、E两种元素离子半径的大小
(5)C的最高价氧化物对应的水化物与E的最高价氧化物对应的水化物反应的离子方程式为
(6)该化合物500℃热分解后生成的固体氧化物可与Mg单质发生置换反应,写出化学方程式
您最近一年使用:0次
名校
解题方法
3 . (I)俄美科学家联合小组宣布合成出114号元素(Fl)的一种同位素,该原子的质量数是289,试回答下列问题:
(1)该元素在周期表中的位置为:_______ ,属于_______ 元素(填“金属”或“非金属”)。
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
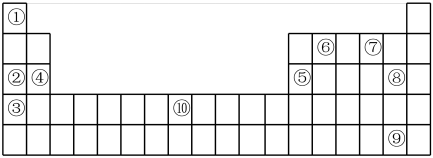
(2)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是_______ (填化学式)。
(3)元素⑦的简单氢化物与③的单质反应的离子方程式为_______ ;
(4)元素②和⑤的最高价氧化物的水化物反应的离子方程式为_______ ;
(5)元素⑩的名称为_______ ,其单质与⑧的单质反应的化学方程式为_______ ;
(6)部分短周期元素的原子半径及主要化合价如下表,判断以下叙述不正确的是_______
A.L2+、R2-的核外电子数相等
B.单质与稀盐酸反应的速率L<Q
C.M与T形成的化合物具有两性
D.简单氢化物的沸点为HnT>HnR
E.T与R可形成的化合物TR2、TR3
F.Q与M的单质均能与盐酸、NaOH溶液反应放出氢气
(1)该元素在周期表中的位置为:
(II)下表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:

(2)②③④三种元素最高价氧化物的水化物碱性由强到弱的顺序是
(3)元素⑦的简单氢化物与③的单质反应的离子方程式为
(4)元素②和⑤的最高价氧化物的水化物反应的离子方程式为
(5)元素⑩的名称为
(6)部分短周期元素的原子半径及主要化合价如下表,判断以下叙述不正确的是
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
B.单质与稀盐酸反应的速率L<Q
C.M与T形成的化合物具有两性
D.简单氢化物的沸点为HnT>HnR
E.T与R可形成的化合物TR2、TR3
F.Q与M的单质均能与盐酸、NaOH溶液反应放出氢气
您最近一年使用:0次
名校
解题方法
4 . 现有短周期主族元素X、Y、Z、R、W、T,R原子最外层电子数是电子层数的2倍,Z是金属元素,Y与Z能形成Z2Y、Z2Y2型化合物,W元素形成的氧化物具有两性,TY2是一种新型高效自来水消毒杀菌剂,五种元素的原子半径与原子序数的关系如图所示,按要求回答下列问题:
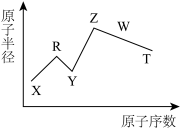
(1)X在元素周期表中的位置是_______ ;T的离子结构示意图为_______ .
(2) Z2Y2的电子式为_______ ,属于_______ 化合物(离子或共价),写出该物质与水反应的离子方程式_______ 。
(3)Y、Z、W、T简单离子半径由大到小的顺序为_______ (用离子符号表示)。
(4)Z最高价氧化物对应水化物与W元素氧化物反应的化学方程式为_______
(5)下列说法正确且能证明元素金属性Z大于W的是_______(填标号)。

(1)X在元素周期表中的位置是
(2) Z2Y2的电子式为
(3)Y、Z、W、T简单离子半径由大到小的顺序为
(4)Z最高价氧化物对应水化物与W元素氧化物反应的化学方程式为
(5)下列说法正确且能证明元素金属性Z大于W的是_______(填标号)。
| A.Z元素单质的熔点比W元素单质的熔点低 |
| B.Z元素的单质能置换出WT3溶液中W元素的单质 |
| C.Z、W最高价氧化物对应水化物的碱性:Z>W |
| D.等物质的量的Z、W元素单质分别与酸反应失去电子数目:Z<W |
您最近一年使用:0次
2023-04-27更新
|
178次组卷
|
2卷引用:山东省德州市2022-2023学年高一下学期4月期中考试化学试题
名校
解题方法
5 . 元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题。
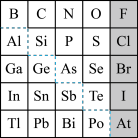
(1)元素Ga在元素周期表中的位置为:第_____ 周期第____ 族。
(2)Sn的最高正价为____ ,Cl的最高价氧化物对应水化物的化学式为___ ,Bi的最高价氧化物为_____ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是______ 元素(填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4______ H2SeO4(填“>”“<”或“=”)。
③氢化物的还原性:H2O______ H2S(填“>”“<”或“=”)。
④原子半径比较:N______ Si(填“>”“<”或“=”)。
(4)可在图中分界线(虚线部分)附近寻找______ (填序号)。
A.优良的催化剂 B.半导体材料C.合金材料 D.农药
(5)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)________ 。

(1)元素Ga在元素周期表中的位置为:第
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③氢化物的还原性:H2O
④原子半径比较:N
(4)可在图中分界线(虚线部分)附近寻找
A.优良的催化剂 B.半导体材料C.合金材料 D.农药
(5)请设计实验比较C、Si的非金属性强弱顺序(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液,化学仪器根据需要选择)
您最近一年使用:0次
2020-02-08更新
|
311次组卷
|
4卷引用:山东省淄博市淄川中学2022-2023学年高一上学期期末学情自测化学试题
名校
解题方法
6 . 回答下列问题:
(1)已知有下列物质:①HNO3;②NaOH;③液氦;④Na2O2;⑤H2O2;⑥CCl4;⑦NH4Cl;⑧KBr,分别将正确的序号填入相应的位置。以上物质中只含有离子键的是_______ ;只含有共价键的是_______ ;含有非极性共价键的离子化合物是_______ ;不含化学键的是_______ 。
(2)在完整的周期表中第三周期半径最大的主族元素,该元素单质与氧气在加热条件下反应,得到产物R,则R中阴离子与阳离子个数比为:_______ 。
(3)硒(Se)化铟(In)是一种新型半导体材料。下列说法正确的是_______(填序号)。
(4)已知短周期四种主族元素分别形成的离子X+、Y2+、Zˉ、W2ˉ均具有相同的电子层结构,则X、Y、Z、W这四种元素原子半径由大到小的顺序是_______ (用元素符号表示)。
(5)A+、Bˉ、C、D四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ C+D↑,则A+的电子式为
C+D↑,则A+的电子式为_______ ;比较C和D的稳定性的强弱:_______ (用化学式表示)。
(6)质量相同的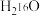 和
和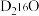 所含中子数之比为
所含中子数之比为_______ 。
(1)已知有下列物质:①HNO3;②NaOH;③液氦;④Na2O2;⑤H2O2;⑥CCl4;⑦NH4Cl;⑧KBr,分别将正确的序号填入相应的位置。以上物质中只含有离子键的是
(2)在完整的周期表中第三周期半径最大的主族元素,该元素单质与氧气在加热条件下反应,得到产物R,则R中阴离子与阳离子个数比为:
(3)硒(Se)化铟(In)是一种新型半导体材料。下列说法正确的是_______(填序号)。
| A.原子半径:In>Se | B.In比Se易失去电子 |
| C.In的金属性比Al弱 | D.硒化铟的化学式为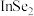 |
(5)A+、Bˉ、C、D四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ
 C+D↑,则A+的电子式为
C+D↑,则A+的电子式为(6)质量相同的
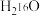 和
和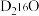 所含中子数之比为
所含中子数之比为
您最近一年使用:0次
名校
解题方法
7 . X、Y、Z、W是原子序数依次增大的前四周期元素,X、Z的周期序数=族序数,由这四种元素组成的单质或化合物存在如图所示的转化关系,其中甲、戊是两常见金属单质,丁是非金属单质,其余为氧化物且丙为具有磁性的黑色晶体。下列说法错误的是
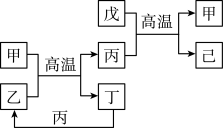

| A.W的原子序数是Z的两倍,金属性强于Z |
| B.W元素在周期表中的位置是第四周期VIII族 |
| C.己属于两性氧化物 |
| D.等物质的量的甲和戊与氯气反应,消耗的氯气的物质的量相等 |
您最近一年使用:0次
名校
解题方法
8 . 短周期元素X、Y、Z、W的原子序数递增,且Z为金属元素,X、W同主族。单质X、Z、W可分别与单质Y化合生成最高价化合物甲、乙、丙。结合如图转化关系,下列判断正确的是
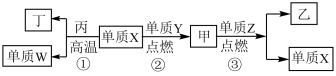

A.反应①可表示为 | B.X位于元素周期表第二周期V主族 |
| C.甲、丙、丁均为酸性氧化物 | D.乙的电子式为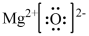 |
您最近一年使用:0次
2022-04-23更新
|
1011次组卷
|
3卷引用: 山东省青岛第五十八中学2022-2023学年高一下学期3月月考化学试题
名校
9 . 下图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
(1)在上述元素的最高价氧化物对应的水化物中,属于强酸的是_______ (用化学式表示,下同);碱性最强的是_______ 。
(2)④、⑤、⑥的简单离子半径由大到小的顺序是_______ (用离子符号表示)。
(3)有两种离子化合物,均由①、④、⑤、⑧四种元素组成。这两种物质可在水溶液中发生反应,写出该反应的离子方程式:_______ 。
(4)由表中元素形成的常见无机化合物A、B、C、X有以下转化关系:
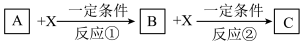
若A、B、C都含元素⑦,X为强电解质,且反应都在溶液中进行,则B的化学式为_______ ,X的化学式可能为_______ 或_______ (写不同类别物质)。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)④、⑤、⑥的简单离子半径由大到小的顺序是
(3)有两种离子化合物,均由①、④、⑤、⑧四种元素组成。这两种物质可在水溶液中发生反应,写出该反应的离子方程式:
(4)由表中元素形成的常见无机化合物A、B、C、X有以下转化关系:

若A、B、C都含元素⑦,X为强电解质,且反应都在溶液中进行,则B的化学式为
您最近一年使用:0次
名校
解题方法
10 . 现有部分短周期元素的信息如表所示:
A、B、D三种单质(分别由X、Y、Z元素组成)和甲、乙、丙、丁、戊五种化合物之间的转化关系如图所示(某些条件已略去)。其中丁是一种筒能燃料,分子中含有18个电子,其组成元素与丙相同。
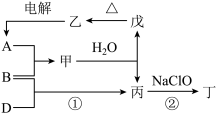
(1)元素X在周期表中的位置是______ ,其简单离子的结构示意图为______ 。
(2)单质B的电子式为______ 。
(3)丙中所含的化学键类型是______ (填序号)。
a.离子键 b.极性共价键 c.非极性共价键
(4)反应②中,0.5 mol 参加反应时转移1 mol电子,该反应的化学方程式为
参加反应时转移1 mol电子,该反应的化学方程式为______ 。
(5)一定条件下,A与 、C(石墨)反应只生成乙和碳化钛(
、C(石墨)反应只生成乙和碳化钛( ),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为
),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为______ 。
| 元素编号 | 元素性质或原子结构信息 |
| X | 第三周期元素中简单离子半径最小的元素 |
| Y | 其最简单氢化物丙的水溶液呈碱性 |
| Z | 原子核外电子数和所在周期数相等 |

(1)元素X在周期表中的位置是
(2)单质B的电子式为
(3)丙中所含的化学键类型是
a.离子键 b.极性共价键 c.非极性共价键
(4)反应②中,0.5 mol
 参加反应时转移1 mol电子,该反应的化学方程式为
参加反应时转移1 mol电子,该反应的化学方程式为(5)一定条件下,A与
 、C(石墨)反应只生成乙和碳化钛(
、C(石墨)反应只生成乙和碳化钛( ),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为
),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为
您最近一年使用:0次
2020-03-02更新
|
1104次组卷
|
7卷引用:山东省济南市2022-2023学年高一下学期期中考试化学试题



