现有部分短周期元素的信息如表所示:
A、B、D三种单质(分别由X、Y、Z元素组成)和甲、乙、丙、丁、戊五种化合物之间的转化关系如图所示(某些条件已略去)。其中丁是一种筒能燃料,分子中含有18个电子,其组成元素与丙相同。
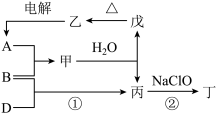
(1)元素X在周期表中的位置是______ ,其简单离子的结构示意图为______ 。
(2)单质B的电子式为______ 。
(3)丙中所含的化学键类型是______ (填序号)。
a.离子键 b.极性共价键 c.非极性共价键
(4)反应②中,0.5 mol 参加反应时转移1 mol电子,该反应的化学方程式为
参加反应时转移1 mol电子,该反应的化学方程式为______ 。
(5)一定条件下,A与 、C(石墨)反应只生成乙和碳化钛(
、C(石墨)反应只生成乙和碳化钛( ),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为
),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为______ 。
| 元素编号 | 元素性质或原子结构信息 |
| X | 第三周期元素中简单离子半径最小的元素 |
| Y | 其最简单氢化物丙的水溶液呈碱性 |
| Z | 原子核外电子数和所在周期数相等 |

(1)元素X在周期表中的位置是
(2)单质B的电子式为
(3)丙中所含的化学键类型是
a.离子键 b.极性共价键 c.非极性共价键
(4)反应②中,0.5 mol
 参加反应时转移1 mol电子,该反应的化学方程式为
参加反应时转移1 mol电子,该反应的化学方程式为(5)一定条件下,A与
 、C(石墨)反应只生成乙和碳化钛(
、C(石墨)反应只生成乙和碳化钛( ),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为
),二者均为某些高温结构陶瓷的主要成分,该反应的化学方程式为
更新时间:2020-03-02 13:54:03
|
相似题推荐
【推荐1】有A、B、C、D、E五种元素的原子序数依次增大。A、B、C位于同一周期,A原子的第一电离能大于B原子,B原子的2p能级上有两个未成对电子,D位于第四周期且原子的d能级上没有电子,C与D形成的化合物为DC2。E原子的3d能级上电子数是4s能级上电子数的三倍。
(1)写出基态E3+的电子排布式___ 。
(2)A原子第一电离能大于B的原因___ 。
(3)一个A2C2分子中含个___ σ键,___ 个π键;AB 离子的空间构型为
离子的空间构型为___ 。
(4)上述五种元素的原子中电负性由大到小顺序是___ (填元素符号)。
(1)写出基态E3+的电子排布式
(2)A原子第一电离能大于B的原因
(3)一个A2C2分子中含个
 离子的空间构型为
离子的空间构型为(4)上述五种元素的原子中电负性由大到小顺序是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】G、M、R、X、Y、W、Q、T为原子序数依次增大的前四周期元素。G的一种简单粒子是一个质子,M基态原子L层中p轨道电子数是s轨道电子数的2倍,R原子K层的电子数与M层的电子数的乘积等于其L层的电子数,X和M是同主族元素,Y与X同周期且相邻,W是第一种过渡元素,Q位于第ⅠB族,T元素最高正价和最低负价的代数和为4.请回答下列问题:
(1)W的元素符号___________ ,Q在周期表中第___________ 列,T基态原子的简化电子排布式是___________ 。
(2)X与M形成的XM3分子的VSEPR模型是_______ ,GYM的电子式为________ 。
(3)R、T均能与氢元素形成气态氢化物,则它们形成的组成最简单的氢化物中,中心原子杂化类型___________ (填“相同”或“不相同”)。
(4)已知高温下4QM→2Q2M+M2,从Q原子价层电子结构的角度分析,能生成Q2M的原因是___________ 。
(5)已知AlY3通常以二聚体(Al2Y6)形式存在,画出其二聚体的结构式___________ (标出配位键)。
(1)W的元素符号
(2)X与M形成的XM3分子的VSEPR模型是
(3)R、T均能与氢元素形成气态氢化物,则它们形成的组成最简单的氢化物中,中心原子杂化类型
(4)已知高温下4QM→2Q2M+M2,从Q原子价层电子结构的角度分析,能生成Q2M的原因是
(5)已知AlY3通常以二聚体(Al2Y6)形式存在,画出其二聚体的结构式
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】X,Y,Z三种短周期元素,它们的原子序数之和等于16,X2,Y2,Z2在常温下都是无色气体,它们均为工业合成某化工产品的重要原料,其流程如下:

已知:①一定条件下,X2与Y2能反应生成A,X2与Z2能反应生成B;
②B和C分子均为常见的10电子微粒。
请回答下列问题:
(1)X元素在周期表中的位置是___________________________________________ ;
(2)X2与Z2可制成新型化学电源(KOH溶液作电解质溶液),两个电极均由多孔石墨制成,通入的气体在电极表面放电,负极电极反应式为________________________ ;
(3)化合物B吸收C后形成的溶液pH______ 7(填“大于”、“小于”或“等于”),其原因是(用离子方程式表示)___________________________________________________________________ ;
(4)写出由C生成A和B的化学方程式______________________________ 。

已知:①一定条件下,X2与Y2能反应生成A,X2与Z2能反应生成B;
②B和C分子均为常见的10电子微粒。
请回答下列问题:
(1)X元素在周期表中的位置是
(2)X2与Z2可制成新型化学电源(KOH溶液作电解质溶液),两个电极均由多孔石墨制成,通入的气体在电极表面放电,负极电极反应式为
(3)化合物B吸收C后形成的溶液pH
(4)写出由C生成A和B的化学方程式
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】X、Y、Z、W为原子序数依次增大的四种短周期元素,其中X元素原子的核外电子总数等于其电子层数,Z元素的气态氢化物和它的氧化物在常温下反应生成Z单质和水,X与Y、W可分别形成YX3和XW型共价化合物,YX3极易溶于水.
(1) 化合物YX3的空间构型为____________ ; Y原子的杂化轨道类型为_______ .
(2)XW的电子式是_____________ .
(3)XW与YX3反应生成一种盐,该盐水溶液的pH________ 7(填“大于”“小于”或“等于”),其原因是(用离子方程式表示)______________________________ .
(4)Z元素氢化物的沸点比H2O________ (填“低”或“高”).Z元素的氢化物有毒,写出用CuSO4溶液吸收Z元素氢化物的离子方程式________________________________ .
(5)已知X单质和Y单质反应生成YX3的反应是可逆反应,ΔH<0.将X、Y的两种单质以等物质的量充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应.下列说法正确的是________ .
a.达到化学平衡时,任何一种物质的正反应速率与逆反应速率相等
b.反应过程中,Y单质的体积分数始终为50%
c.达到化学平衡时,X、Y两种单质在混合气体中的物质的量之比为1∶1
d.达到化学平衡的过程中气体平均相对分子质量减小
e.到达化学平衡后,升高温度,YX3的体积分数增大
(1) 化合物YX3的空间构型为
(2)XW的电子式是
(3)XW与YX3反应生成一种盐,该盐水溶液的pH
(4)Z元素氢化物的沸点比H2O
(5)已知X单质和Y单质反应生成YX3的反应是可逆反应,ΔH<0.将X、Y的两种单质以等物质的量充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应.下列说法正确的是
a.达到化学平衡时,任何一种物质的正反应速率与逆反应速率相等
b.反应过程中,Y单质的体积分数始终为50%
c.达到化学平衡时,X、Y两种单质在混合气体中的物质的量之比为1∶1
d.达到化学平衡的过程中气体平均相对分子质量减小
e.到达化学平衡后,升高温度,YX3的体积分数增大
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D、E是原子序数依次增大的短周期元素,A是短周期中金属性最强的元素,B是地壳中含量最高的金属元素,C单质的晶体是良好的半导体材料,D的最外层电子数与内层电子数之比为3:5。
(1)C的原子结构示意图为_________ ,D在元素周期表中的位置____________ 。
(2)A单质在氧气中燃烧生成化合物甲,甲中所含化学键为__________ ;A单质在E单质中燃烧生成化合物乙,用电子式表示乙的形成过程___________________ 。
(3)F是中学化学常见元素,它的一种氧化物为红棕色粉末,B单质与其在高温条件下反应是冶炼F单质的方法之一,该反应的化学方程式为__________________________ 。
(4)含B元素的化合物常用作净水剂,用文字和化学用语解释净水原因:__________ 。
(5)E元素的非金属性强于D元素,用原子结构解释原因:______________________ ,同周期元素随着原子序数的递增非金属性增强。
(6)工业上将干燥的E单质通入D熔融的单质中可制得化合物D2E2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为___________________ 。
(1)C的原子结构示意图为
(2)A单质在氧气中燃烧生成化合物甲,甲中所含化学键为
(3)F是中学化学常见元素,它的一种氧化物为红棕色粉末,B单质与其在高温条件下反应是冶炼F单质的方法之一,该反应的化学方程式为
(4)含B元素的化合物常用作净水剂,用文字和化学用语解释净水原因:
(5)E元素的非金属性强于D元素,用原子结构解释原因:
(6)工业上将干燥的E单质通入D熔融的单质中可制得化合物D2E2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,该反应的化学方程式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、D、E四种元絭的核电荷数依次增大,且均小于20,A元素的一种核素原子核内没有中子,A、E的原子最外层上都只有一个电子,其中只有E是金属,B元素L层电子数是K层的3倍,D元素原子得一个电子后,形成电子总数与氩原子的电子总数相同的离子。回答下列问题:
(1)A的元素符号_______ ;
(2)写出D离子的电子式:_______ ;
(3)画出B元素原子的结构示意图:_______ ;画出E离子的结构示意图_______ 。
(1)A的元素符号
(2)写出D离子的电子式:
(3)画出B元素原子的结构示意图:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】随原子序数的递增,七种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
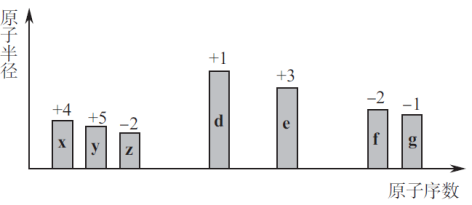
根据判断出的元素回答:
(1)x在元素周期表的位置是________________________ 。
(2)y的最高价氧化物对应的水化物与其氢化物反应,产物中含有化学键的类型为________________ 。
(3)d的单质在空气中充分燃烧,所得产物的电子式为________ ;7.8 g该产物与足量的水完全反应,转移电子的数目为____________________ 。
(4)z、e、f的简单离子半径由大到小的顺序为_______________ (用离子符号表示)。
(5)能说明g的非金属性比f强的实验事实是________________ (列举一条)。

根据判断出的元素回答:
(1)x在元素周期表的位置是
(2)y的最高价氧化物对应的水化物与其氢化物反应,产物中含有化学键的类型为
(3)d的单质在空气中充分燃烧,所得产物的电子式为
(4)z、e、f的简单离子半径由大到小的顺序为
(5)能说明g的非金属性比f强的实验事实是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的前三周期主族和0族元素区,表中虚线处为ⅡA、ⅢA族的连接处,请用相应的化学用语回答下列问题:

(1)写出仅由e形成的两种带有相同电荷数的阴离子的符号________ 、________ 。
(2)d的元素名称为________ ,其双原子分子的电子式为________ 。
(3)图I是表示第三周期8种元素单质的熔点(℃)条形图,已知条形“1”代表Ar,则其中条形“8”代表的是________ (填化学式)晶体,1 mol该晶体中含有________ mol化学键。
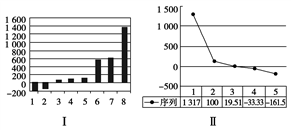
(4)b、c、d、e、f的氢化物的沸点(℃)直角坐标图(图Ⅱ)中序列“5”对应的氢化物的名称是__________ ,空间构型为__________ ;序列“2”对应的氢化物的结构式是__________ ,属于________ (填“极性”或“非极性”)分子。

(1)写出仅由e形成的两种带有相同电荷数的阴离子的符号
(2)d的元素名称为
(3)图I是表示第三周期8种元素单质的熔点(℃)条形图,已知条形“1”代表Ar,则其中条形“8”代表的是

(4)b、c、d、e、f的氢化物的沸点(℃)直角坐标图(图Ⅱ)中序列“5”对应的氢化物的名称是
您最近半年使用:0次



