名校
1 . 从1869年俄国化学家门捷列夫编制出第一张元素周期表到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素“位-构-性”的关系,揭示了元素间的内在联系。下表列出①~⑧八种元素在周期表中的位置,回答下列问题:
(1)②③④的原子半径由大到小的顺序是_______ (填元素符号)。
(2)⑧的元素符号是_______ ,它的最高价含氧酸的分子式是_______ 。
(3)④能形成多种同素异形体,如_______ 、_______ 等,它们之间的转化是_______ 变化(填“物理”或“化学”)。
(4)①与⑤形成的化合物可做野外生氢剂,写出该物质与水反应的化学方程式_______ ,其中氧化剂是_______ 。
(5)⑥与⑦的简单氢化物更稳定的是_______ (填化学式)。
(6)门捷列夫编制元素周期表时预言了几种当时还没有发现的元素,并在表中留了空位,其中铝元素正下方的“类铝”后来被发现并命名为“镓”,元素符号为 ,镓的金属性比铝
,镓的金属性比铝_______ (填“强”或“弱”),其氢氧化物与盐酸反应的化学方程式为_______ 。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)⑧的元素符号是
(3)④能形成多种同素异形体,如
(4)①与⑤形成的化合物可做野外生氢剂,写出该物质与水反应的化学方程式
(5)⑥与⑦的简单氢化物更稳定的是
(6)门捷列夫编制元素周期表时预言了几种当时还没有发现的元素,并在表中留了空位,其中铝元素正下方的“类铝”后来被发现并命名为“镓”,元素符号为
 ,镓的金属性比铝
,镓的金属性比铝
您最近一年使用:0次
2023-01-01更新
|
239次组卷
|
2卷引用:四川省内江市第六中学2022-2023学年高一下学期入学考试化学试题
名校
2 . Ⅰ.短周期元素X、Y、Z、W、Q的原子序数依次增大,Z的原子半径是短周期主族元素中最大的,X、Y、W、Q在元素周期表中的位置如表所示,Y、Q的原子序数之和是X的4倍。回答下列问题:
(1)写出P元素简单氢化物和其最高价氧化物的水化物反应的化学方程式___________ 。
(2)葡萄酒中添加适量的某种Q的氧化物,可以起到杀菌的作用,同时利用其的___________ 性防止葡萄酒被氧化。
(3)X与Y按原子数之比为1:2形成化合物的电子式为___________ ,Y与Z形成的一种化合物是淡黄色固体,该化合物中所含化学键的类型是___________ 。
Ⅱ.汽车尾气(含碳氢化合物、CO、SO2与NO等物质)是城市空气的污染源之一、治理的方法之一是在汽车的排气管上装一个催化转化器(用Pt、Pd合金作催化剂),它的特点是使CO与NO反应,生成可参与大气循环的无毒气体,并促使汽油充分燃烧及SO2的转化。
(4)写出在催化剂的作用下CO与NO反应的化学方程式:___________ 。
(5)使用“催化转化器”的缺点是在一定程度上提高了排放废气的酸度,有可能促进了酸雨的形成,其原因是___________ 。
(6)控制城市空气污染源的方法有___________(填字母)。
| X | P | Y |
| W | Q |
(2)葡萄酒中添加适量的某种Q的氧化物,可以起到杀菌的作用,同时利用其的
(3)X与Y按原子数之比为1:2形成化合物的电子式为
Ⅱ.汽车尾气(含碳氢化合物、CO、SO2与NO等物质)是城市空气的污染源之一、治理的方法之一是在汽车的排气管上装一个催化转化器(用Pt、Pd合金作催化剂),它的特点是使CO与NO反应,生成可参与大气循环的无毒气体,并促使汽油充分燃烧及SO2的转化。
(4)写出在催化剂的作用下CO与NO反应的化学方程式:
(5)使用“催化转化器”的缺点是在一定程度上提高了排放废气的酸度,有可能促进了酸雨的形成,其原因是
(6)控制城市空气污染源的方法有___________(填字母)。
| A.植树造林 | B.开发氢能源 | C.使用电动车 | D.使用无铅汽油 |
您最近一年使用:0次
名校
3 . 部分短周期主族元素原子半径与原子序数的关系如图,根据所学知识回答下列问题。

(1)c、d、e、i四种元素的最简单氢化物中,最稳定的是___________ (填化学式)。
(2)d与f能形成一种淡黄色的物质,其电子式为___________ 。
(3)g的最高价氧化物对应的水化物与f的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(4)由a的单质制成的电池需要注意防水,其原因为___________ (用化学方程式表示)。
(5)门捷列夫在研究元素周期表时,科学地预言了11种当时尚未发现的元素,他认为g的下一周期存在一种“类g”元素,该元素多年后被法国化学家发现,命名为镓(Ga),镓在元素周期表中的位置为___________ 。预测g与Ga的最高价氧化物对应水化物的碱性较强的是___________ (填最高价氧化物对应水化物的化学式)。
(6)使用下列装置再添加合适的药品,可以证明b和h两种元素的非金属性强弱顺序,可供选择的药品为:①浓硫酸②稀硫酸③盐酸④ 固体⑤
固体⑤ ⑥澄清石灰水⑦NaOH溶液
⑥澄清石灰水⑦NaOH溶液

请选择装置丙、丁两处应该加入的药品代号:丙___________ 、丁___________ 。
(7)某实验小组向100mL 溶液中通入气体单质
溶液中通入气体单质 ,溶液中
,溶液中 、
、 的物质的量随通入的
的物质的量随通入的 的物质的量变化如图所示(不考虑与水的反应)。
的物质的量变化如图所示(不考虑与水的反应)。

从开始通入 到
到 时,溶液中
时,溶液中
___________ 。

(1)c、d、e、i四种元素的最简单氢化物中,最稳定的是
(2)d与f能形成一种淡黄色的物质,其电子式为
(3)g的最高价氧化物对应的水化物与f的最高价氧化物对应的水化物反应的离子方程式为
(4)由a的单质制成的电池需要注意防水,其原因为
(5)门捷列夫在研究元素周期表时,科学地预言了11种当时尚未发现的元素,他认为g的下一周期存在一种“类g”元素,该元素多年后被法国化学家发现,命名为镓(Ga),镓在元素周期表中的位置为
(6)使用下列装置再添加合适的药品,可以证明b和h两种元素的非金属性强弱顺序,可供选择的药品为:①浓硫酸②稀硫酸③盐酸④
 固体⑤
固体⑤ ⑥澄清石灰水⑦NaOH溶液
⑥澄清石灰水⑦NaOH溶液
请选择装置丙、丁两处应该加入的药品代号:丙
(7)某实验小组向100mL
 溶液中通入气体单质
溶液中通入气体单质 ,溶液中
,溶液中 、
、 的物质的量随通入的
的物质的量随通入的 的物质的量变化如图所示(不考虑与水的反应)。
的物质的量变化如图所示(不考虑与水的反应)。
从开始通入
 到
到 时,溶液中
时,溶液中
您最近一年使用:0次
2024-01-15更新
|
137次组卷
|
2卷引用:四川省成都市第七中学2023-2024学年高一上学期12月月考化学试题
4 . 下表是元素周期表中前四周期的部分元素,表中所列字母分别代表一种元素。
回答下列问题:
(1)i在元素周期表中的位置是__________ 。
(2)a、e、g、l形成的简单离子其半径由大到小的顺序为__________ (填写离子符号)。
(3)n与o形成的化合物为__________ (填写化学式),将该化合物进行焰色试验,火焰呈__________ 色。
(4)用电子式表示g和m形成化合物的过程__________ 。
(5)将足量d的氢化物溶于水,再取少量 的水溶液滴入其中,反应的离子方程式为
的水溶液滴入其中,反应的离子方程式为__________ 。
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
实验操作:取已除去氧化膜且表面积相等的镁条和铝条,分别投入 盐酸中。
盐酸中。
实验现象:镁与盐酸反应比铝更剧烈。
①比较金属性:
______  (选填“>”或“<”);
(选填“>”或“<”);
②利用元素周期律对上述实验结论进行解释__________ 。
(7)向 的碱性溶液中通入m单质,可得到
的碱性溶液中通入m单质,可得到 ,反应的离子方程式为:
,反应的离子方程式为:__________ 。
a | b | |||||||
c | d | e | f | |||||
g | h | i | j | k | l | m | ||
o | n | |||||||
(1)i在元素周期表中的位置是
(2)a、e、g、l形成的简单离子其半径由大到小的顺序为
(3)n与o形成的化合物为
(4)用电子式表示g和m形成化合物的过程
(5)将足量d的氢化物溶于水,再取少量
 的水溶液滴入其中,反应的离子方程式为
的水溶液滴入其中,反应的离子方程式为(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
实验操作:取已除去氧化膜且表面积相等的镁条和铝条,分别投入
 盐酸中。
盐酸中。实验现象:镁与盐酸反应比铝更剧烈。
①比较金属性:

 (选填“>”或“<”);
(选填“>”或“<”);②利用元素周期律对上述实验结论进行解释
(7)向
 的碱性溶液中通入m单质,可得到
的碱性溶液中通入m单质,可得到 ,反应的离子方程式为:
,反应的离子方程式为:
您最近一年使用:0次
2023-02-17更新
|
196次组卷
|
3卷引用:四川省眉山市2022-2023学年高一上学期期末考试化学试题
名校
解题方法
5 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
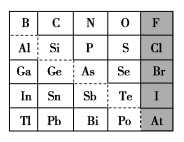
(1)元素 在元素周期表中的位置为第
在元素周期表中的位置为第______ 周期第______ 族。
(2) 的最高化合价为
的最高化合价为______ , 的最高价氧化物对应的水化物的化学式为
的最高价氧化物对应的水化物的化学式为______ , 的最高价氧化物为
的最高价氧化物为______ 。
(3)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是______ 元素(填元素符号)。
②酸性:
______ (填“>”“<”或“=”,下同) 。
。
③氢化物的还原性:
______  。
。
④原子半径:
______  。
。
(4)可在图中分界线(虚线)附近寻找______ (填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料
(5)从下列试剂中选择最佳试剂组合,比较 、
、 的非金属性强弱:
的非金属性强弱:______ 。(可供选择的药品有 固体、稀硫酸、盐酸、饱和
固体、稀硫酸、盐酸、饱和 溶液、饱和
溶液、饱和 溶液、硅酸钠溶液)
溶液、硅酸钠溶液)

(1)元素
 在元素周期表中的位置为第
在元素周期表中的位置为第(2)
 的最高化合价为
的最高化合价为 的最高价氧化物对应的水化物的化学式为
的最高价氧化物对应的水化物的化学式为 的最高价氧化物为
的最高价氧化物为(3)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是
②酸性:

 。
。③氢化物的还原性:

 。
。④原子半径:

 。
。(4)可在图中分界线(虚线)附近寻找
A.优良的催化剂 B.半导体材料 C.合金材料
(5)从下列试剂中选择最佳试剂组合,比较
 、
、 的非金属性强弱:
的非金属性强弱: 固体、稀硫酸、盐酸、饱和
固体、稀硫酸、盐酸、饱和 溶液、饱和
溶液、饱和 溶液、硅酸钠溶液)
溶液、硅酸钠溶液)
您最近一年使用:0次
2020-09-08更新
|
1569次组卷
|
6卷引用:四川省绵阳市东辰学校2023-2024学年高一上学期化学期末复习综合模拟试题



