1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
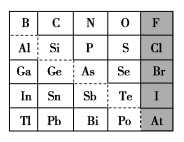
(1)元素 在元素周期表中的位置为第
在元素周期表中的位置为第______ 周期第______ 族。
(2) 的最高化合价为
的最高化合价为______ , 的最高价氧化物对应的水化物的化学式为
的最高价氧化物对应的水化物的化学式为______ , 的最高价氧化物为
的最高价氧化物为______ 。
(3)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是______ 元素(填元素符号)。
②酸性:
______ (填“>”“<”或“=”,下同) 。
。
③氢化物的还原性:
______  。
。
④原子半径:
______  。
。
(4)可在图中分界线(虚线)附近寻找______ (填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料
(5)从下列试剂中选择最佳试剂组合,比较 、
、 的非金属性强弱:
的非金属性强弱:______ 。(可供选择的药品有 固体、稀硫酸、盐酸、饱和
固体、稀硫酸、盐酸、饱和 溶液、饱和
溶液、饱和 溶液、硅酸钠溶液)
溶液、硅酸钠溶液)

(1)元素
 在元素周期表中的位置为第
在元素周期表中的位置为第(2)
 的最高化合价为
的最高化合价为 的最高价氧化物对应的水化物的化学式为
的最高价氧化物对应的水化物的化学式为 的最高价氧化物为
的最高价氧化物为(3)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是
②酸性:

 。
。③氢化物的还原性:

 。
。④原子半径:

 。
。(4)可在图中分界线(虚线)附近寻找
A.优良的催化剂 B.半导体材料 C.合金材料
(5)从下列试剂中选择最佳试剂组合,比较
 、
、 的非金属性强弱:
的非金属性强弱: 固体、稀硫酸、盐酸、饱和
固体、稀硫酸、盐酸、饱和 溶液、饱和
溶液、饱和 溶液、硅酸钠溶液)
溶液、硅酸钠溶液)
更新时间:2020-09-08 21:22:57
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)锂和镁在元素周期表中有特殊“对角线”关系,它们的性质相似。下列有关锂及其化合物的叙述不正确的是___ 。
A.Li2SO4难溶于水
B.Li与N2反应产物是Li3N
C.LiOH难溶于水
D.LiOH与Li2CO3受热都易分解
(2)与铝位于对角线位置的第二周期元素是Be,能区别Be(OH)2和Mg(OH)2的一种试剂是___ ,反应的离子方程式为___ 。
(3)门捷列夫在研究元素周期表时,科学地预言了11种尚未发现的元素,为它们在周期表中留下空位。例如,他预测在铝的下方有一个与铝类似的元素“类铝”,后来被法国化学家于1875年发现,命名为镓。它在周期表中的位置是___ 。
(4)关于与镓同主族的第六周期元素性质的推测中不正确的是___ 。
A.单质是银白色较软的金属
B.其氢氧化物是两性氢氧化物
C.在化合物中显+3价
D.单质与盐酸的反应比铝剧烈
(5)写出短周期主族元素中原子半径最大的原子的单质在空气中加热条件下反应产物的电子式___ 。
(1)锂和镁在元素周期表中有特殊“对角线”关系,它们的性质相似。下列有关锂及其化合物的叙述不正确的是
A.Li2SO4难溶于水
B.Li与N2反应产物是Li3N
C.LiOH难溶于水
D.LiOH与Li2CO3受热都易分解
(2)与铝位于对角线位置的第二周期元素是Be,能区别Be(OH)2和Mg(OH)2的一种试剂是
(3)门捷列夫在研究元素周期表时,科学地预言了11种尚未发现的元素,为它们在周期表中留下空位。例如,他预测在铝的下方有一个与铝类似的元素“类铝”,后来被法国化学家于1875年发现,命名为镓。它在周期表中的位置是
(4)关于与镓同主族的第六周期元素性质的推测中不正确的是
A.单质是银白色较软的金属
B.其氢氧化物是两性氢氧化物
C.在化合物中显+3价
D.单质与盐酸的反应比铝剧烈
(5)写出短周期主族元素中原子半径最大的原子的单质在空气中加热条件下反应产物的电子式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】设X、Y、Z代表3种元素。已知:
①X+和Y-两种离子具有相同的电子层结构;
②Z元素原子核内质子数比Y原子核内质子数少9个;
③Y和Z两种元素可以形成4核42个电子的负一阶阴离子。
因此,请填空:
(1)写出X、Y、Z三种元素的名称:X________ ,Y________ ,Z________ 。
(2)写出X、Y两种元素最高价氧化物对应水化物相互反应的离子方程式:___________________ 。
①X+和Y-两种离子具有相同的电子层结构;
②Z元素原子核内质子数比Y原子核内质子数少9个;
③Y和Z两种元素可以形成4核42个电子的负一阶阴离子。
因此,请填空:
(1)写出X、Y、Z三种元素的名称:X
(2)写出X、Y两种元素最高价氧化物对应水化物相互反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】六种短周期元素在周期表中的相对位置如下所示,其中E元素原子核外电子总数是其最外层电子数的3倍。关于元素周期表及这六种元素性质,请回答:

(1)这六种元素的氢化物中,最稳定的是___________ .(写化学式);
(2)AF2的结构式为_____________ .
(3)在一定条件下,由B单质与H2反应生成1 molG气体时,放出的热量为46.2 kJ,写出该反应的热化学方程式:_____________________ .
(4)工业上用G检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质B生成,写出化学方程式__________________________ .该反应中被氧化的G与参与反应的G的质量之比__________ .
(5)F的单质可由其氧化物与氢化物反应生成,写出该反应的化学方程式:__________ .

(1)这六种元素的氢化物中,最稳定的是
(2)AF2的结构式为
(3)在一定条件下,由B单质与H2反应生成1 molG气体时,放出的热量为46.2 kJ,写出该反应的热化学方程式:
(4)工业上用G检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质B生成,写出化学方程式
(5)F的单质可由其氧化物与氢化物反应生成,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】19世纪中叶,门捷列夫总结了如表所示的元素化学性质的变化情况。请回答:
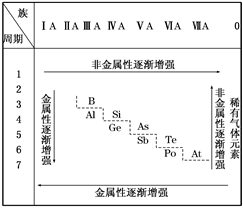
(1)门捷列夫的突出贡献是________ 。
A.提出了原子学说
B.提出了分子学说
C.发现了元素周期律
D.发现能量守恒定律
(2)该表变化表明________ 。
A.事物的性质总是在不断地发生变化
B.元素周期表中最右上角的氦元素是非金属性最强的元素
C.第ⅠA族元素的金属性肯定比同周期的第ⅡA族元素的金属性强
D.物质发生量变到一定程度必然引起质变
(3)按照表中元素的位置,认真观察从第ⅢA族的硼到第ⅦA族的砹连接的一条折线,我们能从分界线附近找到________ 。
A.耐高温材料 B.新型农药材料
C.半导体材料 D.新型催化剂材料
(4)据报道,美国科学家制得一种新原子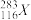 ,它属于一种新元素116号元素(元素符号暂用X代替),关于它的推测正确的是
,它属于一种新元素116号元素(元素符号暂用X代替),关于它的推测正确的是________ 。
A.这种原子的中子数为167
B.它位于元素周期表中第6周期
C.这种元素一定是金属元素
D.这种元素的原子易与氢化合

(1)门捷列夫的突出贡献是
A.提出了原子学说
B.提出了分子学说
C.发现了元素周期律
D.发现能量守恒定律
(2)该表变化表明
A.事物的性质总是在不断地发生变化
B.元素周期表中最右上角的氦元素是非金属性最强的元素
C.第ⅠA族元素的金属性肯定比同周期的第ⅡA族元素的金属性强
D.物质发生量变到一定程度必然引起质变
(3)按照表中元素的位置,认真观察从第ⅢA族的硼到第ⅦA族的砹连接的一条折线,我们能从分界线附近找到
A.耐高温材料 B.新型农药材料
C.半导体材料 D.新型催化剂材料
(4)据报道,美国科学家制得一种新原子
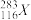 ,它属于一种新元素116号元素(元素符号暂用X代替),关于它的推测正确的是
,它属于一种新元素116号元素(元素符号暂用X代替),关于它的推测正确的是A.这种原子的中子数为167
B.它位于元素周期表中第6周期
C.这种元素一定是金属元素
D.这种元素的原子易与氢化合
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)N在元素周期表中的位置是_______ 。
(2)自然的水银内含7种核素: 、
、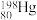 、
、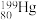 、
、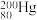 、
、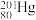 、
、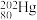 和
和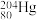 ,它们互称为
,它们互称为_______ 。其中,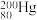 和
和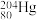 中子数之比为
中子数之比为_______ 。
(3)用电子式表示 的形成过程为
的形成过程为_______ 。
(4)下列有关性质的比较,能用元素周期律解释的是_______(填标号).
(5)已知碲( )与S同主族,则碲及其化合物可能具有的性质正确的是_______(填标号)。
)与S同主族,则碲及其化合物可能具有的性质正确的是_______(填标号)。
(6)硫磺可用于制作黑火药,是炸时的反应为: 。反应中每消耗3.2gS,释放的气体体积为
。反应中每消耗3.2gS,释放的气体体积为_______ L(换算成标准状况)。烟花爆竹的成分中除了加火药,常加入一些金属元素,燃烧时会产生五彩缤纷的火焰。若燃放烟花的火焰呈现紫色,则烟花中可能含有_______ 元素(填名称),该元素的离子结构示意图为_______ 。
(1)N在元素周期表中的位置是
(2)自然的水银内含7种核素:
 、
、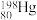 、
、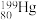 、
、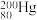 、
、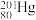 、
、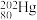 和
和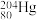 ,它们互称为
,它们互称为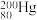 和
和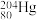 中子数之比为
中子数之比为(3)用电子式表示
 的形成过程为
的形成过程为(4)下列有关性质的比较,能用元素周期律解释的是_______(填标号).
A.酸性; | B.非金属性:O>S |
C.碱性: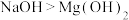 | D.热稳定性: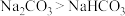 |
 )与S同主族,则碲及其化合物可能具有的性质正确的是_______(填标号)。
)与S同主族,则碲及其化合物可能具有的性质正确的是_______(填标号)。| A.单质碲在常温下是固体 | B.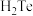 比 比 稳定 稳定 |
C.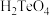 的酸性比 的酸性比 弱 弱 | D. 通入 通入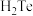 溶液中不发生反应 溶液中不发生反应 |
 。反应中每消耗3.2gS,释放的气体体积为
。反应中每消耗3.2gS,释放的气体体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】下表是元素周期表的一部分。
(1)表中元素⑩的氢化物的化学式为__________ ,此氢化物的还原性比元素⑨的氢化物的还原性_____________ (填强或弱)
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是_____ ,其固态单质属于__________ 晶体
(3)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式
__________________________
(4)表中⑥对应的一种单质呈V形,该单质属于_______ 分子(填“极性”或“非极性”)
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ⑤ | ⑥ | ||
| 三 | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中元素⑩的氢化物的化学式为
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是
(3)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式
(4)表中⑥对应的一种单质呈V形,该单质属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】结合下图所示元素周期表,回答下列问题:___________ (填字母,下同);属于主族元素的有___________ 。
(2)f元素位于第___________ 周期第___________ 族。g元素位于第___________ 周期第___________ 族,i元素位于第___________ 周期第___________ 族。
(3)以下验证c、d、e、j四种元素金属性强弱的方法和结论均正确的是___________(填字母序号)。
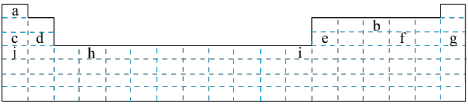
(2)f元素位于第
(3)以下验证c、d、e、j四种元素金属性强弱的方法和结论均正确的是___________(填字母序号)。
| A.比较四种元素形成的最高价氧化物对应的水化物碱性强弱:j>c>d>e |
| B.比较四种元素形成氢化物的难易程度以及氢化物的热稳定性:j<c<d<e |
| C.比较四种元素形成的单质分别与非氧化性酸反应置换氢气的剧烈程度:c>j>d>e |
| D.将空气中久置的四种元素的块状单质分别放入水中,比较与水反应的剧烈程度:j>c>d>e |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下图是元素周期表的一部分,A—I九种元素在元素周期表中的位置如图:

请回答下列问题:
(1)B在周期表中的位置_______ ;E的离子结构示意图______ 。
(2)C的最高价氧化物对应的水化物与C的气态氢化物发生反应,生成物中含有的化学键类型是_____ 。
(3)G、I的最高价氧化物对应的水化物的化学式是_________ 、_____ 。
(4)A、D形成的化合物中只含极性键的物质的电子式为______ 。
(5)F、H的简单离子半径较大的是______ (用离子符号表示),H、I的气态氢化物稳定性较强的是____ (填化学式)。

请回答下列问题:
(1)B在周期表中的位置
(2)C的最高价氧化物对应的水化物与C的气态氢化物发生反应,生成物中含有的化学键类型是
(3)G、I的最高价氧化物对应的水化物的化学式是
(4)A、D形成的化合物中只含极性键的物质的电子式为
(5)F、H的简单离子半径较大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,表中所列的字母分别代表某一化学元素。回答下列问题:

(1)元素B在元素周期表中的位置是第____ 周期第_____ 族,A、B、C三种元素原子半径从大到小的顺序是_________________ ;(填元素符号)
(2)D简单离子的结构示意图为_____________ ,用电子式表示D2C的形成过程_______ 。
(3)下列说法正确的是( ) (填序号)
①B的简单气态氢化物比C的稳定
②D元素的最高价氧化物对应的水化物的碱性比E的强
③D元素的单质与水反应比E元素的单质与水反应更剧烈
④B的简单阴离子比C的简单阴离子还原性强
(4)D单质在空气中燃烧可生成淡黄色粉末X(D2O2),X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和下图所示实验装置证明X有提供氧气的作用。
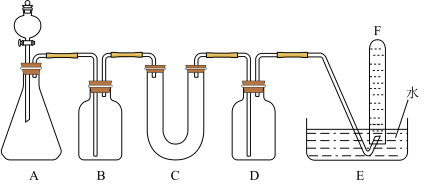
①装置A使用石灰石与浓盐酸反应制取CO2,装置B中饱和NaHCO3溶液的作用是除去_____________ ;(填化学式)
②装置C中X与CO2反应的化学方程式是_____________________ ,装置D盛放NaOH溶液的作用是除去____________ 。(填化学式)

(1)元素B在元素周期表中的位置是第
(2)D简单离子的结构示意图为
(3)下列说法正确的是
①B的简单气态氢化物比C的稳定
②D元素的最高价氧化物对应的水化物的碱性比E的强
③D元素的单质与水反应比E元素的单质与水反应更剧烈
④B的简单阴离子比C的简单阴离子还原性强
(4)D单质在空气中燃烧可生成淡黄色粉末X(D2O2),X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和下图所示实验装置证明X有提供氧气的作用。

①装置A使用石灰石与浓盐酸反应制取CO2,装置B中饱和NaHCO3溶液的作用是除去
②装置C中X与CO2反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】“三酸两碱”是最重要的无机化工产品,广泛用于国防、石油、纺织、冶金、食品等工业。“三酸”是指硝酸、硫酸和盐酸,“两碱”是指烧碱和纯碱。回答下列问题:
(1)请写出硝酸中的氮元素在元素周期表中的位置___________ 。
(2)请将“三酸两碱”中所含位于第三周期的元素,按原子半径由大到小的顺序排列___________ 。
(3)氯的非金属性比硫_______ (填“强”或“弱”),请用一个事实说明你的结论________ 。
(4)某烧碱溶液中含0.1molNaOH,向该溶液通入一定量CO2,充分反应后,将所得溶液低温蒸干,得到固体的组成可能有四种情况,分别是:①________ ;②Na2CO3;③_________ ;④NaHCO3。若该固体溶于水,滴加过量盐酸,再将溶液蒸干,得到固体的质量是_________ g。
(1)请写出硝酸中的氮元素在元素周期表中的位置
(2)请将“三酸两碱”中所含位于第三周期的元素,按原子半径由大到小的顺序排列
(3)氯的非金属性比硫
(4)某烧碱溶液中含0.1molNaOH,向该溶液通入一定量CO2,充分反应后,将所得溶液低温蒸干,得到固体的组成可能有四种情况,分别是:①
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请回答下列问题。
(1)第三周期元素中,化学性质最不活泼的是______ ,可用于制半导体材料的元素是______ ,最高价氧化物的水化物碱性最强的是______ ,酸性最强的是______ ,两性的是______ (用元素符号填空)。
(2)在C、N、O、F中,原子半径最大的是______ 。
(3)第32号元素在元素周期表中的位置为______ 。
(4)利用如图装置可验证同主族元素非金属性的变化规律。
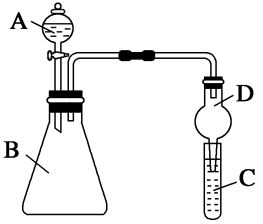
①仪器A的名称为______ ,干燥管D的作用为______ 。
②若要证明非金属性: C1>I,则A中加浓盐酸,B中加KMnO4, KMnO4与浓盐酸常温下反应生成氯气,C中加淀粉-碘化钾混合溶液,观察到C中溶液______ (填现象),即可证明,氯气在C中反应的离子方程式为______ 。从环境保护的观点考虑,此装置缺少尾气处理装置,可用______ 溶液吸收尾气,反应的化学方程式为______ 。
(1)第三周期元素中,化学性质最不活泼的是
(2)在C、N、O、F中,原子半径最大的是
(3)第32号元素在元素周期表中的位置为
(4)利用如图装置可验证同主族元素非金属性的变化规律。

①仪器A的名称为
②若要证明非金属性: C1>I,则A中加浓盐酸,B中加KMnO4, KMnO4与浓盐酸常温下反应生成氯气,C中加淀粉-碘化钾混合溶液,观察到C中溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】比较下列元素的性质(用“>”、“<”表示)
(1)金属性:Li_______ Na;
(2)非金属性:F_______ Cl;
(3)根据元素在周期表中的位置,判断下列各组化合物的酸、碱性强弱:Al(OH)3_______ Mg(OH)2;
(4)原子半径:N_______ O。
(1)金属性:Li
(2)非金属性:F
(3)根据元素在周期表中的位置,判断下列各组化合物的酸、碱性强弱:Al(OH)3
(4)原子半径:N
您最近一年使用:0次



