1 . 某化学研究性学习小组欲配制含有 、Cl-、K+、
、Cl-、K+、 的植物培养液480mL,且要求该培养液中c(Cl-)=c(K+)=c(
的植物培养液480mL,且要求该培养液中c(Cl-)=c(K+)=c( )=0.4mol/L。
)=0.4mol/L。
实验室提供的药品有:NH4Cl、KCl、(NH4)2SO4、K2SO4和蒸馏水。
提供的实验仪器有:药匙、烧杯、玻璃棒、胶头滴管、量筒、称量纸,托盘天平。
请回答下列问题:
(1)该植物培养液中, 的物质的量浓度为
的物质的量浓度为___________ 。
(2)该研究小组配制该植物培养液时,还须用到的实验仪器有___________ 。
(3)甲同学用KCl和(NH4)2SO4,两种物质进行配制,则需称取m(KCl)=___________ g;m[(NH4)2SO4]=___________ g。
(4)请将下列实验步骤按照先后顺序排列:___________ 。
 、Cl-、K+、
、Cl-、K+、 的植物培养液480mL,且要求该培养液中c(Cl-)=c(K+)=c(
的植物培养液480mL,且要求该培养液中c(Cl-)=c(K+)=c( )=0.4mol/L。
)=0.4mol/L。实验室提供的药品有:NH4Cl、KCl、(NH4)2SO4、K2SO4和蒸馏水。
提供的实验仪器有:药匙、烧杯、玻璃棒、胶头滴管、量筒、称量纸,托盘天平。
请回答下列问题:
(1)该植物培养液中,
 的物质的量浓度为
的物质的量浓度为(2)该研究小组配制该植物培养液时,还须用到的实验仪器有
(3)甲同学用KCl和(NH4)2SO4,两种物质进行配制,则需称取m(KCl)=
(4)请将下列实验步骤按照先后顺序排列:
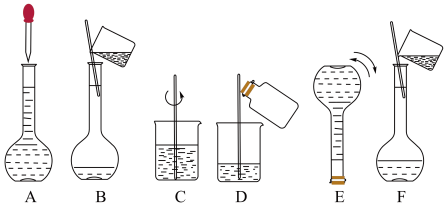
| A.将溶液转移至容量瓶后,未洗涤烧杯和玻璃棒 |
| B.将烧杯内的溶液向容量瓶中转移时,因操作不当使部分溶液溅出容量瓶 |
| C.用胶头滴管向容量瓶中加水时,溶液的凹液面低于容量瓶刻度线 |
| D.用胶头滴管向容量瓶中加水时,俯视容量瓶刻度线 |
您最近半年使用:0次
名校
2 . 人胃酸(主要成分是盐酸)过多,会引起很多胃病,需服用抗酸药治疗。抗酸药胃舒平的主要成分是氢氧化铝,某同学为测定该药中氢氧化铝的质量分数进行如下几步操作(设该药片中的其他成分不与盐酸或氢氧化钠反应):
步聚1:取1粒药片(每片药片的质量为0.50g)研碎
步聚2:将上研碎的药片粉末加入到40.00mL0.40mol/L稀盐酸中溶解
步聚3:用0.40mol/LNaOH溶液中和过量稀盐酸,记录消耗NaOH溶液的体积;
请回答下列问题。
(1)实验室用密度为 质量分数为36.5%的浓盐酸配制该0.40mol/L盐酸溶液240mL,应用量筒量取
质量分数为36.5%的浓盐酸配制该0.40mol/L盐酸溶液240mL,应用量筒量取___________ mL浓盐酸。
(2)实验用到的玻璃仪器有烧杯、玻璃棒、量筒和___________ 。
(3)下列操作会使配制的溶液浓度偏低的有___________ 。
A.转移溶液时,未洗涤玻璃棒和烧杯内壁
B.配制溶液前容量瓶底部有少量蒸馏水残留
C.摇匀后发现液面下降,再加水至刻度线
D.定容时俯视刻度线
E.溶液未冷却即转移到容量瓶中
(4)某同学4次测定所消耗的NaOH溶液的体积如下:
根据这个同学的实验数据,计算这种药片中氢氧化铝的质量分数为___________ %(结果保留小数点后两位)。
步聚1:取1粒药片(每片药片的质量为0.50g)研碎
步聚2:将上研碎的药片粉末加入到40.00mL0.40mol/L稀盐酸中溶解
步聚3:用0.40mol/LNaOH溶液中和过量稀盐酸,记录消耗NaOH溶液的体积;
请回答下列问题。
(1)实验室用密度为
 质量分数为36.5%的浓盐酸配制该0.40mol/L盐酸溶液240mL,应用量筒量取
质量分数为36.5%的浓盐酸配制该0.40mol/L盐酸溶液240mL,应用量筒量取(2)实验用到的玻璃仪器有烧杯、玻璃棒、量筒和
(3)下列操作会使配制的溶液浓度偏低的有
A.转移溶液时,未洗涤玻璃棒和烧杯内壁
B.配制溶液前容量瓶底部有少量蒸馏水残留
C.摇匀后发现液面下降,再加水至刻度线
D.定容时俯视刻度线
E.溶液未冷却即转移到容量瓶中
(4)某同学4次测定所消耗的NaOH溶液的体积如下:
| 测定次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| V[NaOH(aq)]/mL | 16.04 | 15.96 | 16.20 | 16.00 |
您最近半年使用:0次
2024-03-08更新
|
75次组卷
|
2卷引用:浙江省杭州市长河高级中学2023-2024学年高一上学期期末考试化学试题
名校
解题方法
3 . 将30mL 0.5mol•L的稀硫酸加水稀释到500mL,稀释后稀硫酸的溶质的物质的量浓度为
| A.0.03mol/L | B.0.3mol/L | C.0.05mol/L | D.0.15mol/L |
您最近半年使用:0次
名校
解题方法
4 . 用溶质质量分数为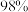 的浓硫酸
的浓硫酸 配制
配制 稀硫酸,下列操作正确的是
稀硫酸,下列操作正确的是
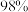 的浓硫酸
的浓硫酸 配制
配制 稀硫酸,下列操作正确的是
稀硫酸,下列操作正确的是| A.将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却 |
| B.必须用到的定量仪器有200mL容量瓶和托盘天平 |
| C.量取浓硫酸的体积为20.0mL |
| D.量取浓硫酸时仰视,定容时俯视,都会使所配硫酸溶液浓度偏大 |
您最近半年使用:0次
5 . 某化学研究性学习小组需配制含有 、Cl-、K+、
、Cl-、K+、 的植物培养液450mL,且要求该培养液中c(Cl-)=c(K+)=c(
的植物培养液450mL,且要求该培养液中c(Cl-)=c(K+)=c( )=0.4mol/L。
)=0.4mol/L。
实验室提供的药品有:NH4Cl、KCl、(NH4)2SO4、K2SO4和蒸馏水;
提供的实验仪器有:①药匙②托盘天平③烧杯④玻璃棒⑤胶头滴管⑥量筒。请回答下列问题:
(1)该植物培养液中, 的物质的量浓度为
的物质的量浓度为___________ 。
(2)该研究小组配制该植物培养液时,还须用到的实验仪器是___________ (填字母)。
A.450mL容量瓶 B.500mL容量瓶 C.两个250mL容量
(3)甲同学用KCl和(NH4)2SO4两种物质进行配制,则需称取m(KCl)=___________ g。
(4)若配制该培养液的其他操作均正确,则下列操作将使所配制溶液的浓度偏低的是___________ (填字母)。
A.将溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
B.将烧杯内的溶液向容量瓶中转移时,因操作不当使部分溶液溅出容量瓶
C.用胶头滴管向容量瓶中加水时,溶液的凹液面高于容量瓶刻度线
D.用胶头滴管向容量瓶中加水时,俯视容量瓶刻度线
E.用己生锈的砝码称量所需物质的质量
 、Cl-、K+、
、Cl-、K+、 的植物培养液450mL,且要求该培养液中c(Cl-)=c(K+)=c(
的植物培养液450mL,且要求该培养液中c(Cl-)=c(K+)=c( )=0.4mol/L。
)=0.4mol/L。实验室提供的药品有:NH4Cl、KCl、(NH4)2SO4、K2SO4和蒸馏水;
提供的实验仪器有:①药匙②托盘天平③烧杯④玻璃棒⑤胶头滴管⑥量筒。请回答下列问题:
(1)该植物培养液中,
 的物质的量浓度为
的物质的量浓度为(2)该研究小组配制该植物培养液时,还须用到的实验仪器是
A.450mL容量瓶 B.500mL容量瓶 C.两个250mL容量
(3)甲同学用KCl和(NH4)2SO4两种物质进行配制,则需称取m(KCl)=
(4)若配制该培养液的其他操作均正确,则下列操作将使所配制溶液的浓度偏低的是
A.将溶液转移至容量瓶后,未洗涤烧杯和玻璃棒
B.将烧杯内的溶液向容量瓶中转移时,因操作不当使部分溶液溅出容量瓶
C.用胶头滴管向容量瓶中加水时,溶液的凹液面高于容量瓶刻度线
D.用胶头滴管向容量瓶中加水时,俯视容量瓶刻度线
E.用己生锈的砝码称量所需物质的质量
您最近半年使用:0次
解题方法
6 . 实验室中需要配制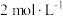 的
的 溶液
溶液 ,配制时应选用的容量瓶的规格和称取的
,配制时应选用的容量瓶的规格和称取的 质量分别是
质量分别是
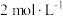 的
的 溶液
溶液 ,配制时应选用的容量瓶的规格和称取的
,配制时应选用的容量瓶的规格和称取的 质量分别是
质量分别是A.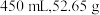 | B.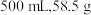 |
C. | D.任意规格,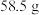 |
您最近半年使用:0次
名校
7 . 下列实验过程可以达到实验目的的是
| 编号 | 实验目的 | 实验过程 |
| A | 配制0.4mol/L的NaOH溶液 | 称取4.0g固体NaOH于烧杯中,加入少量蒸馏水溶解,转移至500mL容量瓶中定容 |
| B | 探究H2O2的还原性 | 向盛有2 mL酸性高锰酸钾溶液的试管中滴加H2O2溶液,观察颜色变化 |
| C | 制取干燥纯净的氢气 | 向稀盐酸中加入锌粒,将生成的气体依次通过浓硫酸、NaOH溶液,然后收集 |
| D | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到饱和氯化铁溶液中 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
8 . 下列说法正确的是
| A.1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol·L-1 |
| B.从1 L 2 mol·L-1的H2SO4溶液中取出0.5 L,该溶液的浓度为1 mol·L-1 |
| C.500 mL 0.5 mol·L-1的CuSO4溶液中含有40 g CuSO4 |
| D.中和100 mL 1 mol·L-1的H2SO4溶液,需NaOH固体4 g |
您最近半年使用:0次
名校
解题方法
9 . I.氯气和漂白粉是现代工业和生活中常用的杀菌消毒剂;某兴趣小组利用所给仪器在实验室制备纯净干燥的氯气;并模拟工业制漂白粉。请回答下列问题:
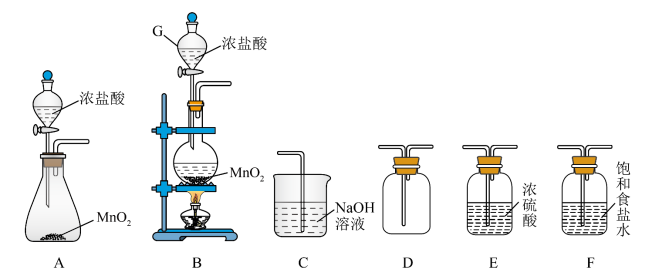
(1)装置G的名称为___________ 。
(2)图中制氯气的化学方程式___________ 。
(3)从图中选择合适装置制备并收集纯净干燥的氯气(仪器不重复使用);仪器连接顺序为(用仪器下方字母表示:如A→B→…)___________ 。
II.漂白粉的制备
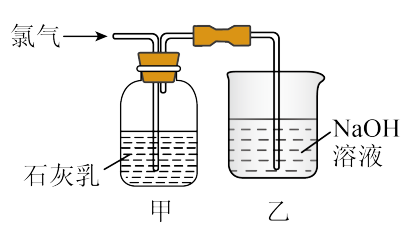
已知:①氯气和石灰乳在反应的过程中会放出热量
②加热条件下氯气与碱会发生歧化反应生成氯酸盐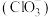
(4)写出制取漂白粉的化学方程式___________ 。
(5)兴趣小组制得的漂白粉中 的含量远超过预期;而
的含量远超过预期;而 含量明显偏低。主要原因可能是(请用化学方程式结合文字表述)
含量明显偏低。主要原因可能是(请用化学方程式结合文字表述)___________ 。
(6)为提高产品中有效成分 的含量;在不改变石灰乳浓度和体积的条件下可采取的操作措施是(任写一种即可)
的含量;在不改变石灰乳浓度和体积的条件下可采取的操作措施是(任写一种即可)___________ 。
(7)本实验使用的浓盐酸试剂瓶标签上的有关数据如下图。
①该浓盐酸中HCl的物质的量浓度为___________ 。
②若用该浓盐酸和蒸馏水配制500mL0.400mol/L的稀盐酸,需要量取_______ mL上述浓盐酸进行配制。

(1)装置G的名称为
(2)图中制氯气的化学方程式
(3)从图中选择合适装置制备并收集纯净干燥的氯气(仪器不重复使用);仪器连接顺序为(用仪器下方字母表示:如A→B→…)
II.漂白粉的制备

已知:①氯气和石灰乳在反应的过程中会放出热量
②加热条件下氯气与碱会发生歧化反应生成氯酸盐
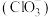
(4)写出制取漂白粉的化学方程式
(5)兴趣小组制得的漂白粉中
 的含量远超过预期;而
的含量远超过预期;而 含量明显偏低。主要原因可能是(请用化学方程式结合文字表述)
含量明显偏低。主要原因可能是(请用化学方程式结合文字表述)(6)为提高产品中有效成分
 的含量;在不改变石灰乳浓度和体积的条件下可采取的操作措施是(任写一种即可)
的含量;在不改变石灰乳浓度和体积的条件下可采取的操作措施是(任写一种即可)(7)本实验使用的浓盐酸试剂瓶标签上的有关数据如下图。
| 盐酸 分子式:HCl 相对分子质量:36.5 密度: 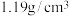 HCl的质量分数:36.5% 体积:500nL |
②若用该浓盐酸和蒸馏水配制500mL0.400mol/L的稀盐酸,需要量取
您最近半年使用:0次
名校
10 . 下列说法正确的是
A.同浓度的 、 、 、 、 溶液体积之比为 溶液体积之比为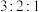 ,则 ,则 浓度之比为 浓度之比为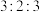 |
B.将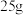 胆矾( 胆矾( )溶于水配成 )溶于水配成 溶液,该溶液的物质的量浓度为 溶液,该溶液的物质的量浓度为 |
C.欲将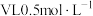 的盐酸浓度增大1倍,可将溶液加热浓缩到原体积的一半 的盐酸浓度增大1倍,可将溶液加热浓缩到原体积的一半 |
D.将 的 的 溶液和 溶液和 的 的 溶液等体积混合后,若忽略溶液体积变化, 溶液等体积混合后,若忽略溶液体积变化,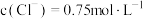 |
您最近半年使用:0次
2023-12-19更新
|
158次组卷
|
3卷引用:山东省实验中学2023-2024学年高一上学期11月期中考试化学试题



