名校
1 . 下列实验方案能达到相应实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 制备 | 向饱和食盐水中通入 后,再通 后,再通 |
| B | 配制1 L 1.0 mol/L NaCl溶液 | 将58.5 g NaCl固体直接溶于1 L水中 |
| C | 鉴别 和 和 | 取样,加入澄清石灰水,若有白色沉淀生成,则为 |
| D | 检验NaOH中的阳离子 | 用洁净的铂丝蘸取待测液,在酒精灯火焰上灼烧 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023高三·全国·专题练习
2 . 现有VL0.5mol·L-1的盐酸,欲将其浓度扩大一倍,以下方法中最宜采用的是
| A.加热浓缩到原来体积的一半 |
| B.加入5mol·L-1的盐酸0.125VL |
| C.加入10mol·L-1的盐酸0.1VL,再稀释至1.5VL |
| D.标准状况下通入11.2VL氯化氢气体 |
您最近一年使用:0次
3 . 氟化钾是一种重要的无机化合物,应用广泛。其一种制备工艺流程如下:

回答下列问题:
(1)“滤渣”中的主要成分是_______ (填化学式),写出该成分的一种用途:_______ 。
(2)写出制备 的反应的化学方程式:
的反应的化学方程式:_______ ;配制 的浓硫酸,需要用量筒量取密度为
的浓硫酸,需要用量筒量取密度为 的98%的浓硫酸
的98%的浓硫酸_______  。
。
(3)制备 的反应其基本反应类型为
的反应其基本反应类型为_______ 。
(4)写出“转化”时发生反应的化学方程式:_______ 。
(5)“系列操作”包括_______ 、过滤分离和干燥。

回答下列问题:
(1)“滤渣”中的主要成分是
(2)写出制备
 的反应的化学方程式:
的反应的化学方程式: 的浓硫酸,需要用量筒量取密度为
的浓硫酸,需要用量筒量取密度为 的98%的浓硫酸
的98%的浓硫酸 。
。(3)制备
 的反应其基本反应类型为
的反应其基本反应类型为(4)写出“转化”时发生反应的化学方程式:
(5)“系列操作”包括
您最近一年使用:0次
4 . 某锥形瓶盛有盐酸和氯化铜的混合溶液100g,向其中逐渐加入溶质质量分数为10%的氢氧化钠溶液,锥形瓶内溶液质量与滴入的氢氧化钠溶液的质量的变化关系如图所示。请计算:

(1)配制质量分数为10%的氢氧化钠溶液200g,需要氢氧化钠的质量_______ g。
(2)反应至A点时,溶液中钠元素的质量是_______ g。

(1)配制质量分数为10%的氢氧化钠溶液200g,需要氢氧化钠的质量
(2)反应至A点时,溶液中钠元素的质量是
您最近一年使用:0次
名校
解题方法
5 . 实验中需用 的
的 溶液950mL,配制时应选用的容量瓶的规格和称取
溶液950mL,配制时应选用的容量瓶的规格和称取 的质量分别为
的质量分别为
 的
的 溶液950mL,配制时应选用的容量瓶的规格和称取
溶液950mL,配制时应选用的容量瓶的规格和称取 的质量分别为
的质量分别为| A.1000mL,212g | B.950mL,201.4g | C.1000mL,201.4g | D.500mL,100.7g |
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
6 . 含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol·L-1。( )
您最近一年使用:0次
2022-07-08更新
|
178次组卷
|
5卷引用:考点03 物质的量的浓度及溶液配制-备战2022年高考化学一轮复习考点帮(全国通用)
(已下线)考点03 物质的量的浓度及溶液配制-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点03 物质的量的浓度及溶液配制-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点03 物质的量的浓度及溶液配制-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点03 物质的量浓度及溶液配制(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第9讲 物质的量浓度
2021高三·全国·专题练习
7 . VL浓度为0.5mol·L-1的盐酸,欲使其浓度增大1倍,可将溶液加热浓缩到0.5VL。( )
您最近一年使用:0次
名校
8 . 实验室需用 的
的 溶液,现选用
溶液,现选用 的容量瓶配制该溶液,下列方法可行的是
的容量瓶配制该溶液,下列方法可行的是
 的
的 溶液,现选用
溶液,现选用 的容量瓶配制该溶液,下列方法可行的是
的容量瓶配制该溶液,下列方法可行的是A.称取 ,加入 ,加入 水 水 |
B.称取 ,加入 ,加入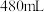 水 水 |
C.称取 ,加水配成 ,加水配成 溶液 溶液 |
D.称取 ,加水配成 ,加水配成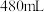 溶液 溶液 |
您最近一年使用:0次
2022-05-26更新
|
542次组卷
|
3卷引用:天津市河东区普通高中2020届高三学业水平合格性模拟考试化学试题
天津市河东区普通高中2020届高三学业水平合格性模拟考试化学试题(已下线)第13讲 物质的量浓度-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )黑龙江省绥化市第九中学2021-2022学年高二下学期期末考试化学试题
名校
9 . 回答下列问题:
(1)标准状况下,1.7gNH3与___ LH2S气体含有的氢原子数相同。
(2)标准状况,NH3与CH4组成的混合气体的平均密度为0.75g·L-1,该混合气体的平均摩尔质量为___ ,NH3的体积分数为___ 。
(3)常温下,在27.9g水中溶解12.1gCu(NO3)2·3H2O,恰好达到饱和。设该溶液密度为1.20g·cm-3。
求:①溶质的质量分数为___ 。
②该溶液中NO 的物质的量浓度为
的物质的量浓度为___ 。
③取出20.0mL该溶液,配成浓度为1.00mol·L-1的稀溶液,则稀释后溶液的体积是___ mL。
④将一根质量为100g的铁棒插入到该溶液中,一段时间后取出,洗净、干燥后称量,铁棒的质量变为100.2g,此时溶液中Fe(NO3)2的物质的量浓度是___ (忽略溶液体积的变化)。
(1)标准状况下,1.7gNH3与
(2)标准状况,NH3与CH4组成的混合气体的平均密度为0.75g·L-1,该混合气体的平均摩尔质量为
(3)常温下,在27.9g水中溶解12.1gCu(NO3)2·3H2O,恰好达到饱和。设该溶液密度为1.20g·cm-3。
求:①溶质的质量分数为
②该溶液中NO
 的物质的量浓度为
的物质的量浓度为③取出20.0mL该溶液,配成浓度为1.00mol·L-1的稀溶液,则稀释后溶液的体积是
④将一根质量为100g的铁棒插入到该溶液中,一段时间后取出,洗净、干燥后称量,铁棒的质量变为100.2g,此时溶液中Fe(NO3)2的物质的量浓度是
您最近一年使用:0次
解题方法
10 . 下列判断中,正确的是
A.1L  溶液中含有98g 溶液中含有98g  ,则该溶液的物质的量浓度为98 ,则该溶液的物质的量浓度为98  |
B.1 L水溶解了0.5mol NaCl,则该溶液的物质的量浓度为0.5  |
C.1000mL  (蔗糖)溶液里含有1mol (蔗糖)溶液里含有1mol  ,则该溶液的物质的量浓度为0.001 ,则该溶液的物质的量浓度为0.001  |
D.10mL  的 的 溶液与100mL 溶液与100mL  的 的 溶液的浓度相同 溶液的浓度相同 |
您最近一年使用:0次



