1 . 制备FeOOH的工艺流程包含如下环节

(1)若在实验室完成上述制备,一定不需要的仪器是______。
(2)模拟氧化时,相关pH变化记录如图。

0~t1时段,pH逐渐减小的原因是反应生成了H2SO4,配平下列化学方程式:______ 。
______FeSO4+______O2+______=______FeOOH↓+______H2SO4
t1~t2时段,经历的反应为:12Fe2++3O2+2H2O=4FeOOH↓+8Fe3+,该过程pH继续平缓下降的原因可能是:______ 。(任写一条)
(3)判断流程中产品是否洗涤干净的方法是:______ 。

(1)若在实验室完成上述制备,一定不需要的仪器是______。
| A.烧杯 | B.漏斗 | C.玻璃棒 | D.蒸发皿 |

0~t1时段,pH逐渐减小的原因是反应生成了H2SO4,配平下列化学方程式:
______FeSO4+______O2+______=______FeOOH↓+______H2SO4
t1~t2时段,经历的反应为:12Fe2++3O2+2H2O=4FeOOH↓+8Fe3+,该过程pH继续平缓下降的原因可能是:
(3)判断流程中产品是否洗涤干净的方法是:
您最近一年使用:0次
2 . 碳酸亚铁晶体[ ]为白色固体,不溶于水,干燥品在空气中稳定,湿品在空气中缓慢氧化为
]为白色固体,不溶于水,干燥品在空气中稳定,湿品在空气中缓慢氧化为 呈茶色,可用作阻燃剂、动物饲料铁添加剂、补血剂等。回答下列问题:
呈茶色,可用作阻燃剂、动物饲料铁添加剂、补血剂等。回答下列问题:
(1)实验室利用 溶液和
溶液和 溶液制备
溶液制备 ,实验装置(夹持仪器已省略)如图所示:
,实验装置(夹持仪器已省略)如图所示:

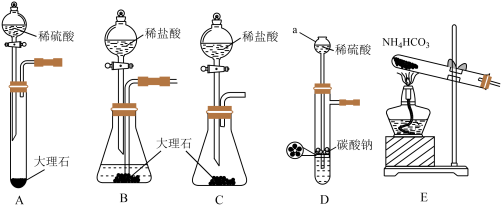
①方框内为制取 的装置,下列装置和药品较为适宜的是
的装置,下列装置和药品较为适宜的是_________ (填字母)。
②装置D中仪器a的名称是___________ 。
③根据①的选择,装置甲中试剂a的名称是_____________ 。
(2) 的制备,步骤如下:
的制备,步骤如下:
通入一段时间 后,向
后,向 溶液中加入过量
溶液中加入过量 溶液,搅拌,反应后过滤,将沉淀洗涤、干燥,得到
溶液,搅拌,反应后过滤,将沉淀洗涤、干燥,得到 。
。
①生成 的离子方程式为
的离子方程式为_________________ 。
②装置丙的作用是_________________ 。
(3)将 溶液换成
溶液换成 溶液能提高产品纯度,原因是
溶液能提高产品纯度,原因是________________ 。
(4)某同学查阅资料得知,煅烧 的产物中含有+2价铁元素,于是他设计了由
的产物中含有+2价铁元素,于是他设计了由 制备
制备 的方案。先向
的方案。先向 中依次加入试剂:稀硫酸、①
中依次加入试剂:稀硫酸、①___________ 和②____________ ;然后再③__________ (填操作)灼烧,即可得到 。
。
 ]为白色固体,不溶于水,干燥品在空气中稳定,湿品在空气中缓慢氧化为
]为白色固体,不溶于水,干燥品在空气中稳定,湿品在空气中缓慢氧化为 呈茶色,可用作阻燃剂、动物饲料铁添加剂、补血剂等。回答下列问题:
呈茶色,可用作阻燃剂、动物饲料铁添加剂、补血剂等。回答下列问题:(1)实验室利用
 溶液和
溶液和 溶液制备
溶液制备 ,实验装置(夹持仪器已省略)如图所示:
,实验装置(夹持仪器已省略)如图所示:

①方框内为制取
 的装置,下列装置和药品较为适宜的是
的装置,下列装置和药品较为适宜的是②装置D中仪器a的名称是
③根据①的选择,装置甲中试剂a的名称是
(2)
 的制备,步骤如下:
的制备,步骤如下:通入一段时间
 后,向
后,向 溶液中加入过量
溶液中加入过量 溶液,搅拌,反应后过滤,将沉淀洗涤、干燥,得到
溶液,搅拌,反应后过滤,将沉淀洗涤、干燥,得到 。
。①生成
 的离子方程式为
的离子方程式为②装置丙的作用是
(3)将
 溶液换成
溶液换成 溶液能提高产品纯度,原因是
溶液能提高产品纯度,原因是(4)某同学查阅资料得知,煅烧
 的产物中含有+2价铁元素,于是他设计了由
的产物中含有+2价铁元素,于是他设计了由 制备
制备 的方案。先向
的方案。先向 中依次加入试剂:稀硫酸、①
中依次加入试剂:稀硫酸、① 。
。
您最近一年使用:0次
3 . 能正确表示下列反应的离子方程式为
A.向 溶液中通入过量 溶液中通入过量 : : |
B.食醋去除水垢中的 : :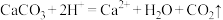 |
C.向碳酸钠溶液中通入少量 : : |
D.次磷酸(一元弱酸)与足量NaOH溶液反应: |
您最近一年使用:0次
2024-04-03更新
|
62次组卷
|
2卷引用:海南省华东师范大学第二附属中学乐东黄流中学2023-2024学年高一上学期11月期中化学试题
名校
4 . 在下列溶液中,各组离子一定能够大量共存的是
A.使酚酞溶液变红的溶液: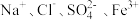 |
B.在pH=1的溶液中: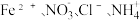 |
C.常温下: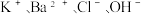 |
D.在pH=1的溶液中: |
您最近一年使用:0次
名校
解题方法
5 . 长期放置的FeSO4溶液易被氧化而变质,某兴趣小组进行了如下实验:
(1)设计实验检验FeSO4溶液的变质程度
①将方案补充完整
②若要使部分变质的FeSO4复原,方法是___________ 。(用离子反应方程式表示)
(2)利用部分变质 的FeSO4溶液制备Fe2O3。
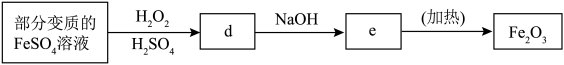
①填写下列各空:
d.___________ ;e.___________ 。
②若100mL该变质溶液制得1.6gFe2O3,则变质前FeSO4溶液的浓度为___________ 。
(3)FeSO4可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将Fe3+转化为Fe2+,以利于人体吸收。为了验证这一猜想,设计了如下实验:
由上述实验能否得出“维生素C可将Fe3+转化为Fe2+”的结论?请说明理由___________ 。
(1)设计实验检验FeSO4溶液的变质程度
①将方案补充完整
| 实验方案 | 实验现象 | 实验结论 | |
| 步骤1 | 取待检测液于试管中,向其中滴加KSCN溶液 | ii | FeSO4溶液部分变质 |
| 步骤2 | i | iii | |
(2)利用

①填写下列各空:
d.
②若100mL该变质溶液制得1.6gFe2O3,则变质前FeSO4溶液的浓度为
(3)FeSO4可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将Fe3+转化为Fe2+,以利于人体吸收。为了验证这一猜想,设计了如下实验:
| 实验方案 | 实验现象 |
| 取适量 Fe2(SO4)3溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液。 | 紫色褪去 |
您最近一年使用:0次
名校
6 . 下列离子方程式书写正确的是
A.向溴化亚铁溶液中通入少量Cl2: |
B.向氯化钡溶液中通SO2: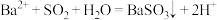 |
C.硫酸铝溶液与过量氨水反应: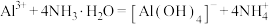 |
D.稀硝酸与过量铁粉反应: |
您最近一年使用:0次
名校
解题方法
7 . 在含有大量Fe2+、 、
、 的强酸性溶液中加入下列试剂后,溶液中主要存在的一组离子正确的是
的强酸性溶液中加入下列试剂后,溶液中主要存在的一组离子正确的是
 、
、 的强酸性溶液中加入下列试剂后,溶液中主要存在的一组离子正确的是
的强酸性溶液中加入下列试剂后,溶液中主要存在的一组离子正确的是A.通入过量Cl2: 、 、 、 、 、 、 、 、 |
B.加入少量NaClO溶液: 、 、 、 、 、 、 、 、 |
C.加入过量NaClO和NaOH的混合溶液: 、 、 、 、 、 、 、 、 |
D.加入过量NaOH溶液: 、 、 、 、 、 、 、 、 |
您最近一年使用:0次
2024-04-01更新
|
194次组卷
|
2卷引用:湖北省云学名校联盟2023-2024学年高一下学期3月联考化学试卷
名校
解题方法
8 . 实验室以锈蚀程度很大的废铁屑为原料制备无水 的流程可简要表示如图:
的流程可简要表示如图: ;
;
② ;
;
③在水溶液中 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀 。
。
试回答下列问题:
(1)“酸溶”过程中发生主要反应有:① ;②
;② ;③
;③___________ (用离子方程式表示)
(2)“酸溶”需控制温度在40℃左右,最佳的加热方式是___________ 。
(3)“过滤”需要的玻璃仪器除烧杯外还有___________ 。
(4) 和
和 反应生成
反应生成 的化学方程式为
的化学方程式为___________ 。
(5)“氧化”过程可在如图所示装置中进行。 与浓盐酸反应生成
与浓盐酸反应生成 和
和 ,其离子方程式为
,其离子方程式为___________
②装置C的作用是___________ 。
③证明装置B溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是___________ 。
 的流程可简要表示如图:
的流程可简要表示如图:
 ;
;②
 ;
;③在水溶液中
 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀 。
。试回答下列问题:
(1)“酸溶”过程中发生主要反应有:①
 ;②
;② ;③
;③(2)“酸溶”需控制温度在40℃左右,最佳的加热方式是
(3)“过滤”需要的玻璃仪器除烧杯外还有
(4)
 和
和 反应生成
反应生成 的化学方程式为
的化学方程式为(5)“氧化”过程可在如图所示装置中进行。

 与浓盐酸反应生成
与浓盐酸反应生成 和
和 ,其离子方程式为
,其离子方程式为②装置C的作用是
③证明装置B溶液中
 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是
您最近一年使用:0次
解题方法
9 . 某实验小组以含铁污泥(主要成分为Fe2O3、FeO、Fe及杂质;杂质与酸不反应,且难溶于水)为原料,设计了如图两种不同的合成路线(部分步骤已略去),用于生产绿矾(FeSO4•7H2O)和柠檬酸铁铵。
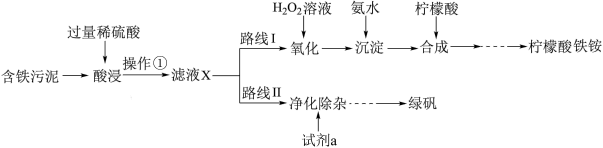
根据所学知识,回答下列问题:
(1)操作①的名称是_______ ,路线I中,加入H2O2溶液的目的是_______ 。
(2)写出“酸浸”时,Fe2O3与硫酸反应的化学方程式:_______ ;检验含有Fe3+的试剂是_______ 。
(3)实验室中配制FeSO4溶液时通常需加入少量的试剂a,目的是_______ 。
(4)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:_______ 。
(5)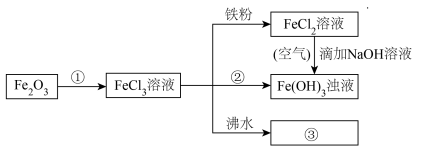
FeCl2溶液→Fe(OH)3浊液的过程中,观察到的实验现象是_______ 。

根据所学知识,回答下列问题:
(1)操作①的名称是
(2)写出“酸浸”时,Fe2O3与硫酸反应的化学方程式:
(3)实验室中配制FeSO4溶液时通常需加入少量的试剂a,目的是
(4)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
(5)

FeCl2溶液→Fe(OH)3浊液的过程中,观察到的实验现象是
您最近一年使用:0次
名校
10 . 下列说法或有关反应的离子方程式正确的是
A.与 反应能放出 反应能放出 的溶液中: 的溶液中: 、 、 、 、 、 、 一定不能大量共存 一定不能大量共存 |
B.稀硝酸与少量的铁屑反应: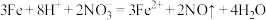 |
C. 溶液中通入少量 溶液中通入少量 : : |
D. 溶液中通入少量 溶液中通入少量 : :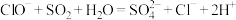 |
您最近一年使用:0次



