解题方法
1 . 化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可以减少该有害物质向环境排放。例如:
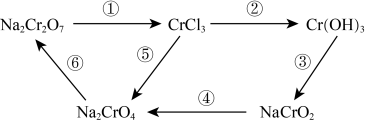
(1)Na2Cr2O7属于___________ (填序号)。
①酸 ②碱 ③盐 ④氧化物
(2)上述转化中,Cr元素化合价不变的步骤是___________ (填序号)。
(3)反应①为:Na2Cr2O7+HCl—NaCl+CrCl3+Cl2↑+H2O (未配平)。其中还原产物为___________ ,Na2Cr2O7与Cl2的计量系数比为___________ 。

(1)Na2Cr2O7属于
①酸 ②碱 ③盐 ④氧化物
(2)上述转化中,Cr元素化合价不变的步骤是
(3)反应①为:Na2Cr2O7+HCl—NaCl+CrCl3+Cl2↑+H2O (未配平)。其中还原产物为
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题。
(1)依据物质的性质分析:CaO、Na2O、Fe2O3、CuO均属于______ (填“酸性氧化物”、“碱性氧化物”或“两性氧化物”),下列物质均能与它们发生反应的是______ (填字母)。
a.水 b.盐酸 c.氢氧化钠溶液
(2)木炭与浓硫酸发生反应: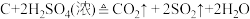 。作还原剂的物质是
。作还原剂的物质是______ ,硫元素的化合价______ (填“升高”或“降低”)。
(3)某反应中反应物与生成物的Fe3+、Mn2+、H+、 、H2O和一种未知离子X
、H2O和一种未知离子X
①已知 在反应中得到电子,则X是
在反应中得到电子,则X是______ 。
②该反应的离子方程式是______ 。
(1)依据物质的性质分析:CaO、Na2O、Fe2O3、CuO均属于
a.水 b.盐酸 c.氢氧化钠溶液
(2)木炭与浓硫酸发生反应:
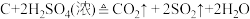 。作还原剂的物质是
。作还原剂的物质是(3)某反应中反应物与生成物的Fe3+、Mn2+、H+、
 、H2O和一种未知离子X
、H2O和一种未知离子X①已知
 在反应中得到电子,则X是
在反应中得到电子,则X是②该反应的离子方程式是
您最近一年使用:0次
3 . Ⅰ.根据物质的组成、结构、性质等进行分类,可预测物质的性质及变化:
(1)SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:___________ 。
(2)现有:①固体KOH②稀硫酸③氨气④熔融NaCl⑤蔗糖⑥铜;其中能导电的是___________ (填序号,下同)属于电解质的是___________ 。
(3)写出NaClO在水溶液中的电离方程式:___________ 。
Ⅱ.物质的量是联系宏观和微观的桥梁:
(4)40.5g某金属氯化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为___________ 。
(5)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为___________ 。
(6)由CO、CO2两气体组成的混合气体12.8g,标准状况下,体积为8.96L。则CO、CO2的物质的量之比为___________ 。
(7)在VmL的硫酸铁溶液中,含有mgFe3+离子,则此溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
(8)若用容量瓶以质量分数98%、密度为1.84g/cm3的浓硫酸配制480mL浓度0.2mol/L稀硫酸,计算需要用量筒量取___________ mL的浓硫酸。
(9)用4×10-3mol的KZO4恰好将60mL0.1mol/L的Na2SO3溶液氧化为Na2SO4,则元素Z在还原产物中的化合价是___________ 。
(1)SiO2是普通玻璃的主要成分,与CO2一样是酸性氧化物,写出SiO2溶于NaOH溶液的化学方程式:
(2)现有:①固体KOH②稀硫酸③氨气④熔融NaCl⑤蔗糖⑥铜;其中能导电的是
(3)写出NaClO在水溶液中的电离方程式:
Ⅱ.物质的量是联系宏观和微观的桥梁:
(4)40.5g某金属氯化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为
(5)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为
(6)由CO、CO2两气体组成的混合气体12.8g,标准状况下,体积为8.96L。则CO、CO2的物质的量之比为
(7)在VmL的硫酸铁溶液中,含有mgFe3+离子,则此溶液中
 的物质的量浓度为
的物质的量浓度为(8)若用容量瓶以质量分数98%、密度为1.84g/cm3的浓硫酸配制480mL浓度0.2mol/L稀硫酸,计算需要用量筒量取
(9)用4×10-3mol的KZO4恰好将60mL0.1mol/L的Na2SO3溶液氧化为Na2SO4,则元素Z在还原产物中的化合价是
您最近一年使用:0次
4 . 现有含HCl和 的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图:
的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图:
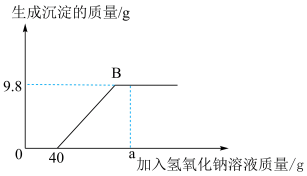
(1)当加入 溶液质量为ag时,溶液中的溶质有
溶液质量为ag时,溶液中的溶质有___________ (写出化学式);
(2)NaOH中Na元素的质量分数___________ (写出计算式);
(3)求混合溶液中 的质量分数
的质量分数___________ (写出计算过程);
(4)求恰好完全反应时,消耗NaOH溶液的总质量___________ (写出计算过程)。
 的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图:
的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图:
(1)当加入
 溶液质量为ag时,溶液中的溶质有
溶液质量为ag时,溶液中的溶质有(2)NaOH中Na元素的质量分数
(3)求混合溶液中
 的质量分数
的质量分数(4)求恰好完全反应时,消耗NaOH溶液的总质量
您最近一年使用:0次
2023-10-11更新
|
160次组卷
|
3卷引用:北京市首都师范大学附属中学2023-2024学年高一上学期10月月考化学试题
北京市首都师范大学附属中学2023-2024学年高一上学期10月月考化学试题(已下线)【精品卷】3.2.2 物质的量在化学方程式计算中的应用课堂例题-人教版2023-2024学年必修第一册12-2023新东方高二上期中考化学12
名校
5 . 根据所学知识,回答下列问题:
(1)硫酸的电离方程式为___________ ,9.8g硫酸溶解在___________ g水中,使H+与H2O个数比为1:50(忽略水的电离)。
(2)9.03×1023个NH3含___________ mol氢原子,在标准状况下的体积为___________ L。
(3)现有标准状况下的四种物质:①44.8L甲烷(CH4);②6.02×1024个水分子;③64gSO2;④0.5molCO2;它们中含有分子数最多的是(填序号,下同)___________ ,原子数最少的是___________ ,体积最大的是___________ 。
(4)在H、O、C、K四种元素中,选择适当的元素组成符合下列要求的物质,将它们的化学式填写在横线上。
①酸___________ ;②碱___________ ;③酸式盐___________ ;④酸性氧化物___________ ;⑤碱性氧化物___________ 。
(5)现有八种物质:①CO2②Na2CO3溶液③NaOH固体④CaCO3⑤醋酸⑥NH3·H2O⑦乙醇⑧液态氯化氢,其中属于电解质的有___________ (填序号,下同),属于非电解质的有___________ 。
(1)硫酸的电离方程式为
(2)9.03×1023个NH3含
(3)现有标准状况下的四种物质:①44.8L甲烷(CH4);②6.02×1024个水分子;③64gSO2;④0.5molCO2;它们中含有分子数最多的是(填序号,下同)
(4)在H、O、C、K四种元素中,选择适当的元素组成符合下列要求的物质,将它们的化学式填写在横线上。
①酸
(5)现有八种物质:①CO2②Na2CO3溶液③NaOH固体④CaCO3⑤醋酸⑥NH3·H2O⑦乙醇⑧液态氯化氢,其中属于电解质的有
您最近一年使用:0次



