1 . 铁、铜及其化合物之间的转化具有重要应用。下列说法错误 的是
| A.常温下使用铁质容器盛装浓硫酸 | B.氯化铁溶液在聚合物的基材上蚀刻出铜电路 |
| C.电解精炼铜时,粗铜连电源的正极 | D.饱和 溶液中滴加稀氨水制备氢氧化铁胶体 溶液中滴加稀氨水制备氢氧化铁胶体 |
您最近半年使用:0次
解题方法
2 . 下列几种物质:①NaHCO3晶体;②Na2O2;③NaHSO4溶液;④CO2;⑤Ba(OH)2溶液;⑥C2H5OH(酒精);⑦KMnO4;⑧氨水;⑨饱和FeCl3溶液。根据要求回答下列问题:
(1)上述各物质属于电解质的是_____ (填物质编号,下同);属于非电解质的是_____ 。
(2)③中盐的电离方程式为_____ ;
(3)③和⑧在水溶液中反应的离子方程式:_____ 。
(4)将⑨加入到沸水中,继续加热溶液呈红褐色,即制得Fe(OH)3胶体,写出该反应的离子方程式:_____ 。
(1)上述各物质属于电解质的是
(2)③中盐的电离方程式为
(3)③和⑧在水溶液中反应的离子方程式:
(4)将⑨加入到沸水中,继续加热溶液呈红褐色,即制得Fe(OH)3胶体,写出该反应的离子方程式:
您最近半年使用:0次
解题方法
3 . 研究物质性质具有重要的价值,根据所学知识回答下列问题:
(1)FeCl3是黑棕色晶体,主要用于金属蚀刻,污水处理。按照物质的分类方法,FeCl3应属于___________ (填序号)。
①酸;②氯化物;③混合物;④盐;⑤化合物;⑥电解质;⑦易溶于水物质
(2)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为___________ ;判断胶体制备是否成功可利用胶体的___________ ;
(3)铁元素是组成人体必不可少的元素之一,以下几种常见的铁元素粒子,既有氧化性又有还原性的是___________ 。
A.Fe B.Fe2+ C.Fe3+
(4)火药是中国的四大发明之一,永远值得华夏儿女骄傲。黑火药在发生爆炸时,发生反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。上述反应中氧化剂:___________ ;氧化产物:___________ 。
(1)FeCl3是黑棕色晶体,主要用于金属蚀刻,污水处理。按照物质的分类方法,FeCl3应属于
①酸;②氯化物;③混合物;④盐;⑤化合物;⑥电解质;⑦易溶于水物质
(2)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为
(3)铁元素是组成人体必不可少的元素之一,以下几种常见的铁元素粒子,既有氧化性又有还原性的是
A.Fe B.Fe2+ C.Fe3+
(4)火药是中国的四大发明之一,永远值得华夏儿女骄傲。黑火药在发生爆炸时,发生反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。上述反应中氧化剂:
您最近半年使用:0次
名校
解题方法
4 . 现有以下物质:a. 溶液,b.液氨,c.
溶液,b.液氨,c. 固体,d.
固体,d. 固体,e.Fe
固体,e.Fe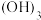 胶体,f.铜,g.
胶体,f.铜,g. ,h.
,h. ,i.熔融
,i.熔融 ,J.稀硫酸
,J.稀硫酸 .澄清石灰水 l.蔗糖
.澄清石灰水 l.蔗糖 .酒精
.酒精
(1)①以上物质中属于非电解质的是_______ (填字母,下同),属于电解质的有_______ ,能导电的有_______ 。
②写出 在水溶液中电离方程式:
在水溶液中电离方程式:_______ 。
③在足量 的水溶液中加入少量
的水溶液中加入少量 的水溶液,发生反应的离子方程式为
的水溶液,发生反应的离子方程式为_______ 。
④在含 的水溶液中缓缓通少量
的水溶液中缓缓通少量 ,该过程的离子反应方程式为
,该过程的离子反应方程式为_______ 。
(2)向煮沸的蒸馏水中逐滴加入饱和 溶液,继续煮沸至溶液呈红褐色,停止加热,可制得
溶液,继续煮沸至溶液呈红褐色,停止加热,可制得 胶体。
胶体。
①制取 胶体的离子方程式为
胶体的离子方程式为_______ 。
②下列描述的分别是胶体的性质或现象,请按要求填空:
A.胶体的聚沉
B.胶体的电泳
C.丁达尔效应
区分胶体和溶液的方法是_______ (填字母,下同);“卢水点豆腐”,利用的性质是_______ ;工厂采用高压静电除尘,利用的胶体性质是_______ 。
 溶液,b.液氨,c.
溶液,b.液氨,c. 固体,d.
固体,d. 固体,e.Fe
固体,e.Fe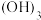 胶体,f.铜,g.
胶体,f.铜,g. ,h.
,h. ,i.熔融
,i.熔融 ,J.稀硫酸
,J.稀硫酸 .澄清石灰水 l.蔗糖
.澄清石灰水 l.蔗糖 .酒精
.酒精(1)①以上物质中属于非电解质的是
②写出
 在水溶液中电离方程式:
在水溶液中电离方程式:③在足量
 的水溶液中加入少量
的水溶液中加入少量 的水溶液,发生反应的离子方程式为
的水溶液,发生反应的离子方程式为④在含
 的水溶液中缓缓通少量
的水溶液中缓缓通少量 ,该过程的离子反应方程式为
,该过程的离子反应方程式为(2)向煮沸的蒸馏水中逐滴加入饱和
 溶液,继续煮沸至溶液呈红褐色,停止加热,可制得
溶液,继续煮沸至溶液呈红褐色,停止加热,可制得 胶体。
胶体。①制取
 胶体的离子方程式为
胶体的离子方程式为②下列描述的分别是胶体的性质或现象,请按要求填空:
A.胶体的聚沉
B.胶体的电泳
C.丁达尔效应
区分胶体和溶液的方法是
您最近半年使用:0次
5 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.常温常压下,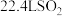 含有的分子数目为 含有的分子数目为 |
B. 溶液含有的 溶液含有的 数目为 数目为 |
C.常温常压下,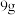 纯水中H原子数为 纯水中H原子数为 |
D.将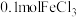 溶于沸水制成胶体,其中含有的胶体粒子数目为 溶于沸水制成胶体,其中含有的胶体粒子数目为 |
您最近半年使用:0次
2024-04-01更新
|
63次组卷
|
2卷引用:福建省漳州市东山第二中学等校2023-2024学年高一上学期期中联考化学试题
6 . 下列叙述均正确且存在因果关系的是
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | 氯水具有漂白性 |
|
B |
| 饱和 |
C |
| 可用 |
D | 胶体具有丁达尔效应 | 用可见光束照射可区分胶体和溶液 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
7 . 下列有关实验的说法不正确的是
| A.为防止试剂污染,取用金属钠后多余的钠不能放回原试剂瓶 |
| B.做焰色试验前,铂丝用稀盐酸清洗并灼烧至与原来的火焰颜色相同 |
| C.向碳酸钠固体滴加几滴蒸馏水,碳酸钠结块变晶体,温度升高,说明碳酸钠遇水是一个放热反应 |
| D.向沸腾的蒸馏水中滴加饱和的氯化铁溶液,可以得到氢氧化铁胶体 |
您最近半年使用:0次
8 . 下列实验操作规范且能达到实验目的的是
| 实验操作 |  | 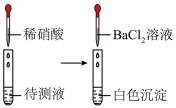 | 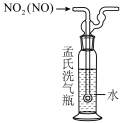 | 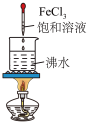 |
| 实验目的 | A.NaCl溶液蒸发结晶 | B.检验待测液中是否含有SO | C.除去NO2中的NO | D.制备Fe(OH)3胶体 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
9 . 新型冠状病毒可通过气溶胶传播,气溶胶属于胶体的一种。下列有关胶体的叙述正确的是
| A.雾是气溶胶,在阳光下可观察到丁达尔效应 |
| B.将Fe(OH)3胶体过滤,在滤纸上能得到分散质 |
| C.向有污染的水中加入胶体,具有杀菌消毒的作用 |
| D.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色的Fe(OH)3胶体 |
您最近半年使用:0次
解题方法
10 . 下列说法正确的是
①把几滴FeCl3饱和溶液滴入250 mL的沸水中制取Fe(OH)3胶体
②胶体都是均匀、透明的液体
③河流在入海口形成的沙洲,原因是胶体遇电解质溶液而聚沉
④胶体不稳定,静置后容易产生沉淀
⑤直径为1.3×10-9 m的“钴酞菁”分子分散在水中能形成胶体,该分子的直径比Na+的大
①把几滴FeCl3饱和溶液滴入250 mL的沸水中制取Fe(OH)3胶体
②胶体都是均匀、透明的液体
③河流在入海口形成的沙洲,原因是胶体遇电解质溶液而聚沉
④胶体不稳定,静置后容易产生沉淀
⑤直径为1.3×10-9 m的“钴酞菁”分子分散在水中能形成胶体,该分子的直径比Na+的大
| A.①③⑤ | B.①③④ | C.①②③④ | D.②③④⑤ |
您最近半年使用:0次

 具有氧化性
具有氧化性 胶体
胶体 的金属性比
的金属性比 强
强 溶液反应制取
溶液反应制取

