解题方法
1 . 下列几种物质:①NaHCO3晶体;②Na2O2;③NaHSO4溶液;④CO2;⑤Ba(OH)2溶液;⑥C2H5OH(酒精);⑦KMnO4;⑧氨水;⑨饱和FeCl3溶液。根据要求回答下列问题:
(1)上述各物质属于电解质的是_____ (填物质编号,下同);属于非电解质的是_____ 。
(2)③中盐的电离方程式为_____ ;
(3)③和⑧在水溶液中反应的离子方程式:_____ 。
(4)将⑨加入到沸水中,继续加热溶液呈红褐色,即制得Fe(OH)3胶体,写出该反应的离子方程式:_____ 。
(1)上述各物质属于电解质的是
(2)③中盐的电离方程式为
(3)③和⑧在水溶液中反应的离子方程式:
(4)将⑨加入到沸水中,继续加热溶液呈红褐色,即制得Fe(OH)3胶体,写出该反应的离子方程式:
您最近一年使用:0次
解题方法
2 . Ⅰ.某课外活动小组进行 胶体的制备实验并检验其相关性质.
胶体的制备实验并检验其相关性质.
(1)若将 饱和溶液分别滴入下列物质中,能形成胶体的是_______.
饱和溶液分别滴入下列物质中,能形成胶体的是_______.
(2)写出制备 胶体的离子方程式:
胶体的离子方程式:______________________________ .
(3) 胶体区别于
胶体区别于 溶液最本质的特征是_______.
溶液最本质的特征是_______.
Ⅱ.实验室可利用 溶液和
溶液和 溶液制备
溶液制备 胶体,也可以反应得到
胶体,也可以反应得到 悬浊液,图中圆的大小代表分散质粒子的相对大小.
悬浊液,图中圆的大小代表分散质粒子的相对大小.

(4)分散系Ⅰ是_______ ,分散系Ⅱ是__________________ ,判断依据是____________________________________ .
(5)制备分散系Ⅱ的化学方程式为____________________ ,该反应属于______________ (填基本反应类型).
(6)区分分散系和分散系Ⅱ的简单方法是__________________ .
 胶体的制备实验并检验其相关性质.
胶体的制备实验并检验其相关性质.(1)若将
 饱和溶液分别滴入下列物质中,能形成胶体的是_______.
饱和溶液分别滴入下列物质中,能形成胶体的是_______.| A.冷水 | B.沸水 | C. 浓溶液 浓溶液 | D. 浓溶液 浓溶液 |
(2)写出制备
 胶体的离子方程式:
胶体的离子方程式:(3)
 胶体区别于
胶体区别于 溶液最本质的特征是_______.
溶液最本质的特征是_______.A. 胶体粒子的直径为 胶体粒子的直径为 | B. 胶体具有丁达尔效应 胶体具有丁达尔效应 |
C. 胶体是均一的分散系 胶体是均一的分散系 | D. 胶体的分散质粒子能透过滤纸 胶体的分散质粒子能透过滤纸 |
Ⅱ.实验室可利用
 溶液和
溶液和 溶液制备
溶液制备 胶体,也可以反应得到
胶体,也可以反应得到 悬浊液,图中圆的大小代表分散质粒子的相对大小.
悬浊液,图中圆的大小代表分散质粒子的相对大小.
(4)分散系Ⅰ是
(5)制备分散系Ⅱ的化学方程式为
(6)区分分散系和分散系Ⅱ的简单方法是
您最近一年使用:0次
名校
解题方法
3 . 下列实验能够达到相应目的的是
| A | B | C | D |
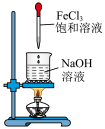 | 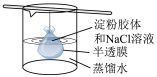 | 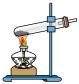 | 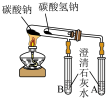 |
将 饱和溶液滴入热NaOH溶液中制备氢氧化铁胶体 饱和溶液滴入热NaOH溶液中制备氢氧化铁胶体 | 一段时间后,若往B烧杯中液体滴加硝酸酸化硝酸银有白色沉淀,则半透膜破损 | C装置可用于固体碳酸氢钠加热分解 | D装置可用于比较碳酸钠和碳酸氢钠的热稳定性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-19更新
|
161次组卷
|
2卷引用:湖北省宜昌市三峡高级中学2023-2024学年高一上学期10月月考化学试题
4 . 下列实验过程不能达到实验目的的是
| 编号 | 实验目的 | 实验过程 |
| A | 称量 的 的 固体 固体 | 在小烧杯中称取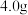 固体 固体 , , |
| B | 检验 溶液中的 溶液中的 | 用铁丝蘸取溶液在外焰上灼烧,看到黄色火焰 |
| C | 制取干燥纯净的氯气 | 在加热条件下,向浓盐酸中加入二氧化锰固体,将生成的气体依次通过饱和食盐水、浓硫酸、然后收集 |
| D | 制备 胶体 胶体 | 将 溶液滴加到饱和 溶液滴加到饱和 溶液中 溶液中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . Ⅰ. 胶体的制备和性质
胶体的制备和性质
在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,继续煮沸并用玻璃棒搅拌至溶液呈红褐色,停止加热,即制得
溶液,继续煮沸并用玻璃棒搅拌至溶液呈红褐色,停止加热,即制得 胶体。
胶体。
(1)①请指出描述中错误的操作原文_____ ,②写出制备 胶体的化学方程式
胶体的化学方程式_____ 。
(2)乙同学将用氯化铁溶液制得的氢氧化铁胶体放入半透膜制成的袋内,如图所示,放置10min后,再更换烧杯中的蒸馏水。该操作称为_____ ,可用于分离胶体与溶液;
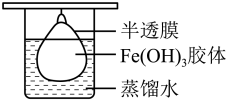
(3)取少量半透膜外最初的液体于试管中,置于暗处用一束强光从侧面照射,_____ (填“能”或“不能”)观察到丁达尔现象。
(4)向置于U形玻璃管中的氢氧化铁胶体中插入两根电极,接通直流电源,发现负极附近红褐色加深,说明氢氧化铁胶粒带_____ 电荷。
Ⅱ.离子反应在工农业生产和日常生活中有着广泛的应用:
(5)工业上得到的粗盐中往往含有 、
、 ,要除去这两种离子,需要加入试剂的化学式依次为NaOH、
,要除去这两种离子,需要加入试剂的化学式依次为NaOH、_____ 、_____ ,然后通过_____ (填操作名称)后,再加入适量的盐酸调节溶液呈中性,通过_____ (填操作名称)得到氯化钠固体。
 胶体的制备和性质
胶体的制备和性质在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和
 溶液,继续煮沸并用玻璃棒搅拌至溶液呈红褐色,停止加热,即制得
溶液,继续煮沸并用玻璃棒搅拌至溶液呈红褐色,停止加热,即制得 胶体。
胶体。(1)①请指出描述中错误的操作原文
 胶体的化学方程式
胶体的化学方程式(2)乙同学将用氯化铁溶液制得的氢氧化铁胶体放入半透膜制成的袋内,如图所示,放置10min后,再更换烧杯中的蒸馏水。该操作称为

(3)取少量半透膜外最初的液体于试管中,置于暗处用一束强光从侧面照射,
(4)向置于U形玻璃管中的氢氧化铁胶体中插入两根电极,接通直流电源,发现负极附近红褐色加深,说明氢氧化铁胶粒带
Ⅱ.离子反应在工农业生产和日常生活中有着广泛的应用:
(5)工业上得到的粗盐中往往含有
 、
、 ,要除去这两种离子,需要加入试剂的化学式依次为NaOH、
,要除去这两种离子,需要加入试剂的化学式依次为NaOH、
您最近一年使用:0次
6 . 化学实验操作有严格的规范,下列实验操作描述错误的是
| A.实验剩余的钠块可以放回原瓶 |
| B.进行焰色试验前,将铂丝用硫酸清洗 |
| C.向试管中滴加试剂时,滴管下端不能接触试管内壁 |
| D.制备氢氧化铁胶体实验时,不宜用玻璃棒搅拌,也不宜使液体沸腾时间过长 |
您最近一年使用:0次
2023-10-17更新
|
381次组卷
|
5卷引用:湖北省重点高中智学联盟2023-2024学年高一上学期10月联考化学试题
名校
解题方法
7 . 下列事实与胶体性质有关的是
①将植物油倒入水中用力搅拌形成油水混合物
②水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染
③节日晚上广场的灯光射向天空,看到一条条五彩的光路
④新冠病毒在空气中可以较长时间存在而传播
⑤胃蛋白酶合剂中的胃蛋白酶,在酸性环境中带正电荷,而一般的滤纸、纱布等纤维性滤材是带负电荷的,因此在制备该合剂时,为避免中和而使胃蛋白酶析出在滤纸上而降低药效,应避免过滤
⑥向 溶液中滴入NaOH溶液出现红褐色沉淀
溶液中滴入NaOH溶液出现红褐色沉淀
⑦江河入海处易形成三角洲
⑧利用血清的纸上电泳以分离各种氨基酸和蛋白质
①将植物油倒入水中用力搅拌形成油水混合物
②水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染
③节日晚上广场的灯光射向天空,看到一条条五彩的光路
④新冠病毒在空气中可以较长时间存在而传播
⑤胃蛋白酶合剂中的胃蛋白酶,在酸性环境中带正电荷,而一般的滤纸、纱布等纤维性滤材是带负电荷的,因此在制备该合剂时,为避免中和而使胃蛋白酶析出在滤纸上而降低药效,应避免过滤
⑥向
 溶液中滴入NaOH溶液出现红褐色沉淀
溶液中滴入NaOH溶液出现红褐色沉淀⑦江河入海处易形成三角洲
⑧利用血清的纸上电泳以分离各种氨基酸和蛋白质
| A.①②④⑤⑦ | B.②③④⑥⑦⑧ | C.②③④⑤⑦⑧ | D.①②③④⑤⑦ |
您最近一年使用:0次
8 . 烧杯中装有一定较稀浓度的FeCl3和FeCl2混合溶液,往里面滴加稀NaOH溶液可得到一种黑色分散系,经分析得知该分散质粒子是直径约为9.3nm的Fe3O4,请填空:
(1)写出FeCl3的电离方程式:___________ 。
(2)根据分散质粒子直径大小,可知该分散系为___________ ,证明方法为:___________ 。(写出实验过程)
(3)得到的黑色分散系中,含有少量Na+和Cl—,___________ (填“能”或“不能”)用过滤的方法除去,原因是___________ 。
(4)FeCl2溶液中通入Cl2可生成FeCl3,写出该反应离子方程式___________ 。
(5)写出实验室用FeCl3溶液制备Fe(OH)3胶体的化学方程式___________ 。
(1)写出FeCl3的电离方程式:
(2)根据分散质粒子直径大小,可知该分散系为
(3)得到的黑色分散系中,含有少量Na+和Cl—,
(4)FeCl2溶液中通入Cl2可生成FeCl3,写出该反应离子方程式
(5)写出实验室用FeCl3溶液制备Fe(OH)3胶体的化学方程式
您最近一年使用:0次
2023-10-09更新
|
59次组卷
|
2卷引用:湖北省宜昌市部分省级示范高中2023-2024学年高一上学期9月考试化学试题
名校
解题方法
9 . 某校学生在学习完胶体的知识后,利用化学兴趣社团活动时间,在实验室中用饱和FeCl3溶液制备Fe(OH)3胶体。具体操作是:取一支烧杯,加入适量的蒸馏水,加热至沸腾。将少量饱和FeCl3溶液分多次缓慢滴入,继续加热至刚好变成红褐色,停止加热。
(1)该反应的化学方程式为___________ 。证明有氢氧化铁胶体生成的实验操作和现象是___________ 。
(2)乙同学认为Fe(OH)3胶体中可能含有FeCl3溶液,为了提纯Fe(OH)3胶体,他可以采用的提纯方法是___________ 。
(3)丙同学将制备好的Fe(OH)3胶体装入U型玻璃管中,插入电极,连通直流电,进行电泳
实验。一段时间后,观察到阴极附近液体颜色加深,原因是:___________ 。
(4)丁同学取适量Fe(OH)3胶体于试管,然后用胶头滴管逐滴向试管中加入稀硫酸,看到的现象是先产生红褐色沉淀,原因是:___________ ,随着稀硫酸的不断滴加,沉淀又溶解,发生的离子反应为:___________ 。
(1)该反应的化学方程式为
(2)乙同学认为Fe(OH)3胶体中可能含有FeCl3溶液,为了提纯Fe(OH)3胶体,他可以采用的提纯方法是
(3)丙同学将制备好的Fe(OH)3胶体装入U型玻璃管中,插入电极,连通直流电,进行电泳
实验。一段时间后,观察到阴极附近液体颜色加深,原因是:
(4)丁同学取适量Fe(OH)3胶体于试管,然后用胶头滴管逐滴向试管中加入稀硫酸,看到的现象是先产生红褐色沉淀,原因是:
您最近一年使用:0次
10 . 下列实验过程可以达到实验目的的是
| 选项 | 实验目的 | 实验过程 |
| A | 配制 的 的 溶液 溶液 | 称取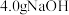 固体于烧杯中,加入少量蒸馏水溶解,转移至 固体于烧杯中,加入少量蒸馏水溶解,转移至 容量瓶中定容 容量瓶中定容 |
| B | 制备 胶体 胶体 | 将 浓溶液滴加到 浓溶液滴加到 饱和溶液中 饱和溶液中 |
| C | 制取干燥、纯净的氢气 | 向稀盐酸中加入锌粒,将生成的气体依次通过浓硫酸、 溶液,然后收集 溶液,然后收集 |
| D | 检验 溶液中的 溶液中的 | 用光洁无锈的铁丝蘸取溶液﹐在酒精灯外焰上灼烧,透过蓝色钴玻璃看到紫色火焰 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



