解题方法
1 . 特殊的分散系——胶体
把一种或多种物质分散在另一种物质中所得到的体系称为分散系,接照分散质的大小可将分散系分为溶液、胶体和浊液三类。三者之间无明显界限。胶体是物质的一种分散状态,比较稳定,外观上胶体溶液不浑浊,用肉眼或普通显微镜均不能辨别。很多蛋白质、淀粉、血液、淋巴液等都属于胶体。胶体还可以按照分散剂的状态分为固溶胶如有色玻璃、气溶胶如雾、烟和液溶胶如FeOH3胶体。1.胶体可以稳定存在的主要原因是______。
| A.胶体粒子直径在1~100nm之间 | B.胶体具有丁达尔现象 |
| C.胶粒带电 | D.胶体外观均匀 |
| A.在豆浆中加入盐卤做豆腐 |
| B.河流入海处易形成沙洲 |
| C.一束平行光线照射蛋白质溶液时,从侧面可看到光亮的通路 |
| D.三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 |
| A.蛋白质溶液 | B.氨水 | C.食盐水 | D.酒精溶液 |
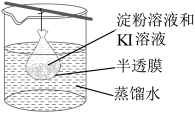
5.在小烧杯中加入20mL蒸馏水加热煮沸后,向沸水申滴入几滴饱和的FeCl3溶液,继续煮沸至溶液呈色即制得FeOH3胶体。
①写出上述胶体制备的化学反应方程式
②取制得的FeOH3胶体装入U形管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色加深,说明氢氧化铁胶粒带
③另取制得的FeOH3胶体于洁净的试管中,向其中逐滴滴加过量稀硫酸,边滴边振荡,观察到的现象是
您最近一年使用:0次
2 . 下列实验操作描述正确的是
| A.制备氢氧化铁胶体实验时,用玻璃棒搅拌可加快反应速率 |
| B.进行焰色试验时如无铂丝,可以用洁净的铁丝代替 |
| C.实验剩余的药品都不可以放回原瓶 |
| D.坩埚不可以用明火直接加热 |
您最近一年使用:0次
2024-02-10更新
|
209次组卷
|
2卷引用:云南师范大学附属中学2023-2024学年高一上学期1月教学测评期末化学试题
解题方法
3 . 室温下进行下列实验,根据实验操作和现象所得结论或目的正确的是
| 选项 | 实验操作和现象 | 结论或目的 |
| A | 将有色鲜花放入盛有干燥氯气的集气瓶中,盖上玻璃片,有色鲜花逐渐褪色 | 氯气具有漂白性 |
| B | 将混有HCl的 气体通入饱和 气体通入饱和 溶液中 溶液中 | 除去HCl杂质 |
| C | 用铂丝(或铁丝)蘸取某白色粉末做焰色试验,火焰呈黄色 | 原粉末中有 ,无 ,无 |
| D | 向沸腾的NaOH溶液中边滴加 饱和溶液,边用玻璃棒搅动,然后继续煮沸 饱和溶液,边用玻璃棒搅动,然后继续煮沸 | 制备 胶体 胶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 化学是一门以实验为基础的学科。回答下列问题:
Ⅰ.影响化学平衡的因素
 溶液中存在平衡:
溶液中存在平衡: (蓝色)
(蓝色)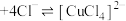 (黄色)
(黄色)
(1)取两支试管,分别加入2 mL 0.5 mol/L 溶液,溶液呈绿色,其原因为
溶液,溶液呈绿色,其原因为____________ 。
(2)将其中一支试管加热,溶液变为黄绿色,则该反应的
______ 0(填“>”或“<”),在另一支试管中加入5滴 溶液,静置,上层清液呈
溶液,静置,上层清液呈______ 色。
Ⅱ.电离平衡常数
(3) 是二元弱酸,其电离平衡常数
是二元弱酸,其电离平衡常数 的表达式为
的表达式为______ 。
(4)向盛有2 mL 1 mol/L醋酸的试管中滴加1 mol/L 溶液,观察到试管中有气泡产生,由此推断的
溶液,观察到试管中有气泡产生,由此推断的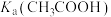
______ 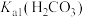 (填“>”或“<”),发生反应的离子方程式为
(填“>”或“<”),发生反应的离子方程式为____________ 。
Ⅲ.盐类水解的应用
(5)向一支试管中加入少量 晶体,然后加入5 mL蒸馏水、振荡,观察到
晶体,然后加入5 mL蒸馏水、振荡,观察到 慢慢溶解,但有少量浑浊,此溶液的pH
慢慢溶解,但有少量浑浊,此溶液的pH______ 7(填“>”“<”或“=”),配制 溶液的正确方法是
溶液的正确方法是____________ 。
(6)向一个烧杯中加入40 mL蒸馏水,加热至水沸腾,然后向沸水中逐滴加入5~6滴饱和 溶液,继续煮沸制得
溶液,继续煮沸制得 胶体。该反应的化学方程式为
胶体。该反应的化学方程式为____________ , 胶体呈
胶体呈______ 色。
Ⅳ.亚铁离子的检验
(7) 与
与______ 色的 溶液反应有特征蓝色沉淀产生,这是检验溶液中
溶液反应有特征蓝色沉淀产生,这是检验溶液中 的常用方法。写出该反应的离子方程式:
的常用方法。写出该反应的离子方程式:____________ 。
Ⅰ.影响化学平衡的因素
 溶液中存在平衡:
溶液中存在平衡: (蓝色)
(蓝色)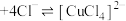 (黄色)
(黄色)
(1)取两支试管,分别加入2 mL 0.5 mol/L
 溶液,溶液呈绿色,其原因为
溶液,溶液呈绿色,其原因为(2)将其中一支试管加热,溶液变为黄绿色,则该反应的

 溶液,静置,上层清液呈
溶液,静置,上层清液呈Ⅱ.电离平衡常数
(3)
 是二元弱酸,其电离平衡常数
是二元弱酸,其电离平衡常数 的表达式为
的表达式为(4)向盛有2 mL 1 mol/L醋酸的试管中滴加1 mol/L
 溶液,观察到试管中有气泡产生,由此推断的
溶液,观察到试管中有气泡产生,由此推断的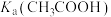
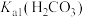 (填“>”或“<”),发生反应的离子方程式为
(填“>”或“<”),发生反应的离子方程式为Ⅲ.盐类水解的应用
(5)向一支试管中加入少量
 晶体,然后加入5 mL蒸馏水、振荡,观察到
晶体,然后加入5 mL蒸馏水、振荡,观察到 慢慢溶解,但有少量浑浊,此溶液的pH
慢慢溶解,但有少量浑浊,此溶液的pH 溶液的正确方法是
溶液的正确方法是(6)向一个烧杯中加入40 mL蒸馏水,加热至水沸腾,然后向沸水中逐滴加入5~6滴饱和
 溶液,继续煮沸制得
溶液,继续煮沸制得 胶体。该反应的化学方程式为
胶体。该反应的化学方程式为 胶体呈
胶体呈Ⅳ.亚铁离子的检验
(7)
 与
与 溶液反应有特征蓝色沉淀产生,这是检验溶液中
溶液反应有特征蓝色沉淀产生,这是检验溶液中 的常用方法。写出该反应的离子方程式:
的常用方法。写出该反应的离子方程式:
您最近一年使用:0次
2024-02-11更新
|
82次组卷
|
2卷引用:天津市南开区2023-2024学年高二上学期期末测试化学试题
真题
5 . 氯化铁是一种重要的盐,下列说法不正确的是
| A.氯化铁属于弱电解质 | B.氯化铁溶液可腐蚀覆铜板 |
| C.氯化铁可由铁与氯气反应制得 | D.氯化铁溶液可制备氢氧化铁胶体 |
您最近一年使用:0次
2023-06-21更新
|
5235次组卷
|
9卷引用:2023年高考浙江卷化学真题(6月)
2023年高考浙江卷化学真题(6月)(已下线)2023年高考浙江卷化学真题(6月)变式题(选择题1-5)(已下线)考点10 铁及其重要化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点14 铁及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题06 元素及其化合物 -2023年高考化学真题题源解密(新高考专用)(已下线)实验05 盐类水解的应用-【同步实验课】2023-2024学年高二化学教材实验大盘点(人教版2019选择性必修1)(已下线)题型01 物质的组成与分类 传统文化 化学用语-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题05 盐类的水解-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)江西省宜春市百树学校2023-2024学年高三上学期暑期阶段测试化学试卷
6 . 下列关于元素及其化合物的性质说法不正确的是
| A.Si粉加入浓盐酸中可转化为SiHCl3 |
| B.FeCl3溶液滴入沸水中可转化为Fe(OH)3胶体 |
| C.葡萄糖在酶的作用下可转化为乙醇 |
| D.K2CrO4溶液加硫酸可转化为K2Cr2O7 |
您最近一年使用:0次
2023-04-14更新
|
380次组卷
|
3卷引用:浙江省金华市十校2023届高三下学期4月模拟考试化学试题
解题方法
7 . 某小组研究实验室制备Fe(OH)3胶体的方法。下列说法不正确 的是
| 序号 | 1 | 2 |
| 实验 |  | 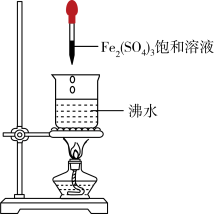 |
| 现象 | 液体变为红褐色后,停止加热,有明显的丁达尔效应,冷却后仍为红褐色 | 液体变为红褐色后,停止加热,有明显的丁达尔效应,冷却后溶液变黄 |
| A.对比实验可知,制备Fe(OH)3胶体选用饱和FeCl3溶液效果更好 |
| B.实验1中液体变红褐色后,持续加热可观察到红褐色沉淀 |
| C.选用饱和溶液以及加热,均为了促进Fe3+的水解 |
| D.对比实验可知,酸根离子不同是造成实验现象差异的重要原因 |
您最近一年使用:0次
2023-01-05更新
|
213次组卷
|
2卷引用:北京市丰台区2022-2023学年高三上学期期末考试化学试题
名校
解题方法
8 . 如图所示为实验室中制备胶体的一种方法。下列说法正确的是
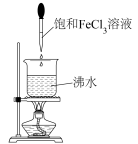

| A.该制备方法属于物理方法 | B.烧杯中液体的颜色逐渐变浅 |
| C.可用丁达尔效应判断是否制得胶体 | D.加热能促使该分散系中的分散质粒子直径减小 |
您最近一年使用:0次
2023-01-05更新
|
413次组卷
|
7卷引用:北京市东城区2022-2023学年高一上学期期末统一检测化学试卷
名校
解题方法
9 . 下列说法错误的是
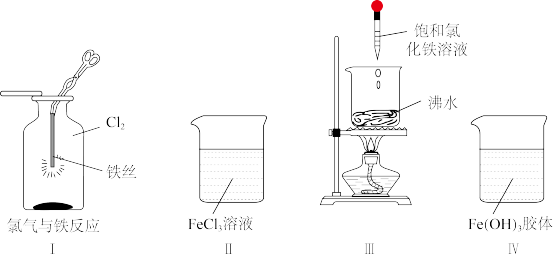
| A.I中铁丝在氯气中剧烈燃烧,该反应体现氯气的助燃性 |
| B.分散质粒子的直径大小:氯化铁溶液<氢氧化铁胶体 |
| C.制备氢氧化铁胶体时,在不断搅拌下向沸水中加入过量的饱和氯化铁溶液 |
| D.用一束光照射II和IV的分散系,IV中能看到一条光亮的“通路” |
您最近一年使用:0次
2022-10-28更新
|
292次组卷
|
5卷引用:河南省南阳六校2022-2023学年高一上学期期中考试化学试题
10 . 完成表格中的内容
| 实验题目 | 利用盐类水解制备胶体、净水和除污 | ||
| 实验目的 | 利用水解反应解决实际问题 | ||
| 实验用品 | Na2CO3溶液,Al2(SO4)3溶液,饱和FeCl3溶液,稀盐酸,植物油,蒸馏水,略浑浊的天然淡水,试管,烧杯,胶头滴管,酒精灯,三脚架,石棉网,激光笔 | ||
| 实验方案设计及实施 | 利用所提供的实验用品,设计并实施实验,解决下列实际问题。 1.制备氢氧化铁胶体。 2.除去略浑浊的天然淡水中的悬浮颗粒物。 3.清除厨房的油污。 | ||
| 实验内容 | 实验 | 实验方案 | 试验现象和结论 |
| 1 | 将蒸馏水煮沸,向煮沸的蒸馏水中逐滴加入饱和FeCl3,继续煮沸至溶液呈透明的红褐色。然后用激光笔从侧面照射。 | ||
| 2 | 向略浑浊的天然淡水中加入Al2(SO4)3溶液。 | ||
| 3 | 取适量蒸馏水与试管,加入适量油脂然后加入碳酸钠溶液振荡。 | ||
您最近一年使用:0次



