名校
1 . 草酸(H2C2O4)及其盐类化合物在化学工业中有重要作用。请回答下列问题:
(1)实验室中可以在50℃左右,用浓硝酸在硝酸汞催化下氧化乙炔(C2H2)气体来制备草酸。其主要装置如下图。
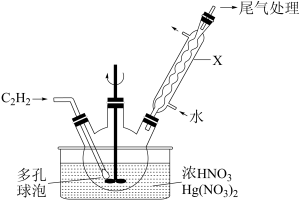
C2H2的电子式为____ ;仪器X的名称为____ ;装置中浓硝酸的还原产物为NO2,生成草酸的化学方程式为____ ,若反应温度高于50℃,生成草酸的速率会减慢,主要原因是____ 。
(2)三草酸合铁酸钾{K3[Fe(C2O4)3]·3H2O}为绿色晶体,溶于水,难溶于乙醇,可作有机反应的催化剂。某实验小组用(NH4)2Fe(SO4)2·6H2O为原料制备三草酸合铁酸钾的步骤如下:
①称取5g(NH4)2Fe(SO4)2·6H2O固体,溶解,加硫酸酸化,搅拌下加入25mL1mol·L-1H2C2O4溶液,静置,析出黄色的FeC2O4·2H2O沉淀,过滤并洗涤沉淀2~3次。
②将上述FeC2O4·2H2O沉淀溶解在10mL饱和草酸钾溶液中,再加入20mL饱和H2C2O4溶液,保持溶液温度40℃左右,缓慢滴加3%H2O2溶液,不断搅拌,沉淀慢慢变为深棕色;加热至沸腾30min,再加入8~9mL草酸溶液,控制pH在3~4,变为绿色透明的三草酸合铁酸钾溶液。
③加热浓缩,缓慢加入95%的乙醇,冷却结晶、过滤,洗涤晶体2~3次,干燥、称量。
其中,生成FeC2O4·2H2O的化学方程式为____ ;保持溶液温度40℃所采用的加热方法是____ ,加热至沸腾30min的目的是____ ;洗涤晶体所用试剂为____ 。
(3)制得的三草酸合铁酸钾晶体中往往会混有少量草酸。为测定K3[Fe(C2O4)3]·3H2O(M=491g/mol)的纯度,进行如下实验:
称取样品10.72g,加稀硫酸溶解后配成100mL溶液。取20.00mL配制的溶液,用浓度为0.2000mol·L-1的KMnO4溶液滴定至终点时消耗KMnO4溶液28.00mL。已知:5H2C2O4+2 +6H+=2Mn2++10CO2↑+8H2O,样品中K3[Fe(C2O4)3]·3H2O的质量分数为
+6H+=2Mn2++10CO2↑+8H2O,样品中K3[Fe(C2O4)3]·3H2O的质量分数为_______ (保留两位小数)。
(1)实验室中可以在50℃左右,用浓硝酸在硝酸汞催化下氧化乙炔(C2H2)气体来制备草酸。其主要装置如下图。

C2H2的电子式为
(2)三草酸合铁酸钾{K3[Fe(C2O4)3]·3H2O}为绿色晶体,溶于水,难溶于乙醇,可作有机反应的催化剂。某实验小组用(NH4)2Fe(SO4)2·6H2O为原料制备三草酸合铁酸钾的步骤如下:
①称取5g(NH4)2Fe(SO4)2·6H2O固体,溶解,加硫酸酸化,搅拌下加入25mL1mol·L-1H2C2O4溶液,静置,析出黄色的FeC2O4·2H2O沉淀,过滤并洗涤沉淀2~3次。
②将上述FeC2O4·2H2O沉淀溶解在10mL饱和草酸钾溶液中,再加入20mL饱和H2C2O4溶液,保持溶液温度40℃左右,缓慢滴加3%H2O2溶液,不断搅拌,沉淀慢慢变为深棕色;加热至沸腾30min,再加入8~9mL草酸溶液,控制pH在3~4,变为绿色透明的三草酸合铁酸钾溶液。
③加热浓缩,缓慢加入95%的乙醇,冷却结晶、过滤,洗涤晶体2~3次,干燥、称量。
其中,生成FeC2O4·2H2O的化学方程式为
(3)制得的三草酸合铁酸钾晶体中往往会混有少量草酸。为测定K3[Fe(C2O4)3]·3H2O(M=491g/mol)的纯度,进行如下实验:
称取样品10.72g,加稀硫酸溶解后配成100mL溶液。取20.00mL配制的溶液,用浓度为0.2000mol·L-1的KMnO4溶液滴定至终点时消耗KMnO4溶液28.00mL。已知:5H2C2O4+2
 +6H+=2Mn2++10CO2↑+8H2O,样品中K3[Fe(C2O4)3]·3H2O的质量分数为
+6H+=2Mn2++10CO2↑+8H2O,样品中K3[Fe(C2O4)3]·3H2O的质量分数为
您最近一年使用:0次
2022-05-03更新
|
1074次组卷
|
2卷引用:四川省宜宾市第四中学校2023-2024学年高三上学期第二次月考理综化学试题
9-10高三·四川成都·阶段练习
2 . A、B、C、D、E五种短周期元素,原子序数依次增大,其中只有C为金属元素。A、C原子序数之和等于E的原子序数,D与B同主族且D原子序数是B原子序数的2倍。AB2和DB2溶于水得到酸性溶液,C2D溶于水得到碱性溶液。
(1)E元素在周期表中的位置为_____ ;工业上制取C单质的化学方程式为______ 。
(2)A的最低负价氢化物的空间构型为____ ;C、D、E的简单离子的离子半径由大到小的顺序是_____ (用离子符号表示)。
(3)在低温下,将E的单质通入饱和NaHCO3溶液中,反应后得到一种微绿色气体E2B、CE和另外一种无色气体。则该反应中E2B、CE这两种产物的物质的量之比n(E2B):n(CE)=_______ 。已知E2B溶于水生成一种具有漂白性的弱酸,该弱酸分子的结构式为__________ 。
(4)化合物C2 D3中,各原子(或离子)最外层均达到8电子稳定结构,则C2D3的电子式为_________ ,该化合物的水溶液在空气中久置后变质,生成一种单质,所得溶液呈强碱性,用化学方程式表示这一变化过程__________ 。
(1)E元素在周期表中的位置为
(2)A的最低负价氢化物的空间构型为
(3)在低温下,将E的单质通入饱和NaHCO3溶液中,反应后得到一种微绿色气体E2B、CE和另外一种无色气体。则该反应中E2B、CE这两种产物的物质的量之比n(E2B):n(CE)=
(4)化合物C2 D3中,各原子(或离子)最外层均达到8电子稳定结构,则C2D3的电子式为
您最近一年使用:0次



