1 . 乙烯是石油裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。请回答:
(1)乙烯的电子式为______ ,结构简式为______ 。
(2)下列可以鉴别甲烷和乙烯的试剂为______(填选项字母)。
(3)已知:2CH3CHO+O2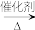 2CH3COOH,以乙烯为主要原料合成乙酸,合成路线如图所示:
2CH3COOH,以乙烯为主要原料合成乙酸,合成路线如图所示:

反应③的反应类型为______ 反应,反应①的化学方程式为:_____ 。反应②的化学方程式为:_____ 。
(4)以乙烯为原料生产塑料的化学方程式:_____ 。
(1)乙烯的电子式为
(2)下列可以鉴别甲烷和乙烯的试剂为______(填选项字母)。
| A.稀硫酸 | B.溴的四氯化碳溶液 |
| C.水 | D.酸性高锰酸钾溶液 |
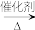 2CH3COOH,以乙烯为主要原料合成乙酸,合成路线如图所示:
2CH3COOH,以乙烯为主要原料合成乙酸,合成路线如图所示:
反应③的反应类型为
(4)以乙烯为原料生产塑料的化学方程式:
您最近一年使用:0次
2022-12-15更新
|
164次组卷
|
2卷引用:云南省昆明北大博雅实验中学2020-2021学年高一下学期期中考试化学试题
名校
解题方法
2 . 对下列化学用语的理解和描述均正确的是
| A.离子方程式H++OH-=H2O可表示所有强酸与强碱溶液的反应 |
B.原子结构示意图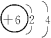 可以表示12C,也可以表示14C 可以表示12C,也可以表示14C |
C.氯离子的电子式: |
| D.氯气溶于水:Cl2+H2O=2H++Cl-+ClO- |
您最近一年使用:0次
2022-12-14更新
|
203次组卷
|
2卷引用:上海市松江二中2021-2022学年高一上学期期末考试化学试题
名校
解题方法
3 . 短周期元素A、B、C、D、E、F的原子序数依次增大。A原子是元素周期表中原子半径最小的原子;B可以与A形成常温下常见的液态物质;C原子的最外层电子数为比最内层电子数少1;D单质在空气中点燃发出耀眼的白光;1molE最多可失去3mol电子,F是第3周期非金属性最强的元素。
(1)A、B形成的具有强氧化性的18电子的物质的电子式为:_______ ;含有化学键的类型:_______ 和_______ 。
(2)C、D最高价氧化物的水化物的碱性:_______ >_______ (填化学式)。
(3)B、C形成的简单离子半径大小_______ >_______ (填具体离子符号)。
(4)E的最高价氧化物的水化物与C的最高价氧化物的水化物在溶液中反应的化学方程式为_______
(5)用电子式表示出化合物CF的形成过程:_______ 。
(1)A、B形成的具有强氧化性的18电子的物质的电子式为:
(2)C、D最高价氧化物的水化物的碱性:
(3)B、C形成的简单离子半径大小
(4)E的最高价氧化物的水化物与C的最高价氧化物的水化物在溶液中反应的化学方程式为
(5)用电子式表示出化合物CF的形成过程:
您最近一年使用:0次
2022-12-14更新
|
83次组卷
|
2卷引用:内蒙古赤峰市松山区第二地质中学2020-2021学年高一下学期第二次阶段检测化学试题
解题方法
4 . 用电子式表示下列物质的结构:
(1)NH4Cl_______ ;
(2)Na2O_______ ;
(3)CO2_______ ;
(4)H2S_______ ;
(5)Na2O2_______ ;
(6)MgCl2_______ ;
(7)上述物质中仅含离子键的是_______ ,仅含共价键的是_______ ,既有离子键又有共价键的是_______ 。(填相应序号)
(1)NH4Cl
(2)Na2O
(3)CO2
(4)H2S
(5)Na2O2
(6)MgCl2
(7)上述物质中仅含离子键的是
您最近一年使用:0次
5 . 已知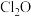 是一种棕黄色的气体,其沸点为
是一种棕黄色的气体,其沸点为 ,易爆炸,室温时开始缓慢分解。一种制备
,易爆炸,室温时开始缓慢分解。一种制备 和次氯酸的实验装置如下:
和次氯酸的实验装置如下:
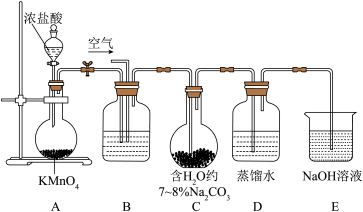
回答下列问题:
(1)写出次氯酸的电子式:_______ 。
(2)装置A烧瓶中发生反应的离子方程式为_______ ( 被还原为
被还原为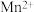 )
)
(3)装置B中盛放的溶液可以是_______ ;为得到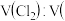 空气
空气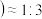 的混合气体,可采用的方法是
的混合气体,可采用的方法是_______ 。
(4)装置C需控制温度在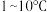 反应,可采取的措施是
反应,可采取的措施是_______ ;烧瓶中 与
与 反应产生
反应产生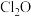 的化学方程式为
的化学方程式为_______ ;用空气稀释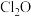 的目的是
的目的是_______ 。
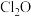 是一种棕黄色的气体,其沸点为
是一种棕黄色的气体,其沸点为 ,易爆炸,室温时开始缓慢分解。一种制备
,易爆炸,室温时开始缓慢分解。一种制备 和次氯酸的实验装置如下:
和次氯酸的实验装置如下:
回答下列问题:
(1)写出次氯酸的电子式:
(2)装置A烧瓶中发生反应的离子方程式为
 被还原为
被还原为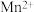 )
)(3)装置B中盛放的溶液可以是
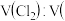 空气
空气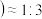 的混合气体,可采用的方法是
的混合气体,可采用的方法是(4)装置C需控制温度在
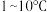 反应,可采取的措施是
反应,可采取的措施是 与
与 反应产生
反应产生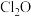 的化学方程式为
的化学方程式为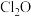 的目的是
的目的是
您最近一年使用:0次
解题方法
6 . 甲图是部分短周期元素的常见化合价与原子序数的关系图:

请回答下列问题:
(1) 元素在周期表中的位置为
元素在周期表中的位置为_______ ,D和G的简单氢化物中沸点高的是_______ (写化学式),A和E形成的化合物的电子式为_______ 。
(2) 、E、G、H的简单离子半径由大到小的顺序为
、E、G、H的简单离子半径由大到小的顺序为_______ 。(用化学式表示)
(3) 的最高价氧化物对应的水化物的浓溶液不稳定,受热可分解,产物之一是H的单质,且当有28mol电子转移时,常温共产生9mol气体,写出该反应的化学方程式
的最高价氧化物对应的水化物的浓溶液不稳定,受热可分解,产物之一是H的单质,且当有28mol电子转移时,常温共产生9mol气体,写出该反应的化学方程式_______ 。
(4)由上述元素中的几种组成a、b、c各物质,某同学设计实验用乙图装置证明元素B、C、F的非金属性强弱(其中溶液b和溶液c均为足量)。

①溶液a和b分别为_______ (填化学式)。
②溶液c中的离子方程式为_______ 。

请回答下列问题:
(1)
 元素在周期表中的位置为
元素在周期表中的位置为(2)
 、E、G、H的简单离子半径由大到小的顺序为
、E、G、H的简单离子半径由大到小的顺序为(3)
 的最高价氧化物对应的水化物的浓溶液不稳定,受热可分解,产物之一是H的单质,且当有28mol电子转移时,常温共产生9mol气体,写出该反应的化学方程式
的最高价氧化物对应的水化物的浓溶液不稳定,受热可分解,产物之一是H的单质,且当有28mol电子转移时,常温共产生9mol气体,写出该反应的化学方程式(4)由上述元素中的几种组成a、b、c各物质,某同学设计实验用乙图装置证明元素B、C、F的非金属性强弱(其中溶液b和溶液c均为足量)。

①溶液a和b分别为
②溶液c中的离子方程式为
您最近一年使用:0次
解题方法
7 . 学习有机化学,掌握有机物的组成、结构、命名和官能团性质是重中之重。
(1)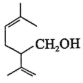 的分子式为
的分子式为______ ,所含官能团的名称为______ 。
(2)用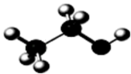 表示乙醇的分子结构,该模型表示乙醇分子的
表示乙醇的分子结构,该模型表示乙醇分子的________ (填“球棍模型”、“比例模型”或“键线式”);
(3)请根据官能团的不同对下列有机物进行分类,把正确答案序号填写在相应横线上。
①CH3CH2OH ②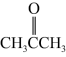 ③CH3CH2Br ④
③CH3CH2Br ④ ⑤
⑤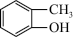 ⑥
⑥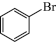 ⑦
⑦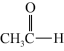 ⑧
⑧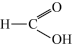 ⑨
⑨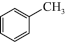 ⑩
⑩
芳香烃:_______ ;醇:_____ ;羧酸:__________ ; 酯:__________ 。
(4)当有机化合物分子中碳原子连有四个不同基团时称为手性碳原子,如A中星号“*”碳原子就是手性碳原子。
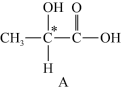
若使A失去手性,下列方法可行的是 。
(1)
 的分子式为
的分子式为(2)用
 表示乙醇的分子结构,该模型表示乙醇分子的
表示乙醇的分子结构,该模型表示乙醇分子的(3)请根据官能团的不同对下列有机物进行分类,把正确答案序号填写在相应横线上。
①CH3CH2OH ②
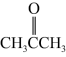 ③CH3CH2Br ④
③CH3CH2Br ④ ⑤
⑤ ⑥
⑥ ⑦
⑦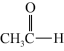 ⑧
⑧ ⑨
⑨ ⑩
⑩
芳香烃:
(4)当有机化合物分子中碳原子连有四个不同基团时称为手性碳原子,如A中星号“*”碳原子就是手性碳原子。

若使A失去手性,下列方法可行的是 。
| A.一定条件下和乙醇发生酯化反应 |
| B.一定条件下和乙酸发生酯化反应 |
| C.一定条件下发生催化氧化反应 |
| D.一定条件下发生消去反应 |
您最近一年使用:0次
解题方法
8 . 下列化学用语不正确 的是
A.羟基的电子式: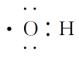 | B.乙烯的结构简式:CH2CH2 |
| C.乙酸乙酯的最简式:C2H4O | D.乙酸分子比例模型: |
您最近一年使用:0次
解题方法
9 . A、B、C、D四种物质之间有下图所示的转化关系。已知A是气体单质,C是红棕色气体。

回答下列问题:
(1)A的电子式:_______ ,C的化学式:_______ 。
(2)在上图D→B的过程中,D表现出强_______ (填“氧化性”或“还原性”)。
(3)写出C→D转化的化学方程式:_______ 。

回答下列问题:
(1)A的电子式:
(2)在上图D→B的过程中,D表现出强
(3)写出C→D转化的化学方程式:
您最近一年使用:0次
解题方法
10 . 反应8NH3+3Cl2=6NH4Cl+N2可用于氯气管道的检漏。下列表示相关微粒的化学用语正确的
A.中子数为20的氯原子: |
B.Cl-的结构示意图: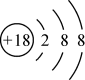 |
C.N2分子的电子式: |
D.NH3的球棍模型: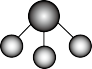 |
您最近一年使用:0次



