名校
解题方法
1 . 人类在金星大气中探测到 ,实验室制备
,实验室制备 的方法有:①
的方法有:①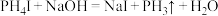 ;②
;② 。已知
。已知 是弱酸,其结构式为
是弱酸,其结构式为 。
。
下列说法不正确的是
 ,实验室制备
,实验室制备 的方法有:①
的方法有:①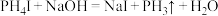 ;②
;② 。已知
。已知 是弱酸,其结构式为
是弱酸,其结构式为 。
。下列说法不正确的是
| A.反应①为非氧化还原反应 | B. 的结构示意图: 的结构示意图: |
C. 是三元酸 是三元酸 | D.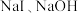 和 和 都是电解质 都是电解质 |
您最近一年使用:0次
2023-11-04更新
|
126次组卷
|
2卷引用:重庆市第一中学校2023-2024学年高一上学期定时练习化学试题
名校
解题方法
2 . 卤族元素相关物质在生产、生活中应用广泛。回答下列问题:
(1) 的离子结构示意图为
的离子结构示意图为______ 。
(2)卤素单质有着相似的化学性质,但同时也有差别。比如 与NaOH反应生成NaCl、NaClO和水,而
与NaOH反应生成NaCl、NaClO和水,而 与NaOH发生如下反应:
与NaOH发生如下反应: 。其中
。其中 的电子式为
的电子式为______ ,用电子式描述NaF的形成过程:______ 。
(3)根据卤族元素性质的相似性和递变性,推测元素砹(At)的单质为有色固体,HAt的稳定性______ (填“大于”或“小于”)HI的稳定性,AgAt______ (填“易”或“难”)溶于水。
(4)不同卤素原子之间以共价键相结合形成的化合物称为卤素互化物,如 等。它们与卤素单质性质相似。
等。它们与卤素单质性质相似。
① 与水反应的产物可能为
与水反应的产物可能为______ (填化学式)。
②下列说法不正确的是______ 。
A.HF、HCl、HBr的沸点依次升高
B. 沸点依次升高
沸点依次升高
C.已知离子半径大小会影响离子键的强弱,从而影响物质的熔点:若离子半径越大,离子键越弱。据此推测NaF、NaCl、NaBr熔点依次降低
D. (X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
(X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
(1)
 的离子结构示意图为
的离子结构示意图为(2)卤素单质有着相似的化学性质,但同时也有差别。比如
 与NaOH反应生成NaCl、NaClO和水,而
与NaOH反应生成NaCl、NaClO和水,而 与NaOH发生如下反应:
与NaOH发生如下反应: 。其中
。其中 的电子式为
的电子式为(3)根据卤族元素性质的相似性和递变性,推测元素砹(At)的单质为有色固体,HAt的稳定性
(4)不同卤素原子之间以共价键相结合形成的化合物称为卤素互化物,如
 等。它们与卤素单质性质相似。
等。它们与卤素单质性质相似。①
 与水反应的产物可能为
与水反应的产物可能为②下列说法不正确的是
A.HF、HCl、HBr的沸点依次升高
B.
 沸点依次升高
沸点依次升高C.已知离子半径大小会影响离子键的强弱,从而影响物质的熔点:若离子半径越大,离子键越弱。据此推测NaF、NaCl、NaBr熔点依次降低
D.
 (X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
(X代表F、Cl、Br)的酸性随着X的原子序数递增逐渐减弱
您最近一年使用:0次
2024-04-04更新
|
201次组卷
|
2卷引用:重庆市巴蜀中学校2023-2024学年高一下学期3月月考化学试题
3 . 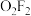 是目前已知的最强氧化剂之一,几乎能和所有物质发生剧烈反应。
是目前已知的最强氧化剂之一,几乎能和所有物质发生剧烈反应。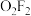 遇
遇 发生反应:
发生反应: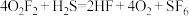 ,关于该反应中涉及到的物质,下列说法错误的是
,关于该反应中涉及到的物质,下列说法错误的是
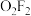 是目前已知的最强氧化剂之一,几乎能和所有物质发生剧烈反应。
是目前已知的最强氧化剂之一,几乎能和所有物质发生剧烈反应。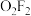 遇
遇 发生反应:
发生反应: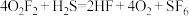 ,关于该反应中涉及到的物质,下列说法错误的是
,关于该反应中涉及到的物质,下列说法错误的是A.F的原子结构示意图: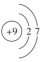 |
B. 的空间填充模型: 的空间填充模型: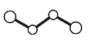 |
C. 的电子式: 的电子式: |
D. 的结构式: 的结构式: |
您最近一年使用:0次
2022-12-03更新
|
212次组卷
|
2卷引用:重庆市2023届高三上学期第四次质量检测化学试题
名校
4 . 碳铵分解的化学方程式为NH4HCO3 NH3↑ + CO2↑+H2O。下列说法不正确的是
NH3↑ + CO2↑+H2O。下列说法不正确的是
 NH3↑ + CO2↑+H2O。下列说法不正确的是
NH3↑ + CO2↑+H2O。下列说法不正确的是| A.NH4HCO3的结构中含有离子键 | B.NH3的电子式为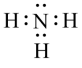 |
C.CO2的比例模型为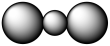 | D.H2O的结构式为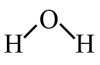 |
您最近一年使用:0次
名校
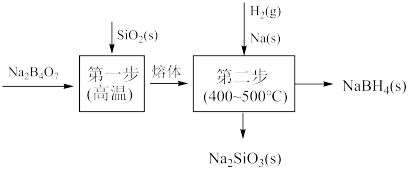
5 . 硼氢化钠(NaBH4)具有强还原性,在工业生产上应用广泛。工业上制备NaBH4的方法之一如下。下列说法错误的是

A.NaBH4的电子式为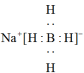 |
| B.将SiO2粉碎能增大得到熔体的速率 |
| C.整个过程中氧化剂与还原剂的物质的量之比为3∶2 |
| D.该工艺过程中无污染性物质产生,符合绿色化学理念 |
您最近一年使用:0次



