1 . 制备 (S呈+2价)的化学方程式为
(S呈+2价)的化学方程式为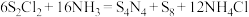 。下列说法正确的是
。下列说法正确的是
 (S呈+2价)的化学方程式为
(S呈+2价)的化学方程式为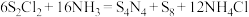 。下列说法正确的是
。下列说法正确的是A.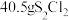 参与反应,转移电子的数目为 参与反应,转移电子的数目为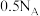 |
B.25℃、101kPa条件下,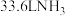 的分子数为 的分子数为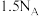 |
C.由 ( (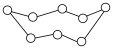 )与 )与 ( ( )组成的混合物中所含共价键的数目为 )组成的混合物中所含共价键的数目为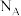 |
D.常温下,1LpH为5的 溶液中,由水电离出的 溶液中,由水电离出的 数目为 数目为 |
您最近一年使用:0次
7日内更新
|
157次组卷
|
3卷引用:2024届河北省沧州市部分高中高三下学期二模化学试题
名校
2 . 氢化钠可用作野外生氢剂: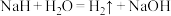 。
。 为阿伏加德罗常数的值,若生成4.0g NaOH,下列叙述正确的是
为阿伏加德罗常数的值,若生成4.0g NaOH,下列叙述正确的是
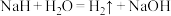 。
。 为阿伏加德罗常数的值,若生成4.0g NaOH,下列叙述正确的是
为阿伏加德罗常数的值,若生成4.0g NaOH,下列叙述正确的是A.转移的电子数为 | B.消耗的 分子中含有孤电子对数为 分子中含有孤电子对数为 |
| C.生成氢气的体积为2.24L | D.该反应为熵减过程 |
您最近一年使用:0次
名校
3 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,11.2LCH3CHO中含有π键的数目为0.5NA |
| B.1mol基态Ni原子中含有未成对电子数为3NA |
| C.100mL8mol/L浓硝酸与6.4g的Cu完全反应转移的电子数目为0.2NA |
| D.工业合成氨的反应通入14gN2和14gH2充分反应后生成NH分子的数目为NA |
您最近一年使用:0次
4 .  为阿伏加德罗常数的值。我国化学家侯德榜改进国外的纯碱生产工艺,提高了原料利用率。其主要原理为
为阿伏加德罗常数的值。我国化学家侯德榜改进国外的纯碱生产工艺,提高了原料利用率。其主要原理为 。下列说法正确的是
。下列说法正确的是
 为阿伏加德罗常数的值。我国化学家侯德榜改进国外的纯碱生产工艺,提高了原料利用率。其主要原理为
为阿伏加德罗常数的值。我国化学家侯德榜改进国外的纯碱生产工艺,提高了原料利用率。其主要原理为 。下列说法正确的是
。下列说法正确的是A.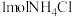 完全分解,产生气体的分子数目为 完全分解,产生气体的分子数目为 |
B.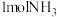 分子所含价层电子对的数目为3 分子所含价层电子对的数目为3 |
C.含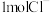 的 的 和 和 的混合物中,质子总数为28 的混合物中,质子总数为28 |
D.标准状况下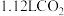 含 含 键的数目为0.2 键的数目为0.2 |
您最近一年使用:0次
5 . 设 为阿伏加德罗常数的值,下列说法中正确的是
为阿伏加德罗常数的值,下列说法中正确的是
 为阿伏加德罗常数的值,下列说法中正确的是
为阿伏加德罗常数的值,下列说法中正确的是A.标准状况下,22.4L正丙醇( )分子中含有 )分子中含有 的数目为8 的数目为8 |
B.24g质量分数为25%的甲醛水溶液中含有氢原子数目为2.4 |
C.pH=1的 溶液与足量的Zn反应产生的氢气分子数目为0.05 溶液与足量的Zn反应产生的氢气分子数目为0.05 |
D.0.1mol  与0.1mol 与0.1mol  反应时,转移电子的数目为0.3 反应时,转移电子的数目为0.3 |
您最近一年使用:0次
2024-05-18更新
|
730次组卷
|
3卷引用:河北省重点高中2023-2024学年高三下学期5月高考模拟化学试题(二)
名校
解题方法
6 . NO是大气污染物之一,有一种治理NO的方法,是在400℃左右、催化剂存在的条件下,使NH3与NO反应生成无污染的N2和H2O。设NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,1.7gNH3中,所含的σ键总数为0.3NA |
| B.通常状况下2.24LH2O分子中,所含的中子总数为0.3NA |
| C.等物质的量的NH3和NO中所含的氮原子数均为NA |
| D.0.2molH2O分子中所含的电子总数为1.6NA |
您最近一年使用:0次
7 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.22.4LNO2含有的原子总数为3NA |
| B.常温下,将2.7g铝片投入浓硝酸中,转移的电子总数为0.3NA |
| C.5.6g铁粉与足量稀硫酸反应,转移的电子总数为0.3NA |
| D.11.2gN2含有的原子总数为0.8NA |
您最近一年使用:0次
名校
8 . 氢元素有氕(H)、氘(D)、氚(T)三种核素,NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,2.24LT2含有的中子数为0.4NA |
| B.1gD2O中,中心原子上的孤电子对数为0.2 NA |
| C.1L0.1mol/LFeCl3溶液中含有的Fe3+数为0.1NA |
| D.电解水(H2O)生成0.2gH2,外电路通过的电子数为0.1NA |
您最近一年使用:0次
9 . 用 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是
 表示阿伏加德罗常数,下列说法正确的是
表示阿伏加德罗常数,下列说法正确的是A.电解精炼Cu时阳极减少32g时,转移电子数一定为 |
B.密闭容器中,2mol 和1mol 和1mol 催化反应后分子,总数大于 催化反应后分子,总数大于 |
C.0℃,pH=1 溶液中含有的氢离子数目小于 溶液中含有的氢离子数目小于 |
D.标准状况下,22.4L HCl溶于水后溶液中有 个HCl分子 个HCl分子 |
您最近一年使用:0次
10 . 用 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是
 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是A. 苯中含有的分子数目为 苯中含有的分子数目为 |
B. 与 与 反应生成 反应生成 的数目小于 的数目小于 |
C. 溶液中含有的 溶液中含有的 数目为 数目为 |
D.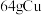 与足量浓硝酸反应时得到电子数目为 与足量浓硝酸反应时得到电子数目为 |
您最近一年使用:0次



