名校
1 . 已知22℃下水的蒸气压为2.7kPa,在该温度和100.0kPa下,用排水集气法收集到H2(g)0.05mol,则干燥后H2(g)的体积应为
| A.1.26L | B.2.45L | C.12.6L | D.24.5L |
您最近一年使用:0次
解题方法
2 . 填空题。
(1)有下列七种物质:①石灰水②KOH③稀硫酸④液氯⑤蔗糖⑥CuSO4•5H2O⑦SO2。其中属于氧化物的是_______ (填序号,下同);属于混合物的是_______ ;属于电解质的是_______ ;属于非电解质的是_______ 。
(2)3.4克NH3中所含氢原子数目与标准状况下约______ LH2S所含氢原子数目相等。
(3)15.6gNa2X中含有Na+0.4mol,则X的摩尔质量为_______ 。
(4)标准状态下,672mL某气体质量为1.92g,该气体的摩尔质量为_______ 。
(5)同温同压下,同质量的甲烷(CH4)和氨气物质的量之比为_______ ;氢原子总数之比为_______ ;体积之比为_______ ;密度之比为_______ 。
(1)有下列七种物质:①石灰水②KOH③稀硫酸④液氯⑤蔗糖⑥CuSO4•5H2O⑦SO2。其中属于氧化物的是
(2)3.4克NH3中所含氢原子数目与标准状况下约
(3)15.6gNa2X中含有Na+0.4mol,则X的摩尔质量为
(4)标准状态下,672mL某气体质量为1.92g,该气体的摩尔质量为
(5)同温同压下,同质量的甲烷(CH4)和氨气物质的量之比为
您最近一年使用:0次
3 . 如图所示,该装置是某医院内给病人输液的部分装置示意图,乙瓶内液体不断通过Q管输入病人体内,刚开始输液时,甲、乙两瓶内药液量相等,液面相平。过了一会儿(此时两个输液瓶内还有大量的溶液),观察两个输液瓶时会发现


| A.甲瓶中的液面高 | B.乙瓶中的液面高 |
| C.甲、乙两瓶中的液面一样高 | D.以上三种情况均有可能 |
您最近一年使用:0次
23-24高一下·全国·课后作业
名校
4 . 碳酸氢铵 常用作膨松剂、缓冲剂。一种制备碳酸氢铵的流程如图所示,已知氨气极易溶于水,“合成”过程中发生了化合反应。下列说法错误的是
常用作膨松剂、缓冲剂。一种制备碳酸氢铵的流程如图所示,已知氨气极易溶于水,“合成”过程中发生了化合反应。下列说法错误的是
 常用作膨松剂、缓冲剂。一种制备碳酸氢铵的流程如图所示,已知氨气极易溶于水,“合成”过程中发生了化合反应。下列说法错误的是
常用作膨松剂、缓冲剂。一种制备碳酸氢铵的流程如图所示,已知氨气极易溶于水,“合成”过程中发生了化合反应。下列说法错误的是
| A.“造气”时,需要控制好煤与空气的用量,减少CO的生成 |
| B.常温常压下,等体积的N2、H2、NH3、CO2所含分子数均相同 |
| C.为了获得更多的NH4HCO3,可以先向水中通入足量CO2,再通入足量NH3 |
| D.N2、H2合成NH3时,每转移3mole-,生成17gNH3 |
您最近一年使用:0次
2024-03-01更新
|
457次组卷
|
7卷引用:5.2.2氨和铵盐课后作业提高篇
名校
解题方法
5 . N4分子是一种不稳定的多氮分子,N4分解后产生无毒的氮气并释放出大量能量,可应用于制造推进剂或炸药,N4分子结构如图所示。下列关于N4和N2的说法错误的是
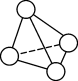

| A.1 mol N4分子含有6 mol N-N键 |
| B.两者互为同素异形体,物理性质不同,化学性质相似 |
| C.相同物质的量的N4和N2所含分子数相等 |
| D.N4是一种新型化合物 |
您最近一年使用:0次
名校
6 . A为一个恒温恒压的容器(如图所示,a是可以自由移动的活塞),常温常压下,向A中充入CO和 的混合气体使A体积等于6L,充分燃烧,恢复常温常压,A的体积为5L,下列说法不正确的是
的混合气体使A体积等于6L,充分燃烧,恢复常温常压,A的体积为5L,下列说法不正确的是

 的混合气体使A体积等于6L,充分燃烧,恢复常温常压,A的体积为5L,下列说法不正确的是
的混合气体使A体积等于6L,充分燃烧,恢复常温常压,A的体积为5L,下列说法不正确的是
A.反应前后气体的总物质的量之比为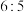 |
B.反应前CO和 的物质的量之比可能为 的物质的量之比可能为 |
C.反应前CO和 的物质的量之比可能为 的物质的量之比可能为 |
D.反应后 的体积为2L 的体积为2L |
您最近一年使用:0次
解题方法
7 . 一种常见酸的分子结构式如图所示。元素W、X、Y原子序数依次增大,且X、Y均位于W的下一周期。下列说法中错误的是


| A.根据元素周期律,最高正化合价:Y>X>W |
| B.W、Y原子可以形成既含极性键又含非极性键分子 |
| C.X、Y分别与W均可以形成10电子分子 |
| D.同温同压下,等体积的W2和Y2气体含有相同的分子数 |
您最近一年使用:0次
解题方法
8 . 下列有关描述正确的是
A.已知酸性 , 所以元素非金属性 , 所以元素非金属性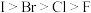 |
B.考古学上常用来鉴定鉴定文物的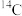 核内中子数为6 核内中子数为6 |
C.在相同的温度和压强下,等体积的 和 和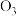 两种气体含有相同的分子数 两种气体含有相同的分子数 |
D.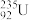 和 和 是中子数不同质子数相同的同种核素 是中子数不同质子数相同的同种核素 |
您最近一年使用:0次
名校
9 . 向蔗糖(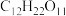 )中滴入98%的浓硫酸,蔗糖会变成疏松的“炭块”,同时产生
)中滴入98%的浓硫酸,蔗糖会变成疏松的“炭块”,同时产生 ,
, ;
; 可用酸性高锰酸钾溶液吸收。请回答下列问题:
可用酸性高锰酸钾溶液吸收。请回答下列问题:
(1)蔗糖的摩尔质量为______ 。17.1 g 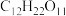 的物质的量为
的物质的量为______ 。
(2)500℃时,34.2 g蔗糖完全燃烧,产生两种气体的体积之比为______ ,其中产生 的体积(折算成标准状况下)为
的体积(折算成标准状况下)为______ L。
(3)质量分数为98%、密度为1.84 g⋅cm 的浓硫酸的物质的量浓度为
的浓硫酸的物质的量浓度为______ mol·L ;酸性高锰酸钾溶液需要用浓度为3 mol⋅L
;酸性高锰酸钾溶液需要用浓度为3 mol⋅L 的硫酸酸化,则实验室配制50 mL该浓度的硫酸需质量分数为98%的浓硫酸
的硫酸酸化,则实验室配制50 mL该浓度的硫酸需质量分数为98%的浓硫酸______ mL,需要用到的定量仪器有______ 。
(4) 被酸性高锰酸钾溶液吸收发生反应的离子方程式为
被酸性高锰酸钾溶液吸收发生反应的离子方程式为______ 。
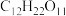 )中滴入98%的浓硫酸,蔗糖会变成疏松的“炭块”,同时产生
)中滴入98%的浓硫酸,蔗糖会变成疏松的“炭块”,同时产生 ,
, ;
; 可用酸性高锰酸钾溶液吸收。请回答下列问题:
可用酸性高锰酸钾溶液吸收。请回答下列问题:(1)蔗糖的摩尔质量为
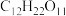 的物质的量为
的物质的量为(2)500℃时,34.2 g蔗糖完全燃烧,产生两种气体的体积之比为
 的体积(折算成标准状况下)为
的体积(折算成标准状况下)为(3)质量分数为98%、密度为1.84 g⋅cm
 的浓硫酸的物质的量浓度为
的浓硫酸的物质的量浓度为 ;酸性高锰酸钾溶液需要用浓度为3 mol⋅L
;酸性高锰酸钾溶液需要用浓度为3 mol⋅L 的硫酸酸化,则实验室配制50 mL该浓度的硫酸需质量分数为98%的浓硫酸
的硫酸酸化,则实验室配制50 mL该浓度的硫酸需质量分数为98%的浓硫酸(4)
 被酸性高锰酸钾溶液吸收发生反应的离子方程式为
被酸性高锰酸钾溶液吸收发生反应的离子方程式为
您最近一年使用:0次
10 . 请回答下列问题:
(1)一定条件下,下列物质可以通过化合反应制得的有___________ (填序号)。
①小苏打 ②硫酸铝 ③氯化亚铁 ④磁性氧化铁
(2)同温同压下,等质量的CO气体和CO2气体的体积比为___________ 。
(3)某实验过程中需要用1.0mol/L H2SO4溶液配制0.1mol/L H2SO4溶液475mL,配制过程中需要用到下列仪器中的___________ (填选项),还缺少的玻璃仪器有量筒、玻璃棒、___________ 。
A.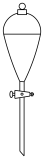 B.
B.  C.
C. 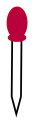 D.
D.
(4)钢铁烤蓝是在钢铁表面形成一层一定厚度和强度的致密氧化膜。古代铁匠常用红热的铁浸入水中形成烤蓝,体现该原理的化学方程式为___________ 。
(5)工业上将Cl2通入冷的石灰乳中制取漂白粉,写出反应的化学方程式___________ 。
(1)一定条件下,下列物质可以通过化合反应制得的有
①小苏打 ②硫酸铝 ③氯化亚铁 ④磁性氧化铁
(2)同温同压下,等质量的CO气体和CO2气体的体积比为
(3)某实验过程中需要用1.0mol/L H2SO4溶液配制0.1mol/L H2SO4溶液475mL,配制过程中需要用到下列仪器中的
A.
 B.
B.  C.
C. 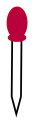 D.
D.
(4)钢铁烤蓝是在钢铁表面形成一层一定厚度和强度的致密氧化膜。古代铁匠常用红热的铁浸入水中形成烤蓝,体现该原理的化学方程式为
(5)工业上将Cl2通入冷的石灰乳中制取漂白粉,写出反应的化学方程式
您最近一年使用:0次



