1 . 用 代表阿伏加德罗常数的数值。下列说法正确的是
代表阿伏加德罗常数的数值。下列说法正确的是
 代表阿伏加德罗常数的数值。下列说法正确的是
代表阿伏加德罗常数的数值。下列说法正确的是A.1mol  含氧原子数为 含氧原子数为 |
B.14g  中含有的分子数为0.5 中含有的分子数为0.5 |
C.标准状况下,2.24L  所含分子数为0.1 所含分子数为0.1 |
D.1 的 的 的溶液中,所含的 的溶液中,所含的 个数为2 个数为2 |
您最近一年使用:0次
2024-03-29更新
|
98次组卷
|
2卷引用:2023年6月福建省普通高中学业水平合格性考试化学试题
名校
2 . 实验室需用 硫酸铜溶液,下列有关该溶液的配制说法正确的是
硫酸铜溶液,下列有关该溶液的配制说法正确的是
 硫酸铜溶液,下列有关该溶液的配制说法正确的是
硫酸铜溶液,下列有关该溶液的配制说法正确的是A.用托盘天平称取胆矾 |
| B.实验中必须用到的玻璃仪器为:烧杯、量筒、容量瓶、玻璃棒 |
| C.定容时仰视容量瓶的刻度线,会造成所配溶液物质的量浓度偏高 |
| D.定容摇匀后发现液面低于刻度线,应再滴加蒸馏水至刻度线 |
您最近一年使用:0次
2024-02-10更新
|
265次组卷
|
2卷引用:云南省师范大学附属中学2023-2024学年高一上学期 期末化学试卷
3 . 下列说法中,正确的是
A.标准状况下, 的质量约为 的质量约为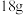 |
B.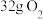 和 和 的混合气体中含有 的混合气体中含有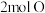 |
C.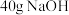 固体溶解在 固体溶解在 水中,所得溶液中溶质的物质的量浓度为 水中,所得溶液中溶质的物质的量浓度为 |
D.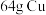 与含 与含 的浓硫酸在加热条件下充分反应,生成 的浓硫酸在加热条件下充分反应,生成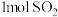 |
您最近一年使用:0次
解题方法
4 . 下列溶液中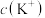 与10mL3
与10mL3 KCl溶液中
KCl溶液中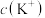 相等的是
相等的是
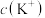 与10mL3
与10mL3 KCl溶液中
KCl溶液中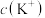 相等的是
相等的是A.15mL2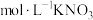 溶液 溶液 | B.20mL0.5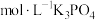 溶液 溶液 |
C.10mL1.5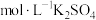 溶液 溶液 | D.15mL1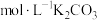 溶液 溶液 |
您最近一年使用:0次
5 .  溶液可以将池塘淤泥里的
溶液可以将池塘淤泥里的 氧化得到无色无味的气体从而起到除臭的作用,0.1mol
氧化得到无色无味的气体从而起到除臭的作用,0.1mol 可以反应标况下的氨气
可以反应标况下的氨气___________ L,为研究这个反应,某同学配制一定物质的量浓度的氨水,将标况下400体积的气通入1体积水中,理论上可以得到___________ mol/L密度为0.95g/mL的氨水。
 溶液可以将池塘淤泥里的
溶液可以将池塘淤泥里的 氧化得到无色无味的气体从而起到除臭的作用,0.1mol
氧化得到无色无味的气体从而起到除臭的作用,0.1mol 可以反应标况下的氨气
可以反应标况下的氨气
您最近一年使用:0次
解题方法
6 . 从1L NaOH溶液取出100mL,若将取出的这100mL NaOH溶液加水稀释至500mL,所得溶液中溶质的物质的量浓度是
NaOH溶液取出100mL,若将取出的这100mL NaOH溶液加水稀释至500mL,所得溶液中溶质的物质的量浓度是______  ?含NaOH的质量
?含NaOH的质量______ 克?
 NaOH溶液取出100mL,若将取出的这100mL NaOH溶液加水稀释至500mL,所得溶液中溶质的物质的量浓度是
NaOH溶液取出100mL,若将取出的这100mL NaOH溶液加水稀释至500mL,所得溶液中溶质的物质的量浓度是 ?含NaOH的质量
?含NaOH的质量
您最近一年使用:0次
7 . 设 表示阿伏加德罗常数,下列叙述中正确的是
表示阿伏加德罗常数,下列叙述中正确的是
 表示阿伏加德罗常数,下列叙述中正确的是
表示阿伏加德罗常数,下列叙述中正确的是A.常温常压下,11.2L氧气所含的原子数为 |
B.1.8g的 中含有的中子总数为 中含有的中子总数为 |
C.物质的量浓度为1mol/L的 溶液中,含有 溶液中,含有 个数为2 个数为2 |
D.常温常压下,46g  和 和 的混合气体中原子总数为3 的混合气体中原子总数为3 |
您最近一年使用:0次
8 . 下列说法正确的是
A.0.5mol  所占体积为11.2L 所占体积为11.2L |
B.标准状况下,1mol 的体积约为22.4L 的体积约为22.4L |
C.标准状况下,14gCO与 的混合气体的体积约为11.2L 的混合气体的体积约为11.2L |
| D.22.4L HCl气体溶于水配成1L溶液,浓度为1 mol/L |
您最近一年使用:0次
9 .  为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.标准状况下, 完全反应,转移电子数目一定为 完全反应,转移电子数目一定为 |
B.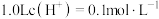 的 的 溶液中 溶液中 的数目为 的数目为 |
C.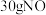 与 与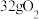 混合后所含原子总数小于 混合后所含原子总数小于 |
D.若核反应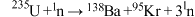 ( (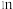 为中子)体系内中子增加 为中子)体系内中子增加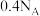 ,则消耗 ,则消耗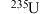 质量为 质量为 |
您最近一年使用:0次
解题方法
10 . 如图是某学校实验室从化学试剂商店买回来的氢氧化钠试剂标签上的部分内容。某同学从该试剂瓶中取出24.0 g固体,配成1 L溶液,请计算:
(1)所得氢氧化钠溶液的物质的量浓度为___________ 。
(2)从所得氢氧化钠溶液中取出200 mL于一烧杯中,投入2.7 g的金属铝,产生的气体在标准状况下的体积为___________ 。(写出解答步骤)
| 氢氧化钠 化学纯(CP) 500 g 品名:氢氧化钠 化学式:NaOH 相对分子质量:40 |
(2)从所得氢氧化钠溶液中取出200 mL于一烧杯中,投入2.7 g的金属铝,产生的气体在标准状况下的体积为
您最近一年使用:0次



