1 . 使用硫酸亚铁铵晶体[(NH4)2Fe(SO4)2·6H2O]滴定法可以测定青铜中铬元素的含量。实验步骤如下:
步骤1:称量硫酸亚铁铵晶[(NH4)2Fe(SO4)2·6H2O]溶于稀硫酸,加水稀释配成1000 mL0.0200 mol/L (NH4)2Fe(SO4)2标准溶液。
步骤2:称取1.00 g青铜样品于250 mL锥形瓶中,加入适量稀硝酸使其完全溶解,再加入适量过二硫酸铵[(NH4)2S2O8]溶液,加热煮沸,使样品中的铬元素完全转化为H2CrO4,冷却后加蒸馏水配制成250 mL溶液,摇匀。
步骤3:取25 mL上述溶液置于锥形瓶中,加入硫酸酸化,滴入4滴N-苯代邻氨基苯甲酸指示剂,用(NH4)2Fe(SO4)2标准溶液满淀至终点。重复上述操作3次。测得消耗(NH4)2Fe(SO4)2标准溶液的体积分别为18.90 mL、17.97 mL、18.03 mL。发生反应的离子方程式为:H2CrO4+Fe2++H+→Cr3++Fe3++H2O (未配平)
下列说法不正确的是
步骤1:称量硫酸亚铁铵晶[(NH4)2Fe(SO4)2·6H2O]溶于稀硫酸,加水稀释配成1000 mL0.0200 mol/L (NH4)2Fe(SO4)2标准溶液。
步骤2:称取1.00 g青铜样品于250 mL锥形瓶中,加入适量稀硝酸使其完全溶解,再加入适量过二硫酸铵[(NH4)2S2O8]溶液,加热煮沸,使样品中的铬元素完全转化为H2CrO4,冷却后加蒸馏水配制成250 mL溶液,摇匀。
步骤3:取25 mL上述溶液置于锥形瓶中,加入硫酸酸化,滴入4滴N-苯代邻氨基苯甲酸指示剂,用(NH4)2Fe(SO4)2标准溶液满淀至终点。重复上述操作3次。测得消耗(NH4)2Fe(SO4)2标准溶液的体积分别为18.90 mL、17.97 mL、18.03 mL。发生反应的离子方程式为:H2CrO4+Fe2++H+→Cr3++Fe3++H2O (未配平)
下列说法不正确的是
| A.在“步骤1”中,用到的玻璃仪器有1000 mL容量瓶、烧杯、玻璃棒、胶头滴管 |
B.在“步骤2”中,铜与硝酸反应的离子方程式为:3Cu+2 +8H+=3Cu2++2NO↑+4H2O +8H+=3Cu2++2NO↑+4H2O |
| C.青铜中铬元素的质量分数为6.344% |
| D.实验中,如果盛放(NH4)2Fe(SO4)2标准溶液的滴定管没有润洗,则测量结果将偏大 |
您最近一年使用:0次
解题方法
2 . 对于下列实验,能正确描述其反应的离子方程式的是
A.氯气溶于水: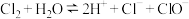 |
B.将水滴入盛有过氧化钠固体的试管中: |
C.用 溶液腐蚀覆铜板制作印刷电路板: 溶液腐蚀覆铜板制作印刷电路板: |
D.用酸性高锰酸钾溶液测定空气中 的含量: 的含量: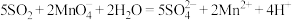 |
您最近一年使用:0次



