解题方法
1 . A、B、C、D四种可溶性盐,其阳离子分别是 、
、 、
、 、
、 中的某一种,阴离子分别是
中的某一种,阴离子分别是 、
、 、
、 、
、 中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有A盐溶液呈蓝色。②分别向4支试管中加入2mL稀盐酸,发现B盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有A盐溶液呈蓝色。②分别向4支试管中加入2mL稀盐酸,发现B盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
(1)根据上述实验事实,推断这几种盐的化学式分别为:B_______ ;C_______ ;D_______ 。
(2)按要求写出下列反应的方程式:
①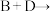
_______ 。(写离子方程式)
② 气体:
气体:_______ 。(写化学方程式)
 、
、 、
、 、
、 中的某一种,阴离子分别是
中的某一种,阴离子分别是 、
、 、
、 、
、 中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有A盐溶液呈蓝色。②分别向4支试管中加入2mL稀盐酸,发现B盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。
中的某一种。现做以下实验:①将四种盐各取少量,分别溶于盛有5mL蒸馏水的4支试管中,只有A盐溶液呈蓝色。②分别向4支试管中加入2mL稀盐酸,发现B盐溶液中产生白色沉淀,C盐溶液中有较多气泡产生,而D盐溶液无明显现象。(1)根据上述实验事实,推断这几种盐的化学式分别为:B
(2)按要求写出下列反应的方程式:
①
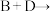
②
 气体:
气体:
您最近一年使用:0次
2022-05-21更新
|
480次组卷
|
2卷引用:湖南省岳阳市2020-2021学年高一上学期教学质量监测化学试题
名校
2 . 现有无色透明溶液,只含有下列离子中的若干种,每种离子的个数相等:Na+、NH 、Cl-、Fe3+、Ba2+、CO
、Cl-、Fe3+、Ba2+、CO 、SO
、SO 。现各取三份100mL溶液进行实验。
。现各取三份100mL溶液进行实验。
实验1:第一份加入足量AgNO3溶液有白色沉淀产生;
实验2:第二份加入足量NaOH溶液加热有气体放出,查资料知有NH 存在;
存在;
实验3:第三份加入足量BaCl2溶液后,有沉淀生成,加入足量盐酸后沉淀全部溶解.
(1)由实验1能否确定有Cl-存在?___ (填“能”或“否”),理由___ 。
(2)实验3中沉淀的化学式为___ ,该沉淀溶于盐酸的离子方程式为___ 。
(3)综合上述实验,能否确定有Na+存在?___ (填“能”或“否”)。请说明理由___ 。
 、Cl-、Fe3+、Ba2+、CO
、Cl-、Fe3+、Ba2+、CO 、SO
、SO 。现各取三份100mL溶液进行实验。
。现各取三份100mL溶液进行实验。实验1:第一份加入足量AgNO3溶液有白色沉淀产生;
实验2:第二份加入足量NaOH溶液加热有气体放出,查资料知有NH
 存在;
存在;实验3:第三份加入足量BaCl2溶液后,有沉淀生成,加入足量盐酸后沉淀全部溶解.
(1)由实验1能否确定有Cl-存在?
(2)实验3中沉淀的化学式为
(3)综合上述实验,能否确定有Na+存在?
您最近一年使用:0次
2021-11-16更新
|
940次组卷
|
4卷引用:湖南省长郡中学2021-2022学年高一上学期期中考试化学试题
23-24高一·全国·假期作业
名校
解题方法
3 . 对一份稀溶液做初步分析后发现,溶液无色、澄清,其中可能含有 、Na+、
、Na+、 、H+、
、H+、 、
、 、Cl-等离子中的若干种。然后又做了如下分析,以确定这些离子是否大量存在。
、Cl-等离子中的若干种。然后又做了如下分析,以确定这些离子是否大量存在。
①用pH试纸检测溶液的酸碱性,结果pH试纸显红色。
②取2 mL溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(1)溶液中一定存在的离子是________ ,一定不存在的离子是______________ 。
(2)上述实验操作中,有错误的操作是(填写序号)________ 。改正该错误的方法是(要做较详细的说明)_______________ 。
(3)到目前为止,仍不能肯定溶液中是否存在的离子是_______________ 。
 、Na+、
、Na+、 、H+、
、H+、 、
、 、Cl-等离子中的若干种。然后又做了如下分析,以确定这些离子是否大量存在。
、Cl-等离子中的若干种。然后又做了如下分析,以确定这些离子是否大量存在。①用pH试纸检测溶液的酸碱性,结果pH试纸显红色。
②取2 mL溶液用BaCl2溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(1)溶液中一定存在的离子是
(2)上述实验操作中,有错误的操作是(填写序号)
(3)到目前为止,仍不能肯定溶液中是否存在的离子是
您最近一年使用:0次
解题方法
4 . 一澄清溶液中可能含有的离子如表所示,为测定其含有的离子的种类,取该溶液进行实验:
实验①:用pH试纸检验,测得溶液呈强酸性。
实验②:取2 mL原溶液于试管中,加入少量CCl4及数滴新制氯水,经振荡,CCl4层呈紫红色。
实验③:取2 mL原溶液,逐渐向其中加入NaOH溶液,使溶液从酸性逐渐变为碱性,滴加过程中和滴加完毕后,均无沉淀产生。
实验④:另取部分上述实验③中的碱性溶液,向其中加入Na2CO3溶液,有白色沉淀生成。
已知:Br2、I2易溶于CCl4,且Br2的CCl4溶液呈橙红色,I2的CCl4溶液呈紫红色。
根据所学知识,回答下列问题:
(1)根据实验①,可排除___________ 的存在。(填离子符号,下同)
(2)根据实验②,可证明含有的离子为___________ ,写出氯水中的氯气与溶液中的离子反应的离子方程式___________ 。该反应中被还原的物质为___________ (填离子符号或化学式)。
(3)根据实验③,可确定肯定不含的离子为___________ 。
(4)根据实验④,可证明___________ 的存在,又排除___________ 的存在。
(5)综上所述,该溶液中上述离子尚不能确定是否存在的是___________ 。
| 阳离子 | K+ 、Mg2+ 、Ba2+ 、Al3+ 、H+ |
| 阴离子 | I- 、Br- 、CO 、SO 、SO 、OH- 、OH- |
实验②:取2 mL原溶液于试管中,加入少量CCl4及数滴新制氯水,经振荡,CCl4层呈紫红色。
实验③:取2 mL原溶液,逐渐向其中加入NaOH溶液,使溶液从酸性逐渐变为碱性,滴加过程中和滴加完毕后,均无沉淀产生。
实验④:另取部分上述实验③中的碱性溶液,向其中加入Na2CO3溶液,有白色沉淀生成。
已知:Br2、I2易溶于CCl4,且Br2的CCl4溶液呈橙红色,I2的CCl4溶液呈紫红色。
根据所学知识,回答下列问题:
(1)根据实验①,可排除
(2)根据实验②,可证明含有的离子为
(3)根据实验③,可确定肯定不含的离子为
(4)根据实验④,可证明
(5)综上所述,该溶液中上述离子尚不能确定是否存在的是
您最近一年使用:0次
5 . 某无色透明溶液中可能大量存在Na+、Mg2+、Cu2+、Ca2+、SO 、OH-、CO
、OH-、CO 和Cl-中的几种。回答下列问题:
和Cl-中的几种。回答下列问题:
(1)不做任何实验就可以肯定原溶液中不存在的离子是_______ 。
(2)取少量溶液滴入紫色石蕊溶液,溶液呈蓝色,原溶液中一定不存在的离子是_______ 。
(3)取少许溶液滴入BaCl2溶液,有白色沉淀产生,加入稀硝酸,白色沉淀完全溶解。原溶液一定不存在的离子是_______ ;写出白色沉淀溶解的离子方程式:_______ 。
(4)由上述过程可知,不能确定是否存在的离子是_______ ,若要确定该离子,应进行的实验为_______ (写出操作过程和实验现象)。
(5)取原溶液20 mL,逐滴加入0.2 mol∙L−1的Ca(OH)2溶液至恰好完全反应,这时消耗的Ca(OH)2溶液的体积为50 mL。用原溶液配制100 mL0.1 mol∙L−1的Na2CO3溶液,应取用的原溶液的体积为_______ mL。
 、OH-、CO
、OH-、CO 和Cl-中的几种。回答下列问题:
和Cl-中的几种。回答下列问题:(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量溶液滴入紫色石蕊溶液,溶液呈蓝色,原溶液中一定不存在的离子是
(3)取少许溶液滴入BaCl2溶液,有白色沉淀产生,加入稀硝酸,白色沉淀完全溶解。原溶液一定不存在的离子是
(4)由上述过程可知,不能确定是否存在的离子是
(5)取原溶液20 mL,逐滴加入0.2 mol∙L−1的Ca(OH)2溶液至恰好完全反应,这时消耗的Ca(OH)2溶液的体积为50 mL。用原溶液配制100 mL0.1 mol∙L−1的Na2CO3溶液,应取用的原溶液的体积为
您最近一年使用:0次
名校
解题方法
6 . 某无色透明溶液中可能大量存在 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
①向第一份溶液中滴入几滴酚酞试液,溶液变红;
②向第二份溶液中加入过量 溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
③向第三份溶液中先加入 溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
已知: 溶于稀硝酸。
溶于稀硝酸。
(1)写出实验②生成白色沉淀涉及的离子方程式:_______ 。
(2)实验③中的白色沉淀组成为_______ (写化学式)。
(3)根据上述实验现象可知,原溶液中一定存在的离子是_______ ,一定不存在的离子是_______ ,不能确定是否存在的离子是_______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:①向第一份溶液中滴入几滴酚酞试液,溶液变红;
②向第二份溶液中加入过量
 溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;③向第三份溶液中先加入
 溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。已知:
 溶于稀硝酸。
溶于稀硝酸。(1)写出实验②生成白色沉淀涉及的离子方程式:
(2)实验③中的白色沉淀组成为
(3)根据上述实验现象可知,原溶液中一定存在的离子是
您最近一年使用:0次
名校
解题方法
7 . A、B、C、D为四种可溶性的盐,它们包含的阳离子和阴离子分别为 、
、 、
、 、
、 和
和 、
、 、
、 、
、 (离子在物质中不能重复出现)。
(离子在物质中不能重复出现)。
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据实验事实可推断:
(1)化学式为:C_______ 、D_______ ;
(2)A与C反应的离子方程式_______ ;
(3)A溶液中阴离子的检验方法_______ 。
 、
、 、
、 、
、 和
和 、
、 、
、 、
、 (离子在物质中不能重复出现)。
(离子在物质中不能重复出现)。①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出。
根据实验事实可推断:
(1)化学式为:C
(2)A与C反应的离子方程式
(3)A溶液中阴离子的检验方法
您最近一年使用:0次
解题方法
8 . 某溶液的溶质可能由下列离子组成:Cl-、SO42-、CO32-、H+、 Ba2+、Na+,某同学进行了如下实验:
(1)向溶液中加入过量的BaCl2溶液,有白色沉淀产生,过滤;
(2)向(1)中滤液里加入AgNO3溶液,有白色沉淀产生;
(3)将(1)中的沉淀加入稀盐酸中,沉淀部分消失,有气体产生。
依据以上实验可以推断,原溶液中一定含有__________ ;一定没有____________________ ;可能含有__________________ 。
(1)向溶液中加入过量的BaCl2溶液,有白色沉淀产生,过滤;
(2)向(1)中滤液里加入AgNO3溶液,有白色沉淀产生;
(3)将(1)中的沉淀加入稀盐酸中,沉淀部分消失,有气体产生。
依据以上实验可以推断,原溶液中一定含有
您最近一年使用:0次
2020-01-30更新
|
544次组卷
|
5卷引用:苏教版高中化学必修1专题2《从海水中获得的化学物质》测试卷
名校
9 . 混合物的分离提纯在生产、生活中有着重要的意义。已知某工业废水中含有大量的 ,还可能含有较多的
,还可能含有较多的 、
、 、
、 、
、 ,以及部分污泥,通过下列流程可从该废水中回收
,以及部分污泥,通过下列流程可从该废水中回收 晶体及固体单质。已知氧化性:
晶体及固体单质。已知氧化性: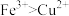 。
。

(1)不需任何实验就可以确定可能存在的离子中___________ (填离子符号)一定不存在。
(2)步骤1采用了___________ 操作。根据步骤2中得到固体混合物可以确定可能存在的离子中___________ (填离子符号)一定存在。
(3)通过实验___________ (填“能”或“不能”)确定是否存在 。
。 的存在对回收
的存在对回收 晶体的纯度
晶体的纯度___________ (填“有”或“无”)影响,理由是___________ 。
(4)步骤3中加入的试剂X为___________ ,发生反应的离子方程式为___________ 。
(5)步骤4中涉及的操作是:蒸发浓缩、___________ 、过滤、洗涤、烘干。
 ,还可能含有较多的
,还可能含有较多的 、
、 、
、 、
、 ,以及部分污泥,通过下列流程可从该废水中回收
,以及部分污泥,通过下列流程可从该废水中回收 晶体及固体单质。已知氧化性:
晶体及固体单质。已知氧化性: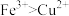 。
。
(1)不需任何实验就可以确定可能存在的离子中
(2)步骤1采用了
(3)通过实验
 。
。 的存在对回收
的存在对回收 晶体的纯度
晶体的纯度(4)步骤3中加入的试剂X为
(5)步骤4中涉及的操作是:蒸发浓缩、
您最近一年使用:0次
2021-11-07更新
|
359次组卷
|
3卷引用:四川省成都市蓉城名校联盟2021-2022学年高一上学期期中联考化学试题
解题方法
10 . 有一瓶澄清溶液,其中可能含有NH 、K+、Ba2+、Al3+、Fe3+、I-、NO
、K+、Ba2+、Al3+、Fe3+、I-、NO 、CO
、CO 、SO
、SO 和
和 。取该溶液进行以下实验:
。取该溶液进行以下实验:
①用pH试纸检验,溶液呈强酸性。
②取适量溶液,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色。
③另取适量溶液,逐滴加入NaOH溶液。
a.溶液从酸性变为中性;b.溶液逐渐产生沉淀;c.沉淀完全溶解;d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
④取适量③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题:
(1)由①可以排除__ 的存在。
(2)由②可以证明__ 的存在,同时排除__ 的存在,理由是__ 。
(3)由③可以证明__ 的存在。写出c、d所涉及的化学反应方程式,是离子反应的用离子方程式表示:c__ ;d__ 。
(4)由④可以证明__ 的存在,同时排除__ 的存在。
 、K+、Ba2+、Al3+、Fe3+、I-、NO
、K+、Ba2+、Al3+、Fe3+、I-、NO 、CO
、CO 、SO
、SO 和
和 。取该溶液进行以下实验:
。取该溶液进行以下实验:①用pH试纸检验,溶液呈强酸性。
②取适量溶液,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色。
③另取适量溶液,逐滴加入NaOH溶液。
a.溶液从酸性变为中性;b.溶液逐渐产生沉淀;c.沉淀完全溶解;d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
④取适量③得到的碱性溶液,加入Na2CO3溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题:
(1)由①可以排除
(2)由②可以证明
(3)由③可以证明
(4)由④可以证明
您最近一年使用:0次



