名校
解题方法
1 . 宏观辨识、微观探析和符号表征是体现化学学科特征的思维方式。某化学兴趣小组设计实验,探究离子反应及氧化还原反应的本质。
Ⅰ.离子反应
(1)向0.2mol·L-1Ba(OH)2溶液中滴入几滴酚酞溶液,装置如图。接通电源,向该溶液中滴入0.2molL-1H2SO4溶液。
①接通电源前,能说明Ba(OH)2在水中电离的实验现象为_______ 。
②随着H2SO4溶液的滴入,观察到烧杯中溶液红色逐渐褪去,产生白色沉淀,小灯泡亮度变暗,这些现象说明该反应的微观本质是Ba2+和OH-浓度降低,写出该反应的离子方程式_______ 。
(2)向0.2mol·L-1Ba(OH)2溶液中滴入0.1mol·L-1的盐酸,测定电导率的变化如图所示。
回答下列问题:_______ 。
②下列化学反应的离子方程式与Ba(OH)2溶液和稀盐酸反应相同的是_______ 。
A.Ba(OH)2溶液和稀硫酸 B.澄清石灰水和稀硝酸
C.NaOH溶液和NaHCO3溶液 D.浓氨水和浓盐酸
Ⅱ.氧化还原反应
(3)部分含硫物质如图所示,其中H2S和X是大气污染物。这些物质之间的相互转化为工业生产和处理环境问题提供了理论支持。 ,其中反应①的离子方程式是
,其中反应①的离子方程式是______________ ,若欲将X转化成“安全物质”Z,使其对环境的影响最小,需加入_________ (填字母)。
a.氧化剂 b.还原剂 c.酸性物质 d.碱性物质
X转化为Z可以说明氧化还原的实质是_________ ,检验Z中阴离子的实验操作方法是_________ 。
Ⅰ.离子反应
(1)向0.2mol·L-1Ba(OH)2溶液中滴入几滴酚酞溶液,装置如图。接通电源,向该溶液中滴入0.2molL-1H2SO4溶液。
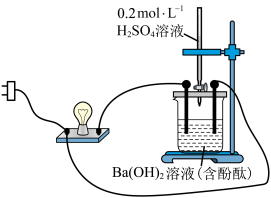
①接通电源前,能说明Ba(OH)2在水中电离的实验现象为
②随着H2SO4溶液的滴入,观察到烧杯中溶液红色逐渐褪去,产生白色沉淀,小灯泡亮度变暗,这些现象说明该反应的微观本质是Ba2+和OH-浓度降低,写出该反应的离子方程式
(2)向0.2mol·L-1Ba(OH)2溶液中滴入0.1mol·L-1的盐酸,测定电导率的变化如图所示。
回答下列问题:
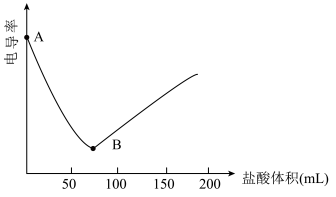
②下列化学反应的离子方程式与Ba(OH)2溶液和稀盐酸反应相同的是
A.Ba(OH)2溶液和稀硫酸 B.澄清石灰水和稀硝酸
C.NaOH溶液和NaHCO3溶液 D.浓氨水和浓盐酸
Ⅱ.氧化还原反应
(3)部分含硫物质如图所示,其中H2S和X是大气污染物。这些物质之间的相互转化为工业生产和处理环境问题提供了理论支持。
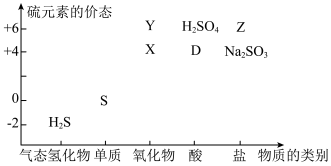
 ,其中反应①的离子方程式是
,其中反应①的离子方程式是a.氧化剂 b.还原剂 c.酸性物质 d.碱性物质
X转化为Z可以说明氧化还原的实质是
您最近一年使用:0次
2023-04-23更新
|
170次组卷
|
3卷引用:河南省南阳市2022-2023学年高一上学期1月期末考试化学试题
河南省南阳市2022-2023学年高一上学期1月期末考试化学试题河南省南阳市唐河县第一高级中学2023-2024学年高一上学期12月月考化学试题(已下线)专项02 离子反应和氧化还原反应的应用-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
2 . 某实验小组为制备高铁酸钾( )并进行相关探究,设计如下实验装置:
)并进行相关探究,设计如下实验装置:
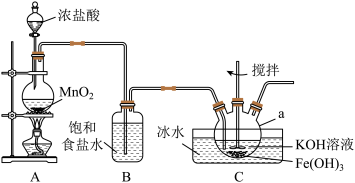
已知:高铁酸钾为紫色固体,可溶于水,微溶于浓KOH溶液,难溶于有机物,在0~5℃、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出 。请回答下列问题:
。请回答下列问题:
(1)仪器a的名称为___________ ;装置B中饱和食盐水的作用是___________ 。
(2)装置A制取氯气的反应中,氧化剂和还原剂的物质的量之比为___________ 。
(3)装置C中生成 的离子方程式为
的离子方程式为___________ 。
(4)该实验装置中存在的一个明显缺陷是___________ 。
(5)将装置C中混合物溶于冷的浓KOH溶液中,过滤,用无水乙醇洗涤,即得粗产品。粗产品中的可溶性杂质可通过___________ 方法进一步提纯。
 )并进行相关探究,设计如下实验装置:
)并进行相关探究,设计如下实验装置:
已知:高铁酸钾为紫色固体,可溶于水,微溶于浓KOH溶液,难溶于有机物,在0~5℃、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出
 。请回答下列问题:
。请回答下列问题:(1)仪器a的名称为
(2)装置A制取氯气的反应中,氧化剂和还原剂的物质的量之比为
(3)装置C中生成
 的离子方程式为
的离子方程式为(4)该实验装置中存在的一个明显缺陷是
(5)将装置C中混合物溶于冷的浓KOH溶液中,过滤,用无水乙醇洗涤,即得粗产品。粗产品中的可溶性杂质可通过
您最近一年使用:0次
2023-06-21更新
|
105次组卷
|
2卷引用:河南省大联考2022-2023学年高二下学期阶段性测试(五)化学试题
解题方法
3 . 回答下列问题
(1)在汽车尾气系统中装置催化转化器,可有效降低 NOx 的排放,当尾气中空气不足时,NOx在催化转化器中被还原成 N2 排出。 写出 NO 被 CO 还原的化学方程式:_____ 。
(2)实验室里迅速制备少量氯气可利用以下反应:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
①用双线桥法表示出电子转移情况:_____ 。
②用单线桥法表示出电子转移情况:_____ 。
③该反应中氧化剂是_____ ,发生氧化反应的是_____ 。
(1)在汽车尾气系统中装置催化转化器,可有效降低 NOx 的排放,当尾气中空气不足时,NOx在催化转化器中被还原成 N2 排出。 写出 NO 被 CO 还原的化学方程式:
(2)实验室里迅速制备少量氯气可利用以下反应:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
①用双线桥法表示出电子转移情况:
②用单线桥法表示出电子转移情况:
③该反应中氧化剂是
您最近一年使用:0次
2021-10-28更新
|
99次组卷
|
2卷引用:河南省周口经济开发区黄泛区高级中学2021-2022学年高一上学期第一次月考化学试题



