1 . 氯气是一种重要的化工原料,可用于生产塑料、合成纤维和染料等。实验室某实验小组现用下图装置来制取氯气并对氯气的某些性质和用途进行探究(K为开关,夹持装置已省略)。请回答下列问题:__________ 。
(2)检验装置A、B的气密性:将仪器①的活塞和开关K关闭,从长颈漏斗处加水至液面高于锥形瓶中的液面,若________ ,则说明装置气密性良好。
(3)装置A中发生反应的化学方程式为__________ 。
(4)装置E中的试剂是___________ ,作用是___________ 。
(5)装置C中为湿润的KI-淀粉试纸,通入 后试纸变蓝,则该反应的离子方程式为
后试纸变蓝,则该反应的离子方程式为_________ ;该小组为了研究干燥的氯气与金属钠之间的反应,欲在装置C中直接放置一块纯净的金属钠进行实验,该方案存在不妥之处,请你指出不妥之处并改正:__________ 。
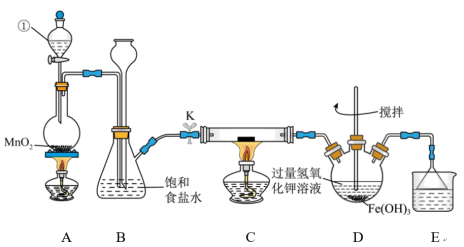
(2)检验装置A、B的气密性:将仪器①的活塞和开关K关闭,从长颈漏斗处加水至液面高于锥形瓶中的液面,若
(3)装置A中发生反应的化学方程式为
(4)装置E中的试剂是
(5)装置C中为湿润的KI-淀粉试纸,通入
 后试纸变蓝,则该反应的离子方程式为
后试纸变蓝,则该反应的离子方程式为
您最近一年使用:0次
2024-03-19更新
|
45次组卷
|
2卷引用:湖南省雅礼教育集团2023-2024学年高二下学期期中考试化学试题
2 . 氯元素是非常重要的非金属元素,某化学活动社团为了探究氯气的制法、性质和用途,设计了如下实验装置。

(1)B中饱和食盐水的作用是_______ 。
(2)请写出二氧化锰与浓盐酸反应的化学方程式_______ 。
(3)广口瓶C、E中的有色布条褪色的是_______ (填“C”或“E”)。
(4)装置F可用于制漂白粉,漂白粉的有效成分是_______ 。(写化学式)
(5)烧杯G的作用是处理尾气。请写出G中反应的离子方程式_______ 。
(6)检验G中阳离子的方法是_______ ;写出I中反应化学方程式_______ 。

(1)B中饱和食盐水的作用是
(2)请写出二氧化锰与浓盐酸反应的化学方程式
(3)广口瓶C、E中的有色布条褪色的是
(4)装置F可用于制漂白粉,漂白粉的有效成分是
(5)烧杯G的作用是处理尾气。请写出G中反应的离子方程式
(6)检验G中阳离子的方法是
您最近一年使用:0次
名校
解题方法
3 . 氯气在工业生产中有重要的用途。某课外活动小组利用下列装置在实验室中制备氯气,并进行有关氯气性质的研究。

(1)该小组同学欲用图1所示仪器及试剂(不一定全用)制备并收集干燥纯净的氯气。
①写出实验室制氯气的化学方程式:____ ;浓盐酸在反应中体现了____ (填编号)的性质。
A.酸性 B.氧化性 C.还原性 D.不稳定性
②选择装置,将各仪器按先后顺序连接起来,应该是a接_____,_____接_____,_____接_____,_____接h(用导管口处的字母表示)。____
(2)该小组同学设计并分别利用图2和图3所示装置探究氯气的氧化性,已知碘单质遇淀粉会变蓝。

①G中的现象是_____ ,原因是_____ (用化学方程式表示)。
②H中的现象是____ ,I中发生的离子反应方程式为____ 。

(1)该小组同学欲用图1所示仪器及试剂(不一定全用)制备并收集干燥纯净的氯气。
①写出实验室制氯气的化学方程式:
A.酸性 B.氧化性 C.还原性 D.不稳定性
②选择装置,将各仪器按先后顺序连接起来,应该是a接_____,_____接_____,_____接_____,_____接h(用导管口处的字母表示)。
(2)该小组同学设计并分别利用图2和图3所示装置探究氯气的氧化性,已知碘单质遇淀粉会变蓝。

①G中的现象是
②H中的现象是
您最近一年使用:0次
4 . 氯气在人类生产、生活中用途非常常广泛,化工生产过程中排出的大量含氯废气与氯化氢气体用过量氢氧化钠吸收,在吸收后的溶液中可以大量共存的离子是
A. | B. | C. | D. |
您最近一年使用:0次
2022-09-13更新
|
423次组卷
|
3卷引用:湖南省长沙市长郡中学2022-2023学年高一上学期期中考试化学试题



