名校
1 . 硫及其化合物的“价-类”二维图体现了化学变化之美。___________ (用化学式表示,下同),从硫元素的化合价角度分析,图中所示物质既有氧化性又有还原性的物质有___________ 。
(2)将X与H2S混合,反应的化学方程式为___________ ,其中氧化产物与还原产物的物质的量之比为___________ 。
(3)Z的稀溶液可与Ba(OH)2溶液发生反应,其离子方程式为___________ ;
(4)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是___________;
(5)某小组实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取SO2,有同学认为制得的SO2中可能混有杂质(不考虑水蒸气),其杂质气体的化学式为___________ 。
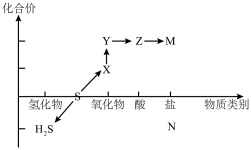
(2)将X与H2S混合,反应的化学方程式为
(3)Z的稀溶液可与Ba(OH)2溶液发生反应,其离子方程式为
(4)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是___________;
| A.Na2S+S | B.Na2SO3+S | C.SO2+Na2SO4 | D.Na2SO3+Na2SO4 |
(5)某小组实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取SO2,有同学认为制得的SO2中可能混有杂质(不考虑水蒸气),其杂质气体的化学式为
您最近一年使用:0次
名校
解题方法
2 . 氮和硫是化工生产中的重要元素。下列相关物质的性质与用途具有对应关系的是
| A.液氨汽化时吸收大量热,可用作制冷剂 |
| B.碳酸氢铵受热易分解,可用作化学肥料 |
| C.二氧化硫易溶于水,可用作纸浆漂白剂 |
| D.浓硫酸具有吸水性,可用来作氨气的干燥剂 |
您最近一年使用:0次
3 . 哲学中“量变引起质变”规律广泛存在于化学反应.下列反应不符合这一规律的是
| A.Fe-Cu合金和稀硝酸反应 | B.Zn和硫酸反应 |
C.氨水吸收尾气中的 | D.硫黄在空气中燃烧 |
您最近一年使用:0次
4 . 现有下列5种与生产生活相关的物质。
①碳酸氢钠②浓硫酸③氧化铁④次氯酸钠⑤四氧化三铁
(1)常用作油漆、涂料的红色颜料的是_______ (填序号)。
(2)用作治疗胃酸的是_______ (填序号)。
(3)84消毒液的主要成分是_______ (填序号)。
(4)具有磁性的是_______ (填序号)。
(5)能作干燥剂的是_______ (填序号)。
①碳酸氢钠②浓硫酸③氧化铁④次氯酸钠⑤四氧化三铁
(1)常用作油漆、涂料的红色颜料的是
(2)用作治疗胃酸的是
(3)84消毒液的主要成分是
(4)具有磁性的是
(5)能作干燥剂的是
您最近一年使用:0次
5 . 下列实验操作对应现象描述正确的是
| A.向紫色石蕊溶液中滴加氨水,溶液变红色 | B.蘸有浓硫酸的玻璃棒接近氨水瓶口,产生白烟 |
C.加热含足量 的品红溶液,溶液变红色 的品红溶液,溶液变红色 | D.在稀硫酸中加入铁粉,溶液变黄色 |
您最近一年使用:0次
名校
解题方法
6 . 在下列反应中,硫元素表现出氧化性的是
| A.稀硫酸与锌粒的反应 | B.浓硫酸与铜反应 |
| C.硫化氢使氯水褪色 | D.三氧化硫与水反应 |
您最近一年使用:0次
2024-04-19更新
|
232次组卷
|
2卷引用:山西省临汾市襄汾高级中学校2023-2024学年度高一下学期第一次月考化学试题
名校
解题方法
7 . 下列说法正确的是
A.实验室可用 和稀 和稀 反应制备 反应制备 气体 气体 |
| B.碳酸钡可用于胃肠X射线造影检查 |
C.向稀 中加入过量 中加入过量 粉,充分反应后,滴入 粉,充分反应后,滴入 溶液,溶液变成红色 溶液,溶液变成红色 |
D.向 溶液中加入足量铜片并加热,充分反应后,被还原 溶液中加入足量铜片并加热,充分反应后,被还原 的物质的量小于 的物质的量小于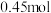 |
您最近一年使用:0次
2024-04-18更新
|
195次组卷
|
2卷引用:山西省临汾市襄汾高级中学校2023-2024学年度高一下学期第一次月考化学试题
名校
8 . 化学与生产、生活密切相关,下列说法不正确的是
| A.碳化硅俗称金刚砂,可用作耐高温材料 |
| B.在医疗上,硫酸钡、碳酸钡均可用作消化系统X射线检查的内服剂 |
| C.常温下,为方便运输,可用铁制容器来盛装浓硝酸或浓硫酸 |
D.FeCl2、 都可以通过化合反应制得 都可以通过化合反应制得 |
您最近一年使用:0次
名校
解题方法
9 . 氮和硫是化工生产中的重要元素。下列相关物质的性质与用途具有对应关系的是
| A.氮气的化学性质稳定、可用作保存食品 |
| B.碳酸氢铵受热易分解,可用作化学肥料 |
| C.二氧化硫易溶于水,可用作纸浆漂白剂 |
| D.浓硫酸具有脱水性,可用作气体干燥剂 |
您最近一年使用:0次
10 . 为检验浓硫酸和木炭反应的产物,某同学设计如图所示装置进行实验。据此回答下列问题:

(1)指出上述装置中的一处错误:___________ ;写出装置A中发生反应的化学方程式:___________ 。
(2)装置B中无水硫酸铜的作用是___________ ;证明产物中有CO2的实验现象是___________ ;浓硫酸与木炭的反应体现了浓H2SO4的___________ 性。
(3)取下装置C,在该试管口套上气球,将无色溶液加热恢复至红色,冷却后,发现溶液颜色___________ (填“变深”或"变浅”)。
(4)装置C可以用装置F代替,则装置F中SO2与Fe3+发生反应的离子方程式为___________ ,某同学为验证SO2与Fe3+发生反应,设计如下实验:取适量反应后的溶液,滴加少量溴水,溴水褪色说明发生反应。该方案是否合理并说明理由:___________ 。

(1)指出上述装置中的一处错误:
(2)装置B中无水硫酸铜的作用是
(3)取下装置C,在该试管口套上气球,将无色溶液加热恢复至红色,冷却后,发现溶液颜色
(4)装置C可以用装置F代替,则装置F中SO2与Fe3+发生反应的离子方程式为
您最近一年使用:0次



