名校
解题方法
1 . 下列说法正确的是
A. 通入紫色石蕊试液,溶液先变红后褪色,体现了 通入紫色石蕊试液,溶液先变红后褪色,体现了 酸性氧化物的性质和漂白性 酸性氧化物的性质和漂白性 |
| B.加热条件下,碳单质与浓硝酸反应,体现了浓硝酸的氧化性和酸性 |
| C.浓硫酸使胆矾由蓝色变为无色,说明浓硫酸具有吸水性 |
D.制玻璃的反应 说明非金属性: 说明非金属性: |
您最近一年使用:0次
2 . 下列类比结果正确的是
A. 与 与 溶液不反应,则 溶液不反应,则 与 与 溶液也不反应 溶液也不反应 |
B. 与S反应生成 与S反应生成 ,则 ,则 与S反应生成 与S反应生成 |
C.实验室用浓硫酸和 固体共热制 固体共热制 ,则可用浓硫酸和 ,则可用浓硫酸和 共热制 共热制 |
| D.浓硝酸常温下可溶解铜,则浓硝酸常温下也可以溶解铁 |
您最近一年使用:0次
名校
3 . 下列气体既能用浓硫酸又能用碱石灰干燥的是
A.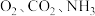 | B.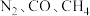 | C.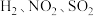 | D.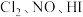 |
您最近一年使用:0次
4 . 室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向 溶液中通入 溶液中通入 ,溶液变为浅绿色 ,溶液变为浅绿色 | 还原性: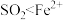 |
| B | 向盛有某盐溶液的试管中滴入氢氧化钠溶液后,试管口处湿润的红色石蕊试纸未变蓝 | 该盐中一定不含 |
| C | 将含有 的废气(含有少量氨气)通入 的废气(含有少量氨气)通入 溶液中,出现白色沉淀 溶液中,出现白色沉淀 |  与 与 溶液反应生成 溶液反应生成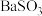 沉淀 沉淀 |
| D | 向蔗糖中加入浓硫酸,搅拌得黑色海绵状固体,并放出刺激性气味的气体 | 浓硫酸体现脱水性和强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 下列说法正确的是
| A.浓硫酸有强氧化性,所以浓硫酸不可以用于干燥具有还原性的气体SO2 |
| B.浓硫酸具有吸水性,因而能使蔗糖炭化 |
| C.pH小于7的雨水通常称为酸雨 |
| D.SO2的漂白原理与Ca(ClO)2溶液、H2O2和氯水的漂白原理不同 |
您最近一年使用:0次
6 . 某化学兴趣小组为探究铜与浓硫酸的反应,用如图所示装置进行有关实验.甲同学取 片和
片和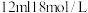 浓
浓 放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的
放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的 和
和 剩余。
剩余。 与浓
与浓 反应的化学方程式是
反应的化学方程式是____________ 。
(2)装置D盛有品红溶液,当C中气体集满后,D中有可能观察到的现象是____________ ,装置D中试管口放置的棉花中应浸一种液体,该液体是____________ ,其作用是____________ 。
(3)装置B的作用是贮存多余的气体.当D处有明显现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中试剂瓶中液面下降,长颈漏斗中液面上升.B中应放置的液体是____________ (填序号)。
a.水 b.酸性 溶液 c.浓溴水 d.饱和
溶液 c.浓溴水 d.饱和 溶液
溶液
 片和
片和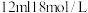 浓
浓 放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的
放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的 和
和 剩余。
剩余。 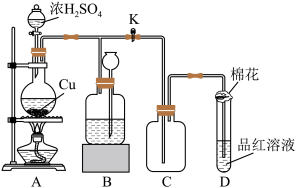
 与浓
与浓 反应的化学方程式是
反应的化学方程式是(2)装置D盛有品红溶液,当C中气体集满后,D中有可能观察到的现象是
(3)装置B的作用是贮存多余的气体.当D处有明显现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中试剂瓶中液面下降,长颈漏斗中液面上升.B中应放置的液体是
a.水 b.酸性
 溶液 c.浓溴水 d.饱和
溶液 c.浓溴水 d.饱和 溶液
溶液
您最近一年使用:0次
7 . 已知A、B、C、D、E、F、G、H可以发生如图所示的转化关系,反应中部分生成物已略去。其中,A、G为同一主族元素形成的单质,B、C、H在通常情况下为气体,E是水晶的主要成分,化合物C是一种形成酸雨的大气污染物。________ ;F________ 。
(2)反应①的化学方程式是________ 。
反应②的离子方程式是________ 。
(3)下列溶液中能用来区分B和C气体的是________ (填序号)。
①澄清石灰水 ② 溶液 ③酸性
溶液 ③酸性 溶液 ④氯水 ⑤品红溶液 ⑥紫色石蕊溶液
溶液 ④氯水 ⑤品红溶液 ⑥紫色石蕊溶液
(4) 的酸性
的酸性________ D的酸性(填“强于”或“弱于”),请用离子方程式予以证明:________ 。

(2)反应①的化学方程式是
反应②的离子方程式是
(3)下列溶液中能用来区分B和C气体的是
①澄清石灰水 ②
 溶液 ③酸性
溶液 ③酸性 溶液 ④氯水 ⑤品红溶液 ⑥紫色石蕊溶液
溶液 ④氯水 ⑤品红溶液 ⑥紫色石蕊溶液(4)
 的酸性
的酸性
您最近一年使用:0次
2024-05-08更新
|
122次组卷
|
2卷引用:甘肃省天水市第一中学2023-2024学年高一下学期4月月考化学试题
名校
8 . 硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。____________ 。
(2)X与Y能发生反应,还原剂与氧化剂的物质的量之比为______ 。
(3) 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是____________ 。
(4)硫酸是用途广泛的化工原料,可作脱水剂,吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸为原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即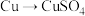
方案乙:由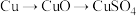
①方案甲中铜和浓硫酸反应的化学方程式是____________ 。该反应体现了浓硫酸的____________ 。
②这两种方案,你认为哪一种方案更合理?______ ,理由是____________ 。

(2)X与Y能发生反应,还原剂与氧化剂的物质的量之比为
(3)
 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是(4)硫酸是用途广泛的化工原料,可作脱水剂,吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸为原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即
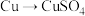
方案乙:由
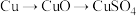
①方案甲中铜和浓硫酸反应的化学方程式是
②这两种方案,你认为哪一种方案更合理?
您最近一年使用:0次
名校
解题方法
9 . 化学实验是验证假设、推断结论的重要方法。某小组同学学习了氧化还原知识后,对 的性质进行了探究。
的性质进行了探究。
(1)写出碳与浓硫酸在加热条件下反应的化学方程式:________ ,装置④的作用是________ ,证明产物中有 的实验现象是
的实验现象是________ 。
(2)装置⑤中溶液不褪色,⑥中溶液变浑浊,据此现象能否说明装置①的反应产物中有 ?
?________ (填“能”或“不能”),理由是________ 。
Ⅱ.有同学认为 、
、 均是酸性氧化物,性质相似,由
均是酸性氧化物,性质相似,由 与
与 溶液反应,推测
溶液反应,推测 与
与 溶液反应也生成
溶液反应也生成 ,通过如图所示装置验证假设。实验过程发现:开始装置A中出现浑浊,溶液逐渐变为黄绿色,随着
,通过如图所示装置验证假设。实验过程发现:开始装置A中出现浑浊,溶液逐渐变为黄绿色,随着 不断通入,产生大量白色沉淀,溶液黄绿色又褪去。
不断通入,产生大量白色沉淀,溶液黄绿色又褪去。________ 。
(4)通入 一段时间后,黄绿色消失,发生反应的离子方程式是
一段时间后,黄绿色消失,发生反应的离子方程式是________ 。
 的性质进行了探究。
的性质进行了探究。
(1)写出碳与浓硫酸在加热条件下反应的化学方程式:
 的实验现象是
的实验现象是(2)装置⑤中溶液不褪色,⑥中溶液变浑浊,据此现象能否说明装置①的反应产物中有
 ?
?Ⅱ.有同学认为
 、
、 均是酸性氧化物,性质相似,由
均是酸性氧化物,性质相似,由 与
与 溶液反应,推测
溶液反应,推测 与
与 溶液反应也生成
溶液反应也生成 ,通过如图所示装置验证假设。实验过程发现:开始装置A中出现浑浊,溶液逐渐变为黄绿色,随着
,通过如图所示装置验证假设。实验过程发现:开始装置A中出现浑浊,溶液逐渐变为黄绿色,随着 不断通入,产生大量白色沉淀,溶液黄绿色又褪去。
不断通入,产生大量白色沉淀,溶液黄绿色又褪去。
(4)通入
 一段时间后,黄绿色消失,发生反应的离子方程式是
一段时间后,黄绿色消失,发生反应的离子方程式是
您最近一年使用:0次
名校
解题方法
10 . 根据下列实验操作和现象所得出的结论或解释正确的是
选项 | 实验操作和现象 | 结论或解释 |
A | 将 气体通入滴入酚酞的NaOH溶液,溶液红色褪去 气体通入滴入酚酞的NaOH溶液,溶液红色褪去 |  具有漂白性 具有漂白性 |
B | 将一块用砂纸打磨过的铝条放入试管,再加入98%的浓硫酸,铝条表面无明显现象 | 铝与浓硫酸常温下不反应 |
C | 将 通入 通入 溶液中生成的气体,先通入足量的酸性 溶液中生成的气体,先通入足量的酸性 溶液,再通入澄清石灰水中变浑浊 溶液,再通入澄清石灰水中变浑浊 | 说明酸性: |
D | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



