1 . 下列关于浓硫酸的叙述不正确的是
| A.用浓硫酸在纸上书写的字迹变黑,体现了浓硫酸的脱水性 |
| B.空气中敞口久置的浓硫酸质量增大,体现了浓硫酸的吸水性 |
| C.常温下,浓硫酸可以用铁罐车来运输 |
| D.稀释浓硫酸时,将水直接注入浓硫酸中 |
您最近半年使用:0次
2 . 下列不能 用浓硫酸干燥的气体是
| A.N2 | B.NH3 | C.SO2 | D.H2 |
您最近半年使用:0次
名校
3 . 氮、硫的氧化物都会引起环境问题,越来越引起人们的重视。如图是氮、硫元素的各种价态与物质类别的对应关系:
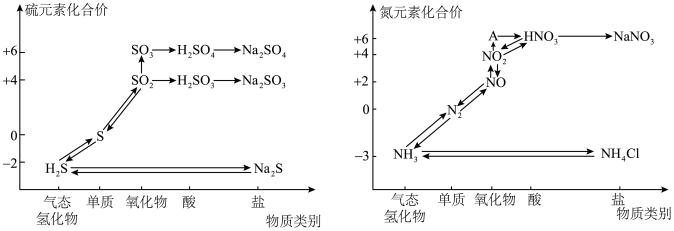
(1)根据A对应的化合价和物质类别, 为
为___________ (写分子式),从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的含氮化合物有___________ 。
(2)氮气的结构决定了氮气能够在空气中稳定存在,写出氮气的电子式___________ 。
(3)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择___________ ,反应的离子方程式为___________ 。
(4)工厂里常采用 溶液吸收
溶液吸收 气体,使其转化为化工产品
气体,使其转化为化工产品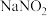 和
和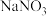 ,试写出其化学方程式:
,试写出其化学方程式:___________ 。
(5)铜与稀硫酸不反应,在一定条件下却可以与浓硫酸发生反应。写出铜与浓硫酸反应的化学方程式:___________ 。

(1)根据A对应的化合价和物质类别,
 为
为(2)氮气的结构决定了氮气能够在空气中稳定存在,写出氮气的电子式
(3)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择
(4)工厂里常采用
 溶液吸收
溶液吸收 气体,使其转化为化工产品
气体,使其转化为化工产品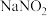 和
和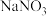 ,试写出其化学方程式:
,试写出其化学方程式:(5)铜与稀硫酸不反应,在一定条件下却可以与浓硫酸发生反应。写出铜与浓硫酸反应的化学方程式:
您最近半年使用:0次
名校
4 . 按要求填空
(1)浓硫酸具有如下的性质: A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。
①浓硫酸使蔗糖变黑___________ ;
②碳投入热的浓硫酸中溶解___________ ;
③浓硫酸与氧化铜反应___________ ;
④浓硫酸干燥氢气___________ 。
(2)浓硝酸具有如下的性质:A.酸性B.强氧化性C.不稳定性,下列事实主要表现浓硝酸的什么性质(填字母序号)。
①浓硝酸需避光保存___________ ;
②常温下可用铝或者铁遇浓硝酸钝化___________ 。
(3)二氧化硫气体在下列反应中表现的性质填写在横线上(填字母序号)。
A氧化性 B.漂白性 C.还原性 D.酸性氧化物的性质
①SO2+2OH= +H2O
+H2O___________ ;
②SO2+2H2S=3S↓+2H2O___________ ;
③SO2+Ca(OH)2=CaSO3↓+H2O___________ ;
④SO2+Cl2+2H2O=2HCl+H2SO4___________ 。
(4)氮元素是地球大气中含量最多的元素,请完成下列有关问题:
①写出氮元素的原子结构示意图:___________ 。
②通常情况下,氮气性质不活泼,其原因是___________ 。
A氮分子是双原子分子 B.氮元素的非金属性很强
C.氮原子的半径较小 D.破坏氮分子中的化学键很难
③N2的电子式:___________ 。
④氨是一种重要的化工原料,请写出工业合成氨的化学方程式:___________ 。
⑤检验NH3的方法是___________ 。
(1)浓硫酸具有如下的性质: A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。
①浓硫酸使蔗糖变黑
②碳投入热的浓硫酸中溶解
③浓硫酸与氧化铜反应
④浓硫酸干燥氢气
(2)浓硝酸具有如下的性质:A.酸性B.强氧化性C.不稳定性,下列事实主要表现浓硝酸的什么性质(填字母序号)。
①浓硝酸需避光保存
②常温下可用铝或者铁遇浓硝酸钝化
(3)二氧化硫气体在下列反应中表现的性质填写在横线上(填字母序号)。
A氧化性 B.漂白性 C.还原性 D.酸性氧化物的性质
①SO2+2OH=
 +H2O
+H2O②SO2+2H2S=3S↓+2H2O
③SO2+Ca(OH)2=CaSO3↓+H2O
④SO2+Cl2+2H2O=2HCl+H2SO4
(4)氮元素是地球大气中含量最多的元素,请完成下列有关问题:
①写出氮元素的原子结构示意图:
②通常情况下,氮气性质不活泼,其原因是
A氮分子是双原子分子 B.氮元素的非金属性很强
C.氮原子的半径较小 D.破坏氮分子中的化学键很难
③N2的电子式:
④氨是一种重要的化工原料,请写出工业合成氨的化学方程式:
⑤检验NH3的方法是
您最近半年使用:0次
5 . 完成下列问题
(1)请结合SO2类别、价态及特性,在如下图实验装置验证SO2的性质(经检验,装置的气密性良好)。___________ 。
②中的溶液褪色,写出该反应的离子方程式___________ 。
③中产生淡黄色浑浊,体现了SO2的___________ 。
(2)通入足量SO2后④中无明显现象,将其分成两份分别加入下列物质后均产生白色沉淀。
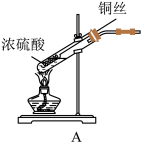
(3)A装置中试管内发生反应的化学方程式为___________ ,浓硫酸起到的作用是___________ 。实验中使用可抽动的铜丝的优点是___________ 。浓硫酸也可与非金属反应,写出碳与浓硫酸反应的化学方程式为___________ 。___________ 。
(1)请结合SO2类别、价态及特性,在如下图实验装置验证SO2的性质(经检验,装置的气密性良好)。
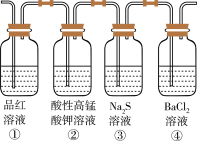
②中的溶液褪色,写出该反应的离子方程式
③中产生淡黄色浑浊,体现了SO2的
(2)通入足量SO2后④中无明显现象,将其分成两份分别加入下列物质后均产生白色沉淀。
| 加入的物质 | H2O2 | 氨水 |
| 沉淀的化学式 |
(3)A装置中试管内发生反应的化学方程式为
您最近半年使用:0次
名校
解题方法
6 . 硫酸是十分重要的化工原料。工业上用黄铁矿又称为二硫化亚铁 制备硫酸的工艺如下图所示。
制备硫酸的工艺如下图所示。 中硫元素的化合价是
中硫元素的化合价是_______ 。
(2)写出过程Ⅱ发生反应的化学方程式_______ 。
(3)下图是模拟工业过程Ⅱ来探究 的催化氧化过程。
的催化氧化过程。_______ 。
(4)装置丙中盛放的是 的浓硫酸,目的是
的浓硫酸,目的是_______ 。
(5)装置丁的作用是吸收并检验 已除净,现象是
已除净,现象是_______ ,写出反应的离子方程式_______ 。
(6)装置戊中的现象是_______ ,说明 催化氧化时有
催化氧化时有 剩余。
剩余。
 制备硫酸的工艺如下图所示。
制备硫酸的工艺如下图所示。
 中硫元素的化合价是
中硫元素的化合价是(2)写出过程Ⅱ发生反应的化学方程式
(3)下图是模拟工业过程Ⅱ来探究
 的催化氧化过程。
的催化氧化过程。
(4)装置丙中盛放的是
 的浓硫酸,目的是
的浓硫酸,目的是(5)装置丁的作用是吸收并检验
 已除净,现象是
已除净,现象是(6)装置戊中的现象是
 催化氧化时有
催化氧化时有 剩余。
剩余。
您最近半年使用:0次
7 . 浓硫酸分别与三种钠盐反应,现象如图。下列分析不正确的是

A. 中试管口白雾是 中试管口白雾是 遇水蒸气所致,利用硫酸的难挥发性 遇水蒸气所致,利用硫酸的难挥发性 |
B. 体现了浓硫酸的强氧化性 体现了浓硫酸的强氧化性 |
C. 中有 中有 产生 产生 |
D. 中浓 中浓 被还原成 被还原成 |
您最近半年使用:0次
名校
8 . 浓硫酸分别和三种钠盐反应,现象见图。下列分析正确的是

| A.①②③均为氧化还原反应 |
B.对比①和②可以说明还原性 |
C.②中试管口白雾是HCl遇水蒸气所致,说明酸性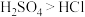 |
D.③中浓 被还原成 被还原成 |
您最近半年使用:0次
名校
解题方法
9 . 硫黄制酸在我国的工业发展进程中具有重要地位,其工业流程示意图如下,下列说法不正确的是
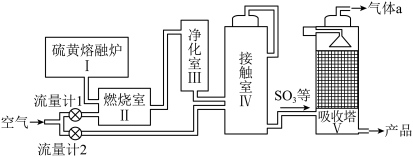
A.Ⅱ中主要反应的化学方程式: |
B.Ⅳ中主要反应的化学方程式: |
C.Ⅴ中用浓硫酸吸收 |
| D.Ⅱ、Ⅳ、Ⅴ中均采用逆流原理 |
您最近半年使用:0次
名校
10 . 关于M元素的有关图示,下列说法不正确的是
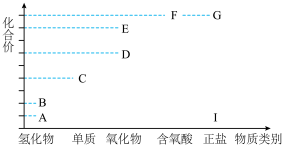
A.依据题给价一类二维图综合分析可知 元素为氮元素. 元素为氮元素. |
B.物质B可用作火箭燃料,其电子式为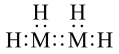 |
C.D或 均可在一定条件下与 均可在一定条件下与 反应得到C 反应得到C |
| D.物质F的浓溶液具有强氧化性,可以用铁制或铝制容器盛放 |
您最近半年使用:0次



