名校
1 .  和
和 在生产、生活和科学研究中有着广泛的应用,在实验室用下图装置验证木炭与浓硫酸反应中生成的气体成分,下列有关说法正确的是
在生产、生活和科学研究中有着广泛的应用,在实验室用下图装置验证木炭与浓硫酸反应中生成的气体成分,下列有关说法正确的是

 和
和 在生产、生活和科学研究中有着广泛的应用,在实验室用下图装置验证木炭与浓硫酸反应中生成的气体成分,下列有关说法正确的是
在生产、生活和科学研究中有着广泛的应用,在实验室用下图装置验证木炭与浓硫酸反应中生成的气体成分,下列有关说法正确的是
A.①中品红褪色证明 有氧化性 有氧化性 |
| B.②中的试剂X应该是浓硫酸 |
| C.③中的试剂Y应该是NaOH溶液 |
D.②中颜色变浅,但不消失,且③中出现浑浊,即可证明气体中有 |
您最近一年使用:0次
2023-07-17更新
|
277次组卷
|
5卷引用:黑龙江省哈尔滨市第三中学校2022-2023学年高一下学期期末考试化学试题
黑龙江省哈尔滨市第三中学校2022-2023学年高一下学期期末考试化学试题(已下线)第01讲 硫及其化合物-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)福建省福清第一中学2023-2024学年高一下学期开学适应性练习化学试题(已下线)5.1.2 硫酸新疆石河子第一中学2023-2024学年高二上学期9月月考化学试题
2 . 有关元素及其化合物知识的说法正确的是( )
| A.浓硝酸能与木炭反应,证明浓硝酸既具有强氧化性又具有强酸性 |
| B.浓硫酸具有吸水性,因而能使蔗糖炭化 |
| C.高温下SiO2与Na2CO3反应生成Na2SiO3和CO2,证明硅酸酸性强于碳酸 |
| D.铵盐受热都能分解,但不一定都能生成氨气 |
您最近一年使用:0次
名校
3 . 回答下列问题:
(1)写出下列实验事实与所给酸对应的性质(填序号)
A.酸性 B.挥发性 C.吸水性 D.脱水性 E.不稳定性 F.氧化性
①浓硝酸使紫色石蕊试液先变红后褪色___________
②浓硫酸可作氯气的干燥剂___________
③浓硫酸加到蔗糖中,蔗糖变黑___________
(2)“绿色化学”的主要内容之一是指从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物。下列化学反应符合“绿色化学”理念的是___________
①制 :
: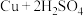 (浓)
(浓)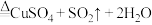
②制 ;
;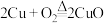 ;
; (稀)
(稀)
③制 :
: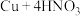 (浓)
(浓)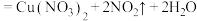
④制 :
: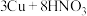 (稀)
(稀)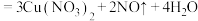
(3)某同学向 溶液中通入
溶液中通入 ,未观察到白色沉淀生成,由此可知酸性强弱:
,未观察到白色沉淀生成,由此可知酸性强弱:
___________ HCl(填“>”或“<”)。取上述所得溶液进行下列操作,能观察到白色沉淀生成的___________ (填字母)。
A.通入 B.滴加
B.滴加 溶液 C.滴加稀盐酸 D.滴加NaOH溶液
溶液 C.滴加稀盐酸 D.滴加NaOH溶液
(4) 中有+4价的硫,它既有氧化性又有还原性,现有试剂:溴水、
中有+4价的硫,它既有氧化性又有还原性,现有试剂:溴水、 溶液、
溶液、 、NaOH溶液、氨水。
、NaOH溶液、氨水。
①要证明 具有还原性,应选用的试剂是
具有还原性,应选用的试剂是___________ ,看到的现象是___________ 。
②选用 与
与 反应,反应的现象是
反应,反应的现象是___________ ,反应的离子方程式为___________ 。
(1)写出下列实验事实与所给酸对应的性质(填序号)
A.酸性 B.挥发性 C.吸水性 D.脱水性 E.不稳定性 F.氧化性
①浓硝酸使紫色石蕊试液先变红后褪色
②浓硫酸可作氯气的干燥剂
③浓硫酸加到蔗糖中,蔗糖变黑
(2)“绿色化学”的主要内容之一是指从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物。下列化学反应符合“绿色化学”理念的是
①制
 :
: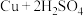 (浓)
(浓)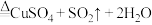
②制
 ;
;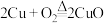 ;
; (稀)
(稀)
③制
 :
: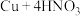 (浓)
(浓)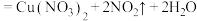
④制
 :
: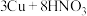 (稀)
(稀)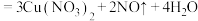
(3)某同学向
 溶液中通入
溶液中通入 ,未观察到白色沉淀生成,由此可知酸性强弱:
,未观察到白色沉淀生成,由此可知酸性强弱:
A.通入
 B.滴加
B.滴加 溶液 C.滴加稀盐酸 D.滴加NaOH溶液
溶液 C.滴加稀盐酸 D.滴加NaOH溶液(4)
 中有+4价的硫,它既有氧化性又有还原性,现有试剂:溴水、
中有+4价的硫,它既有氧化性又有还原性,现有试剂:溴水、 溶液、
溶液、 、NaOH溶液、氨水。
、NaOH溶液、氨水。①要证明
 具有还原性,应选用的试剂是
具有还原性,应选用的试剂是②选用
 与
与 反应,反应的现象是
反应,反应的现象是
您最近一年使用:0次
4 . 某化学学习小组为了探究铁质材料碳素钢(仅含有C和Fe)和浓硫酸反应的气体产物,利用下列装置(部分夹持仪器已省略)进行了如下实验探究活动:
(1)仪器X的名称为_______ 。
(2)能证明实验生成 的实验现象为
的实验现象为_______ ; 进入装置C中被氧化为
进入装置C中被氧化为 ,
, 被还原为
被还原为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:_______ 。
(3)实验过程中观察到G中无水硫酸铜由白色变成蓝色,F中发生反应的化学方程式为_______ ;产生该气体(F中的反应物)的原因为_______ 。
(4)若装置D中澄清石灰水变浑浊,装置H中澄清石灰水未变浑浊,再结合(3)推知碳素钢与浓硫酸反应产生的气体中除了含有 外,还有
外,还有_______ (填化学式);铁质材料中碳与浓硫酸反应的化学方程式为_______ 。装置H后增加装置I的目的是_______ 。

(1)仪器X的名称为
(2)能证明实验生成
 的实验现象为
的实验现象为 进入装置C中被氧化为
进入装置C中被氧化为 ,
, 被还原为
被还原为 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(3)实验过程中观察到G中无水硫酸铜由白色变成蓝色,F中发生反应的化学方程式为
(4)若装置D中澄清石灰水变浑浊,装置H中澄清石灰水未变浑浊,再结合(3)推知碳素钢与浓硫酸反应产生的气体中除了含有
 外,还有
外,还有
您最近一年使用:0次
2023-04-16更新
|
231次组卷
|
3卷引用:黑龙江省哈尔滨市2022-2023学年高一下学期学业质量检测化学试题
黑龙江省哈尔滨市2022-2023学年高一下学期学业质量检测化学试题湖北省宜昌市协作体2022-2023学年高一下学期期中考试化学试题(已下线)专题01 硫、氮、硅及其化合物-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)
名校
解题方法
5 . 某研究性学习小组利用所示装置探究二氧化硫的性质。(装置中固定仪器未画出)

(1)A中所装试剂为铜片和________ 。(填试剂名称)。
(2)D中试剂为0.5mol/LBaCl2溶液,实验中无明显现象,若改为同浓度的Ba(NO3)2溶液,则出现白色沉淀,此沉淀的化学式为______ ,证明SO2具有________ 性。
(3)装置B用于验证SO2的漂白性,则其中所装溶液可以为________ 。
(4)E中Na2S溶液用于验证SO2的氧化性,预期观察到的现象为________ ,涉及的离子方程式为_________ 。
(5)指出上述装置中一处明显的不足:________ 。

(1)A中所装试剂为铜片和
(2)D中试剂为0.5mol/LBaCl2溶液,实验中无明显现象,若改为同浓度的Ba(NO3)2溶液,则出现白色沉淀,此沉淀的化学式为
(3)装置B用于验证SO2的漂白性,则其中所装溶液可以为
| A.酸性高锰酸钾溶液 | B.品红溶液 |
| C.石蕊试液 | D.蓝色的碘—淀粉溶液 |
(4)E中Na2S溶液用于验证SO2的氧化性,预期观察到的现象为
(5)指出上述装置中一处明显的不足:
您最近一年使用:0次
名校
6 . 浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物,某同学设计了如下图所示的实验。请据此回答下列问题:
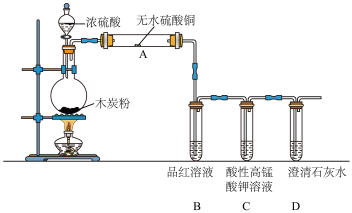
(1)连接好装置后(未加试剂),检验该装置的气密性的操作是:_____ 。
(2)实验过程中圆底烧瓶内发生反应的化学方程式为_____ 。
(3)A装置现象是_____ ,证明产物中_____ 生成(填写化学式,下同)。
(4)B装置现象是_____ ,证明产物中有_____ 生成。
(5)D装置现象是_____ ,证明产物中有_____ 生成。
(6)C装置的作用是_____ ,发生反应的离子方程式是_____ 。

(1)连接好装置后(未加试剂),检验该装置的气密性的操作是:
(2)实验过程中圆底烧瓶内发生反应的化学方程式为
(3)A装置现象是
(4)B装置现象是
(5)D装置现象是
(6)C装置的作用是
您最近一年使用:0次
7 . 下列实验操作能达到目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 证明Cu和浓 反应生成 反应生成 | 向少量铜与浓 反应后的溶液中慢慢加水,溶液变蓝 反应后的溶液中慢慢加水,溶液变蓝 |
| B | 证明 气体中混有 气体中混有 气体 气体 | 将混合气体通入盛有品红溶液的洗气瓶 |
| C | 证明木炭在加热时能与浓硝酸发生反应 | 将灼热的木炭加入到浓硝酸中,有红棕色气体产生 |
| D | 检验晶体中含有 | 取少量晶体溶于水,滴加NaOH溶液,用湿润的红色石蕊试纸检验产生的气体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 为检验浓硫酸与木炭在加热条件下反应产生的SO2和CO2气体,设计了如图所示实验装置,D中放有用I2和淀粉的蓝色溶液浸湿的脱脂棉。
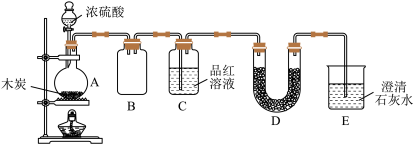
回答下列问题:
(1)装置A中发生反应的化学方程式为___________ ,该反应体现了浓硫酸的___________ 。
(2)实验时,装置B的作用是___________ 。
(3)装置D中发生反应的离子方程式为___________ ;当D中产生___________ 现象时,可以说明使E中澄清石灰水变浑浊的是CO2,而不是SO2。
(4)若不设置装置C,判断该装置是否也能证明浓硫酸与木炭在加热条件下能产生SO2并说明理由:___________ 。

回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)实验时,装置B的作用是
(3)装置D中发生反应的离子方程式为
(4)若不设置装置C,判断该装置是否也能证明浓硫酸与木炭在加热条件下能产生SO2并说明理由:
您最近一年使用:0次
名校
9 . 下列叙述不正确的是
| A | B | C | D |
 |  |   |  |
| 主要成分为Fe2O3,可用作红色涂料 | 利用丁达尔效应证明烧杯中的分散系是胶体 | 蔗糖中加入浓硫酸搅拌后变黑,因为浓硫酸有吸水性 | 加热时熔化的铝不滴落,证明Al2O3的熔点比Al高 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-01更新
|
469次组卷
|
2卷引用:黑龙江省双鸭山市第一中学2022-2023学年高一下学期4月月考(普通班)化学试题
名校
解题方法
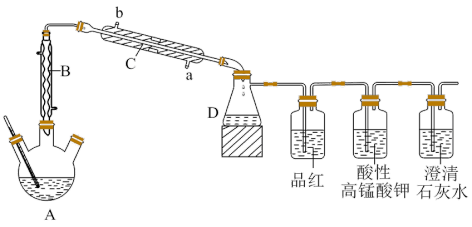
10 . 乙醇、浓硫酸在不同温度下可以发生不同的反应。某同学准备用如图装置制取乙醚(夹持及加热装置已略去)。
已知:①乙醇与浓硫酸混合加热到140℃时反应生成乙醚(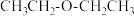 );加热到170℃时反应生成乙烯(
);加热到170℃时反应生成乙烯(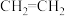 );
);
②乙醚和乙醇的部分物理性质如下表:
回答下列问题:
(1)加热前需向A中加入碎瓷片,若加热一段时间后发现没有加入碎瓷片,应该如何处理_______ 。
(2)仪器B的名称为_______ ;装置中B的作用为_______ ;C中冷凝水应该从_______ (填“a”或“b”)口进入。
(3)实验中发现A中溶液逐渐变黑,某同学猜测产生这种现象的原因是浓硫酸有脱水性,使乙醇碳化,碳与浓硫酸反应生成了 和
和 ,则D后面的三个洗气瓶中会看到
,则D后面的三个洗气瓶中会看到_______ 现象,证明该同学猜测正确。
(4)若实验中使用了20mL无水乙醇,最后收集到乙醚12mL,则该实验中乙醚的产率为_______ %。(保留整数)

已知:①乙醇与浓硫酸混合加热到140℃时反应生成乙醚(
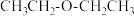 );加热到170℃时反应生成乙烯(
);加热到170℃时反应生成乙烯(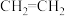 );
);②乙醚和乙醇的部分物理性质如下表:
性质 物质 | 沸点/℃ | 水中的溶解性 | 密度/( ) ) |
| 乙醇 | 78 | 任意比例混溶 | 0.8 |
| 乙醚 | 34.6 | 难溶 | 0.7 |
(1)加热前需向A中加入碎瓷片,若加热一段时间后发现没有加入碎瓷片,应该如何处理
(2)仪器B的名称为
(3)实验中发现A中溶液逐渐变黑,某同学猜测产生这种现象的原因是浓硫酸有脱水性,使乙醇碳化,碳与浓硫酸反应生成了
 和
和 ,则D后面的三个洗气瓶中会看到
,则D后面的三个洗气瓶中会看到(4)若实验中使用了20mL无水乙醇,最后收集到乙醚12mL,则该实验中乙醚的产率为
您最近一年使用:0次



