1 . 类比是研究物质性质的常用方法之一。下列说法正确的是
| A.已知溶解性CaCO3<Ca(HCO3)2,推测溶解性Na2CO3<NaHCO3 |
| B.已知Fe与S加热生成FeS,推测Cu与S加热生成Cu2S |
| C.已知Al(OH)3可以治疗胃酸过多,推测NaOH也可以治疗胃酸过多 |
| D.已知Fe可以置换出CuSO4溶液中的铜,推测Na也可以置换出CuSO4溶液中的铜 |
您最近一年使用:0次
2021-03-13更新
|
249次组卷
|
3卷引用:重庆市第七中学校2020-2021学年高一上学期12月月考化学试题
名校
解题方法
2 . 类推思维是化学解题中常用的一种思维方法,下列有关反应方程式的类推正确的是
| 已知 | 类推 | |
| A. | 将Fe加入 溶液中: 溶液中: | 将Na加入到 溶液中: 溶液中: |
| B. | 稀 硫酸与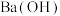 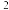 溶液反应至中性: 溶液反应至中性: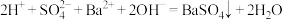 |  溶液与 溶液与 溶液反应至中性: 溶液反应至中性: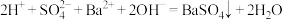 |
| C. | 铁和氯气反应: | 铁和硫单质反应: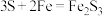 |
| D. |  是酸性气体,可以用浓 是酸性气体,可以用浓 干燥 干燥 |  也是酸性气体,可以用浓 也是酸性气体,可以用浓 干燥 干燥 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-03-13更新
|
396次组卷
|
5卷引用:重庆市第二十九中学2020-2021学年高一上学期12月月考化学试题
名校
解题方法
3 . 物质的类别和核心元素的化合价是研究物质性质的两个基本视角。请根据如图所示,回答下列问题:

(1)Y是形成酸雨的主要物质之一,它溶于水反应的化学方程式为_____ ;另一类硝酸型酸雨主要由人类活动产生的NOx造成的,写出NO2与水反应的化学方程式为______ ;酸雨的pH______ (填范围)。
(2)Y能使品红溶液褪色,它与一种黄绿色气体等体积通入水中得到的溶液却几乎没有漂白性,反应的离子方程式为_______ ;Y也能使酸性高锰酸钾溶液褪色,写出该反应的离子方程式,并用单线桥法标明电子转移的方向和数目_____ ,体现了Y的_____ 性。
(3)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为_____ 。
(4)现用98%的浓硫酸(ρ=1.84g/cm3)配制成浓度为0.5mol/L的稀硫酸500mL,回答下列问题:
①所需浓硫酸的体积为______ mL。
②将浓硫酸沿烧杯内壁缓缓注入盛水的烧杯中,不断搅拌的目的是_____ ,若搅拌过程中有液体溅出,会导致最终所配溶液浓度_____ (填“偏大”、“偏小”或“无影响”,下同)。
③在转入容量瓶前,烧杯中的液体应先_____ ,否则会使浓度_____ 。
(5)已知S的氧化性较弱,则硫粉与铜加热反应的化学方程式为_____ 。
(6)欲制备Na2S2O3(硫代硫酸钠),从氧化还原反应角度分析,合理的是_____ (填序号)。
A.Na2S+S B.Na2SO3+S C.Na2SO3+Na2SO4 D.SO2+Na2SO4

(1)Y是形成酸雨的主要物质之一,它溶于水反应的化学方程式为
(2)Y能使品红溶液褪色,它与一种黄绿色气体等体积通入水中得到的溶液却几乎没有漂白性,反应的离子方程式为
(3)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为
(4)现用98%的浓硫酸(ρ=1.84g/cm3)配制成浓度为0.5mol/L的稀硫酸500mL,回答下列问题:
①所需浓硫酸的体积为
②将浓硫酸沿烧杯内壁缓缓注入盛水的烧杯中,不断搅拌的目的是
③在转入容量瓶前,烧杯中的液体应先
(5)已知S的氧化性较弱,则硫粉与铜加热反应的化学方程式为
(6)欲制备Na2S2O3(硫代硫酸钠),从氧化还原反应角度分析,合理的是
A.Na2S+S B.Na2SO3+S C.Na2SO3+Na2SO4 D.SO2+Na2SO4
您最近一年使用:0次
2020-03-23更新
|
278次组卷
|
2卷引用:重庆市育才中学2019-2020学年高一下学期3月月考化学试题
4 . 下列反应中,调节反应物用量或浓度不会改变反应产物的是( )
| A.H2S在O2燃烧 | B.铁在硫蒸气中燃烧 |
| C.SO2通入澄清石灰水中 | D.硫酸中加入锌粉 |
您最近一年使用:0次
2020-01-12更新
|
263次组卷
|
9卷引用:09-10年万州二中高一下学期期末考试化学卷
名校
5 . 下列物质中,不能由单质直接化合生成的是( )
| A.NO2 | B.Cu2S | C.SO2 | D.FeCl3 |
您最近一年使用:0次
6 . 水银温度计打碎在地面上,可在汞滴上覆盖一层物质避免发生汞中毒,该物质是
| A.硫磺粉 | B.氯化钠 | C.生石灰 | D.纯碱 |
您最近一年使用:0次



