1 . 硫的化合物在生产、生活中应用广泛。根据所学知识,回答下列问题:
(1)某兴趣小组为探究 的还原性做了如图实验。
的还原性做了如图实验。

①通入足量 后,装置B中的现象是
后,装置B中的现象是___________ ,装置C的作用是___________ 。
②该小组同学认为 与
与 溶液发生的是氧化还原反应。写出
溶液发生的是氧化还原反应。写出 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:___________ 。
(2)铬是环境中的一种主要污染物,可以用焦亚硫酸钠( )处理含铬酸性废水(含有
)处理含铬酸性废水(含有 ),其反应为
),其反应为 ,反应中氧化剂与还原剂的物质的量之比为
,反应中氧化剂与还原剂的物质的量之比为___________ 。
(3) 具有多种性质。
具有多种性质。
①浓 使蔗糖变黑,体现了浓
使蔗糖变黑,体现了浓 具有
具有___________ 性。
②浓 在加热条件下可与碳单质反应,写出反应的化学方程式:
在加热条件下可与碳单质反应,写出反应的化学方程式:___________ 。
③过量的锌与一定量浓 反应,随着硫酸溶液变稀得到的两种气体产物依次为
反应,随着硫酸溶液变稀得到的两种气体产物依次为___________ 、___________ 。
(4)硫酸盐是化工生产和药物、颜料制备中的重要物质。
①石膏可用于调节水泥的凝结时间,生石膏的化学式为___________ 。
②绿矾的化学式为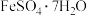 ,其用途有
,其用途有___________ (任写一点)。
(1)某兴趣小组为探究
 的还原性做了如图实验。
的还原性做了如图实验。
①通入足量
 后,装置B中的现象是
后,装置B中的现象是②该小组同学认为
 与
与 溶液发生的是氧化还原反应。写出
溶液发生的是氧化还原反应。写出 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:(2)铬是环境中的一种主要污染物,可以用焦亚硫酸钠(
 )处理含铬酸性废水(含有
)处理含铬酸性废水(含有 ),其反应为
),其反应为 ,反应中氧化剂与还原剂的物质的量之比为
,反应中氧化剂与还原剂的物质的量之比为(3)
 具有多种性质。
具有多种性质。①浓
 使蔗糖变黑,体现了浓
使蔗糖变黑,体现了浓 具有
具有②浓
 在加热条件下可与碳单质反应,写出反应的化学方程式:
在加热条件下可与碳单质反应,写出反应的化学方程式:③过量的锌与一定量浓
 反应,随着硫酸溶液变稀得到的两种气体产物依次为
反应,随着硫酸溶液变稀得到的两种气体产物依次为(4)硫酸盐是化工生产和药物、颜料制备中的重要物质。
①石膏可用于调节水泥的凝结时间,生石膏的化学式为
②绿矾的化学式为
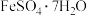 ,其用途有
,其用途有
您最近一年使用:0次
2024-01-09更新
|
725次组卷
|
3卷引用:河北省保定市部分高中2023-2024学年高一上学期12月期中化学试题
河北省保定市部分高中2023-2024学年高一上学期12月期中化学试题(已下线)第01讲 硫及其化合物-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)河北省邯郸市磁县第一中学2023-2024学年高一上学期六调月考化学试题
名校
解题方法
2 . 阅读下面一段材料并回答问题。
 是锌的一种氧化物,不溶于水、乙醇,可溶于大多数酸、强碱等,在浓氢氧化钠溶液中可生成
是锌的一种氧化物,不溶于水、乙醇,可溶于大多数酸、强碱等,在浓氢氧化钠溶液中可生成 。
。
 有着广泛的用途。它可用作白色颜料,俗称锌白,其优点是遇酸性气体
有着广泛的用途。它可用作白色颜料,俗称锌白,其优点是遇酸性气体 不变黑,因为生成的
不变黑,因为生成的 也是白色的。
也是白色的。 也可用于某些化工原料的脱硫,利用
也可用于某些化工原料的脱硫,利用 水悬浊液吸收
水悬浊液吸收 ,再通入空气,最终可得到
,再通入空气,最终可得到 。
。 具有收敛作用,可杀菌并且加速伤口愈合,在医药上常调制成软膏。
具有收敛作用,可杀菌并且加速伤口愈合,在医药上常调制成软膏。 还是新一代的光电半导体材料,因其具有良好的抗辐射性能,可以在太空等环境应用。
还是新一代的光电半导体材料,因其具有良好的抗辐射性能,可以在太空等环境应用。
工业上有多种制备 的方法,直接沉淀法是其中一种。该法是以可溶性锌盐和一水合氨(
的方法,直接沉淀法是其中一种。该法是以可溶性锌盐和一水合氨( )为原料,发生如下反应:
)为原料,发生如下反应: ;
; 。用此法可以制得纳米级
。用此法可以制得纳米级 ,其在磁、光、电、敏感性等方面具有普通
,其在磁、光、电、敏感性等方面具有普通 无法比拟的特殊性能和新用途。
无法比拟的特殊性能和新用途。

(1) 遇
遇 发生反应的化学方程式是
发生反应的化学方程式是___________ ; 用于工业脱硫最终生成
用于工业脱硫最终生成 的反应方程式为
的反应方程式为___________
(2)下列说法正确的是___________
A. 可用作光电半导体材料
可用作光电半导体材料
B.用一水合氨制备 的反应不是氧化还原反应
的反应不是氧化还原反应
C.纳米级 和普通
和普通 粒子大小不同,性能有所不同
粒子大小不同,性能有所不同
 是锌的一种氧化物,不溶于水、乙醇,可溶于大多数酸、强碱等,在浓氢氧化钠溶液中可生成
是锌的一种氧化物,不溶于水、乙醇,可溶于大多数酸、强碱等,在浓氢氧化钠溶液中可生成 。
。 有着广泛的用途。它可用作白色颜料,俗称锌白,其优点是遇酸性气体
有着广泛的用途。它可用作白色颜料,俗称锌白,其优点是遇酸性气体 不变黑,因为生成的
不变黑,因为生成的 也是白色的。
也是白色的。 也可用于某些化工原料的脱硫,利用
也可用于某些化工原料的脱硫,利用 水悬浊液吸收
水悬浊液吸收 ,再通入空气,最终可得到
,再通入空气,最终可得到 。
。 具有收敛作用,可杀菌并且加速伤口愈合,在医药上常调制成软膏。
具有收敛作用,可杀菌并且加速伤口愈合,在医药上常调制成软膏。 还是新一代的光电半导体材料,因其具有良好的抗辐射性能,可以在太空等环境应用。
还是新一代的光电半导体材料,因其具有良好的抗辐射性能,可以在太空等环境应用。工业上有多种制备
 的方法,直接沉淀法是其中一种。该法是以可溶性锌盐和一水合氨(
的方法,直接沉淀法是其中一种。该法是以可溶性锌盐和一水合氨( )为原料,发生如下反应:
)为原料,发生如下反应: ;
; 。用此法可以制得纳米级
。用此法可以制得纳米级 ,其在磁、光、电、敏感性等方面具有普通
,其在磁、光、电、敏感性等方面具有普通 无法比拟的特殊性能和新用途。
无法比拟的特殊性能和新用途。
(1)
 遇
遇 发生反应的化学方程式是
发生反应的化学方程式是 用于工业脱硫最终生成
用于工业脱硫最终生成 的反应方程式为
的反应方程式为(2)下列说法正确的是
A.
 可用作光电半导体材料
可用作光电半导体材料B.用一水合氨制备
 的反应不是氧化还原反应
的反应不是氧化还原反应C.纳米级
 和普通
和普通 粒子大小不同,性能有所不同
粒子大小不同,性能有所不同
您最近一年使用:0次
3 . 请从1-A和1-B两题中任选 1 个作答 ,若两题均作答,按1-A评分_______ 。
| 1-A补齐物质及其用途的连线 | 1-B补齐物质及其用途的连线 |
| 物质用途 A.氯气 a.作清洁燃料 B.乙烯 b.制漂白粉 C.甲烷 c.作制冷剂 D.氨 d.作植物生长调节剂 | 物质用途 A.过氧化钠 a.作光导纤维 B.二氧化硅 b.作供氧剂 C.碳酸钠 c.作漂白剂 D.二氧化硫 d.作食用碱 |
您最近一年使用:0次
名校
4 . 补齐物质及其用途的连线。________
| 物质 | 用途 |
| A.二氧化硫 | a.光导纤维 |
| B.液氨 | b.制硫酸 |
| C.次氯酸钠 | c.制冷剂 |
| D.二氧化硅 | d.漂白剂 |
您最近一年使用:0次
解题方法
5 . 氮、硫及其化合物是重要的化工原料,研究其性质、用途和转化具有重要意义。
(1)氮的化合物常用作制冷剂的是_______ (填名称),向蔗糖中滴加少量浓硫酸并搅拌,出现“黑色面包”,并产生刺激性无色气体,这一现象显示浓硫酸的_______ (填性质)。
(2)燃煤排放的尾气中含有二氧化硫、氮的氧化物(主要为NO)等污染物,工业上采用NaClO碱性溶液作为吸收剂可同时对烟气进行脱硫、脱硝。脱硫的离子方程式为_______ ,实验证明相对于 ,NO更难脱除,其原因可能是
,NO更难脱除,其原因可能是_______ 。
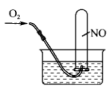
(3)将3.84 g Cu和足量稀硝酸充分反应,生成的气体体积为_______ L(在标准状况下),用排_______ (填“水”或“空气”)法收集该气体,将收集到的气体的试管倒立于水槽中缓缓通入_______ L (标准状况)使NO恰好完全反应,写出观察到的现象:
(标准状况)使NO恰好完全反应,写出观察到的现象:_______ 。
(1)氮的化合物常用作制冷剂的是
(2)燃煤排放的尾气中含有二氧化硫、氮的氧化物(主要为NO)等污染物,工业上采用NaClO碱性溶液作为吸收剂可同时对烟气进行脱硫、脱硝。脱硫的离子方程式为
 ,NO更难脱除,其原因可能是
,NO更难脱除,其原因可能是(3)将3.84 g Cu和足量稀硝酸充分反应,生成的气体体积为
 (标准状况)使NO恰好完全反应,写出观察到的现象:
(标准状况)使NO恰好完全反应,写出观察到的现象:
您最近一年使用:0次
解题方法
6 . 离子反应广泛用于化学研究、化工生产、医疗诊断和环境保护等各个领域。
(1)SO2是一种酸性氧化物。工业上,可用足量的稀氨水吸收少量SO2,写出发生反应的离子方程式:_______ 。
(2)SO2具有较强的还原性,能使酸性高锰酸钾溶液褪色,反应中被还原的元素是_______ (填元素符号)。
(3)某硫酸厂每天排放1.12×104m3(标准状况)尾气,其中含0.2%(体积分数)的SO2。现用浓度为0.5 mol/L的NaOH废碱液(假设其他成分不参与反应)进行处理,每天至少需要这种废碱液的体积为_______ L。
(4)某同学向BaCl2溶液中通入SO2,未观察到有白色沉淀生成。取上述所得溶液进行下列操作,依然不能观察到有白色沉淀生成的是_______(填标号)。
(5)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸作原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO4
方案乙:Cu→CuO→CuSO4
①方案甲中,铜和浓硫酸发生反应的化学方程式是_______ 。
②这两种方案,你认为哪一种方案更合理?_______ 。理由是_______ 。
(1)SO2是一种酸性氧化物。工业上,可用足量的稀氨水吸收少量SO2,写出发生反应的离子方程式:
(2)SO2具有较强的还原性,能使酸性高锰酸钾溶液褪色,反应中被还原的元素是
(3)某硫酸厂每天排放1.12×104m3(标准状况)尾气,其中含0.2%(体积分数)的SO2。现用浓度为0.5 mol/L的NaOH废碱液(假设其他成分不参与反应)进行处理,每天至少需要这种废碱液的体积为
(4)某同学向BaCl2溶液中通入SO2,未观察到有白色沉淀生成。取上述所得溶液进行下列操作,依然不能观察到有白色沉淀生成的是_______(填标号)。
| A.通入Cl2 | B.滴加稀硝酸 | C.滴加稀盐酸 | D.滴加NaOH溶液 |
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO4
方案乙:Cu→CuO→CuSO4
①方案甲中,铜和浓硫酸发生反应的化学方程式是
②这两种方案,你认为哪一种方案更合理?
您最近一年使用:0次
名校
7 . 补齐物质与其用途之间的连线_______ 。
| 物质 用途 A.浓硫酸——————a.作干燥剂 B.二氧化硫 b.作红色颜料 C.碳酸氢钠 c.作漂白剂 D.氧化铁 d.作膨松剂 |
您最近一年使用:0次
名校
8 . 补齐物质与其用途之间的连线_______ 。


您最近一年使用:0次



