1 .  是硫元素中一种重要物质。在生产生活中有容重要用途。
是硫元素中一种重要物质。在生产生活中有容重要用途。
(1)某研究小组用如图装置进行 与
与 溶液反应的相关实验(夹持装置已略去)
溶液反应的相关实验(夹持装置已略去) 时C中观察到的现象为
时C中观察到的现象为__________________________ 。
②根据以上现象,该小组同学认为 与
与 溶液发生氧化还原反应。
溶液发生氧化还原反应。
a.写出 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:___________________________ 。
b.该小组同学向C试管反应后的溶液中加入硝酸酸化的 溶液,若出现白色沉淀,即可证明反应生成了
溶液,若出现白色沉淀,即可证明反应生成了 。该做法
。该做法_________ (填“合理”或“不合理”),理由是___________________________ 。
③为了验证 具有还原性,实验中可以代替
具有还原性,实验中可以代替 溶液的试剂有
溶液的试剂有______________ (填字母)。
A.浓硫酸 B.酸性 溶液 C.碘水 D.NaCl溶液
溶液 C.碘水 D.NaCl溶液
(2)某同学利用如图所示的装置研究 的性质:(熔点:
的性质:(熔点: 为
为 ,
, 为16.8℃,沸点:
为16.8℃,沸点: 为
为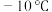 ,
, 为45℃)
为45℃) 催化氧化的反应,其化学方程式是
催化氧化的反应,其化学方程式是___________________________ 。
②甲同学按I、Ⅱ、Ⅲ、IV的顺序连接装置,装置Ⅲ中溶液逐渐褪色,生成 ,同时酸性增强,则该反应的离子方程式是(忽略
,同时酸性增强,则该反应的离子方程式是(忽略 的影响)
的影响)___________________________ 。
③乙同学按I、Ⅱ、IV顺序连接装置,若装置IV中有 溶液,反应后增重4.8g,则装置IV中发生反应的化学方程式是
溶液,反应后增重4.8g,则装置IV中发生反应的化学方程式是___________________________ 。
 是硫元素中一种重要物质。在生产生活中有容重要用途。
是硫元素中一种重要物质。在生产生活中有容重要用途。(1)某研究小组用如图装置进行
 与
与 溶液反应的相关实验(夹持装置已略去)
溶液反应的相关实验(夹持装置已略去) 
 时C中观察到的现象为
时C中观察到的现象为②根据以上现象,该小组同学认为
 与
与 溶液发生氧化还原反应。
溶液发生氧化还原反应。a.写出
 与
与 溶液反应的离子方程式:
溶液反应的离子方程式:b.该小组同学向C试管反应后的溶液中加入硝酸酸化的
 溶液,若出现白色沉淀,即可证明反应生成了
溶液,若出现白色沉淀,即可证明反应生成了 。该做法
。该做法③为了验证
 具有还原性,实验中可以代替
具有还原性,实验中可以代替 溶液的试剂有
溶液的试剂有A.浓硫酸 B.酸性
 溶液 C.碘水 D.NaCl溶液
溶液 C.碘水 D.NaCl溶液(2)某同学利用如图所示的装置研究
 的性质:(熔点:
的性质:(熔点: 为
为 ,
, 为16.8℃,沸点:
为16.8℃,沸点: 为
为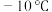 ,
, 为45℃)
为45℃)
 催化氧化的反应,其化学方程式是
催化氧化的反应,其化学方程式是②甲同学按I、Ⅱ、Ⅲ、IV的顺序连接装置,装置Ⅲ中溶液逐渐褪色,生成
 ,同时酸性增强,则该反应的离子方程式是(忽略
,同时酸性增强,则该反应的离子方程式是(忽略 的影响)
的影响)③乙同学按I、Ⅱ、IV顺序连接装置,若装置IV中有
 溶液,反应后增重4.8g,则装置IV中发生反应的化学方程式是
溶液,反应后增重4.8g,则装置IV中发生反应的化学方程式是
您最近一年使用:0次
2024-02-20更新
|
484次组卷
|
4卷引用:广西柳州铁一中学2023-2024学年高一上学期期末考试化学试卷
名校
2 . 空气中主要污染有 、
、 、
、 等,其中
等,其中 是造成酸雨的主要成分。某研究小组对
是造成酸雨的主要成分。某研究小组对 导致酸雨的成因进行探究,用下图装置进行实验。
导致酸雨的成因进行探究,用下图装置进行实验。
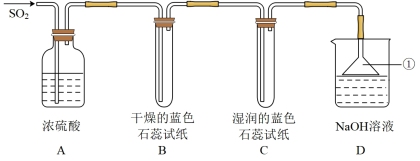
(1)装置A的作用是___________ (填“干燥”或“氧化”)SO2气体。
(2)实验过程中,装置B内干燥的蓝色石蕊试纸的颜色没有发生变化,装置C内湿润的蓝色石蕊试纸变___________ 色,说明 与水反应生成一种酸,该酸的化学式是
与水反应生成一种酸,该酸的化学式是___________ 。
(3)仪器①的名称是___________ ,其倒扣的目的是___________ 。
(4)若通入的 气体中混有少量
气体中混有少量 气体,要完成上述实验,需对该实验装置进行改进的方案是
气体,要完成上述实验,需对该实验装置进行改进的方案是___________ 。
(5)若往盛有水的烧杯中缓慢通入 气体。测得所得溶液的pH
气体。测得所得溶液的pH___________ 7(填“>”或“<”),然后每隔1h测定溶液的pH,发现pH逐渐变小,直至恒定,其原因是___________ (用化学方程式表示)
 、
、 、
、 等,其中
等,其中 是造成酸雨的主要成分。某研究小组对
是造成酸雨的主要成分。某研究小组对 导致酸雨的成因进行探究,用下图装置进行实验。
导致酸雨的成因进行探究,用下图装置进行实验。
(1)装置A的作用是
(2)实验过程中,装置B内干燥的蓝色石蕊试纸的颜色没有发生变化,装置C内湿润的蓝色石蕊试纸变
 与水反应生成一种酸,该酸的化学式是
与水反应生成一种酸,该酸的化学式是(3)仪器①的名称是
(4)若通入的
 气体中混有少量
气体中混有少量 气体,要完成上述实验,需对该实验装置进行改进的方案是
气体,要完成上述实验,需对该实验装置进行改进的方案是(5)若往盛有水的烧杯中缓慢通入
 气体。测得所得溶液的pH
气体。测得所得溶液的pH
您最近一年使用:0次
解题方法
3 . 下图是铜与浓硫酸反应并验证其产物性质的装置图。请回答下列问题。

(1)试管①中发生反应的化学方程式为_______ ;其中硫酸发生了_______ (填“氧化”或“还原”)反应。
(2)一段时间后,④中溶液无明显现象,⑤⑥⑦溶液均褪色,试管⑤⑥⑦中的现象分别说明SO2具有_______ 、_______ 、漂白性。
(3)下列说法正确的是_______ (填字母)。
a.上下移动铜丝可控制反应的发生与停止
b.反应结束后,从导管向装置中鼓入空气,使气体完全被吸收,防止污染
c.实验结束后,试管①中有白色固体出现,为确认白色固体为产物 ,可立刻向试管①中加水,观察颜色
,可立刻向试管①中加水,观察颜色
(4)充分反应后发现,铜丝与硫酸都有剩余,在此情况下,加入下列物质能使溶液中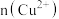 变大的是
变大的是_______ (填字母)。
a. b.
b. c.
c.
(5)反应停止后,待装置冷却,向试管④中加入氯水,产生白色沉淀,反应的离子方程式为___ 。

(1)试管①中发生反应的化学方程式为
(2)一段时间后,④中溶液无明显现象,⑤⑥⑦溶液均褪色,试管⑤⑥⑦中的现象分别说明SO2具有
(3)下列说法正确的是
a.上下移动铜丝可控制反应的发生与停止
b.反应结束后,从导管向装置中鼓入空气,使气体完全被吸收,防止污染
c.实验结束后,试管①中有白色固体出现,为确认白色固体为产物
 ,可立刻向试管①中加水,观察颜色
,可立刻向试管①中加水,观察颜色(4)充分反应后发现,铜丝与硫酸都有剩余,在此情况下,加入下列物质能使溶液中
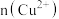 变大的是
变大的是a.
 b.
b. c.
c.
(5)反应停止后,待装置冷却,向试管④中加入氯水,产生白色沉淀,反应的离子方程式为
您最近一年使用:0次
4 . 如图是实验室制取SO2并验证SO2的A.还原性、B.氧化性、C.酸性氧化物的性质、D.漂白性,请选择正确的性质填入横线(用字母填空):

(1)①中的实验表现的是SO2_______ ,
(2)②中的实验表现的是SO2_______ 。
(3)③中的实验表现的是SO2_______ 。
(4)④中的实验表现的是SO2_______ 。
(5)⑤中的实验表现的是SO2_______ 。

(1)①中的实验表现的是SO2
(2)②中的实验表现的是SO2
(3)③中的实验表现的是SO2
(4)④中的实验表现的是SO2
(5)⑤中的实验表现的是SO2
您最近一年使用:0次
解题方法
5 . 某课外小组设计了下图所示的实验装置(图中固定装置已略去),进行SO2性质的研究。
(1)从物质分类的角度,SO2属于____ (填“酸性”或“碱性”)氧化物。
①图中D装置可用来验证SO2具有该性质,其中所加入的试剂是________________ 。
②当向该装置通入SO2时,A中实验现象为_________ ,用化学用语解释其原因___________ 。
(2)从元素化合价的角度分析,SO2具有___ 性。
①当向该装置通入SO2一段时间后,可观察C中实验现象为___ ,说明SO2具有_____ 性。
②如验证SO2还具有另一方面的性质,可选择的药品是___ ,实验现象__________ 。
A.过氧化氢 B.浓硫酸C.氯水 D.硫化钠溶液
(3)B中的品红溶液现象是___________ ,证明SO2具有_________ 性。
(4)多余的SO2一般用氢氧化钠溶液吸收,反应的离子方程式_________________ 。
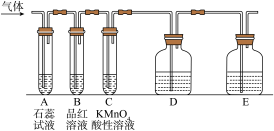
(1)从物质分类的角度,SO2属于
①图中D装置可用来验证SO2具有该性质,其中所加入的试剂是
②当向该装置通入SO2时,A中实验现象为
(2)从元素化合价的角度分析,SO2具有
①当向该装置通入SO2一段时间后,可观察C中实验现象为
②如验证SO2还具有另一方面的性质,可选择的药品是
A.过氧化氢 B.浓硫酸C.氯水 D.硫化钠溶液
(3)B中的品红溶液现象是
(4)多余的SO2一般用氢氧化钠溶液吸收,反应的离子方程式
您最近一年使用:0次
2020-01-17更新
|
134次组卷
|
3卷引用:广西壮族自治区崇左市大新县大新中学2019-2020学年高一上学期期末考试化学试题



