解题方法
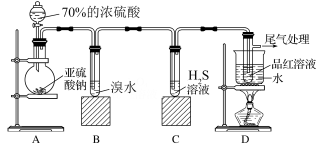
1 . 为探究SO2的性质,某同学按如图所示的装置进行实验。
完成下列填空:
(1)装置A中盛放浓硫酸的仪器名称是________ ,A中发生反应的化学方程式是_______________ 。
(2)实验开始后,装置B中的现象是_____ ,说明SO2具有_______ (填序号);装置C中发生反应的化学方程式是_______________ 说明 SO2具有_______ (填序号)。
a.氧化性 b.还原性 c.漂白性 d.酸性
(3)装置D的目的是探究SO2与品红作用的可逆性,写出实验操作及现象__________ ;尾气可采用_____________ 溶液吸收。

完成下列填空:
(1)装置A中盛放浓硫酸的仪器名称是
(2)实验开始后,装置B中的现象是
a.氧化性 b.还原性 c.漂白性 d.酸性
(3)装置D的目的是探究SO2与品红作用的可逆性,写出实验操作及现象
您最近一年使用:0次
2 . 将SO2和H2S混合,有淡黄色固体出现,该反应中H2S表现出
| A.还原性 | B.漂白性 | C.酸性 | D.氧化性 |
您最近一年使用:0次
2019-10-24更新
|
731次组卷
|
7卷引用:上海市鲁迅中学高三化学练习卷一
上海市鲁迅中学高三化学练习卷一上海市静安区彭浦高级中学2017-2018学年高三上学期期中考试化学试题(人教版2019)必修第二册 模块学业水平合格性测评上海市新场中学2020-2021学年高二下学期期中考试化学试题上海市长征中学2020-2021学年高一下学期期中考试化学试题(已下线)5.1.1硫和二氧化硫-随堂练习(已下线)5.1.1 硫和二氧化硫
名校
解题方法
3 . 实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。

(1)盛装Na2SO3的仪器名称为_______ 。仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成一段液柱,若_______ ,则整个装置气密性良好。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择_______ (填字母)。
a.蒸馏水
b.饱和NaHCO3溶液
c.饱和NaHSO3溶液
d.饱和NaOH溶液
(3)装置C中的试剂可以验证二氧化硫的氧化性,现象为_______ 。
(4)为验证二氧化硫的还原性,充分反应后,取装置D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ :向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案合理的是方案_______ (填“Ⅰ”“Ⅱ”或“Ⅲ”);装置D中发生反应的离子方程式为_______ 。
(5)装置E的作用是_______ ,装置F中为_______ 溶液。

(1)盛装Na2SO3的仪器名称为
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择
a.蒸馏水
b.饱和NaHCO3溶液
c.饱和NaHSO3溶液
d.饱和NaOH溶液
(3)装置C中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取装置D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ :向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案合理的是方案
(5)装置E的作用是
您最近一年使用:0次
2022-08-24更新
|
418次组卷
|
9卷引用:苏教版(2020)高一必修第一册专题4 总结检测
13-14高三上·江西·阶段练习
4 . 二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。探究二氧化硫的制取和性质都有着非常重要的意义。
(1)工业上用黄铁矿(FeS2,其中S元素为-1价)在高温下和氧气反应制备SO2:4FeS2+11O2 2Fe2O3+8SO2。该反应中被氧化的元素是
2Fe2O3+8SO2。该反应中被氧化的元素是______ (填元素符号)。当该反应转移5.50mol电子时,生成的二氧化硫在标准状况下的体积为______ L。
(2)①实验室可用70%的浓硫酸和亚硫酸钠反应制取二氧化硫,如果能控制反应速度,下图中可选用的发生装置是______ (填写字母)。
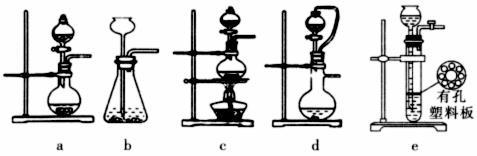
②若用硫酸和亚硫酸钠反应制取3.36L(标准状况)二氧化硫,如果已有25.2%亚硫酸钠(质量分数)被氧化成硫酸钠,则至少需称取该亚硫酸钠______ g(保留一位小数)。
(3)某化学兴趣小组设计用如图装置验证二氧化硫的化学性质。

①能说明二氧化硫具有氧化性的实验现象为______ 。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成
上述方案中合理的是______ (填“Ⅰ”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子方程式为______ 。
(1)工业上用黄铁矿(FeS2,其中S元素为-1价)在高温下和氧气反应制备SO2:4FeS2+11O2
 2Fe2O3+8SO2。该反应中被氧化的元素是
2Fe2O3+8SO2。该反应中被氧化的元素是(2)①实验室可用70%的浓硫酸和亚硫酸钠反应制取二氧化硫,如果能控制反应速度,下图中可选用的发生装置是

②若用硫酸和亚硫酸钠反应制取3.36L(标准状况)二氧化硫,如果已有25.2%亚硫酸钠(质量分数)被氧化成硫酸钠,则至少需称取该亚硫酸钠
(3)某化学兴趣小组设计用如图装置验证二氧化硫的化学性质。

①能说明二氧化硫具有氧化性的实验现象为
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成
上述方案中合理的是
您最近一年使用:0次
13-14高三上·上海虹口·期末
名校
解题方法
5 . 下图所示的是验证二氧化硫性质的微型实验,a、b、c、d是浸有相关溶液的棉球。将浓硫酸滴入装有亚硫酸钠固体的培养皿中。

关于此实验的“现象”“解释或结论”以及对应关系均正确的是( )

关于此实验的“现象”“解释或结论”以及对应关系均正确的是( )
| 选项 | 现象 | 解释或结论 |
| A | a处黄色褪去 | 非金属性:Br>S |
| B | b处变为红色 | 二氧化硫与水反应生成酸性物质 |
| C | c处变为蓝色 | 二氧化硫具有一定的氧化性 |
| D | d处红色先褪去后恢复 | 二氧化硫具有漂白性且漂白性不稳定 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2014-04-28更新
|
1615次组卷
|
8卷引用:2013届上海市虹口区高三上学期期末教学质量调研化学试卷
(已下线)2013届上海市虹口区高三上学期期末教学质量调研化学试卷(已下线)2014高考名师推荐化学氧、硫及其化合物主要性质(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第3讲 硫及其化合物【押题专练】(已下线)2018年12月2日 《每日一题》人教必修1- 每周一测【全国百强校】山西省大同市第一中学2018-2019学年高一上学期期末考试化学试题(已下线)2019年12月1日《每日一题》人教版(必修1)—— 每周一测(已下线)上海市虹口区2013年高考一模化学试题(已下线)课后-5.1.1 硫和二氧化硫-人教2019必修第二册
6 . 下列含硫化合物中,硫元素既有氧化性又有还原性的是
| A.S | B.H2S | C.Na2SO3 | D.SO3 |
您最近一年使用:0次



