1 . 下列关于硅酸的说法正确的是
| A.硅酸可以通过SiO2和水的化合反应制得 |
| B.用反应Na2SiO3+2HCl===H2SiO3(胶体)+2NaCl制取硅酸是利用了可溶性酸制难溶性酸的原理 |
| C.硅酸难溶于水,不能与NaOH溶液反应 |
| D.硅胶可用作袋装食品的干燥剂 |
您最近一年使用:0次
名校
解题方法
2 . 下列说法正确的是
| A.硅胶作袋装食品的干燥剂的过程中没有发生化学变化 |
B.pH=2的溶液中可能大量存在Na+、NH 、 SiO 、 SiO |
| C.2HCl+Na2SiO3=H2SiO3↓+2NaCl说明Cl的非金属性强于Si |
D.向Na2SiO3溶液中通入过量SO2的离子方程式:SiO +SO2+H2O= H2SiO3↓ +SO +SO2+H2O= H2SiO3↓ +SO |
您最近一年使用:0次
3 . 化学与生活、生产密切相关,下列说法正确的是( )
| A.月饼因富含油脂而易被氧化,保存时常放入装有硅胶的透气袋 |
| B.离子交换膜在工业上应用广泛,在氯碱工业中使用阴离子交换膜 |
| C.钢铁在潮湿的空气中,易发生化学腐蚀生锈 |
| D.《本草经集注》中关于鉴别硝石(KNO3)和朴硝(Na2SO4)的记载:“以火烧之,紫青烟起,乃真硝石也”,该方法应用了焰色反应 |
您最近一年使用:0次
名校
4 . 下列说法中正确的是
| A.Al、SiO2、Ca(OH)2、NaHCO3等既能与盐酸反应,又能与氢氧化钠溶液反应 |
B.若a、b、c分别为Si、SiO2、H2SiO3,则可以通过一步反应实现如图所示的转化关系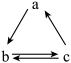 |
C.Fe2O3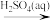 Fe2(SO4)3(aq) Fe2(SO4)3(aq) 无水Fe2(SO4)3 无水Fe2(SO4)3 |
D.Na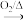 Na2O2 Na2O2 NaI NaI |
您最近一年使用:0次
解题方法
5 . 在Na+浓度为0.5 mol·L-1的某澄清溶液中,还可能还有K+、Ag+、Ca2+、Ba2+、NO3-、CO32-、SiO32-、SO42-中的若干种,现取该溶液100mL进行如下实验
已知:H2SiO3为不容水的胶状沉淀,加热时易分解为两种物质
请回答下列问题:
(1)实验Ⅰ能确定一定存在的离子是______________ ;一定不存在的离子是____________ 。
(2)实验Ⅱ中沉淀洗涤、灼烧至恒重,所涉及的化学方程式为____________________ ;
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,求K+的最小浓度_______________ 。
已知:H2SiO3为不容水的胶状沉淀,加热时易分解为两种物质
| 序号 | 实验内容 | 实验结果 |
| Ⅰ | 向该溶液中加入足量稀盐酸 | 生成白色胶状沉淀并放出标况下0.56L气体 |
| Ⅱ | 将Ⅰ中产生的混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4g |
| Ⅲ | 向Ⅱ的滤液中滴加BaCl2溶液 | 无明显现象 |
(1)实验Ⅰ能确定一定存在的离子是
(2)实验Ⅱ中沉淀洗涤、灼烧至恒重,所涉及的化学方程式为
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,求K+的最小浓度
您最近一年使用:0次
6 . 下列关于硅酸的说法正确的是
| A.硅酸可以通过SiO2和水的化合反应制得 |
| B.用反应Na2SiO3+2HCl===2NaCl+H2SiO3(胶体)制取硅酸是利用了可溶性酸制难溶性酸的原理 |
| C.硅酸难溶于水,不能与NaOH溶液反应 |
| D.硅胶可用作袋装食品的干燥剂 |
您最近一年使用:0次
19-20高二·浙江·期末
解题方法
7 . 下列说法或做法正确的是
A. 通入硅酸钠中析出硅酸沉淀,所以硅酸的酸性小于碳酸 通入硅酸钠中析出硅酸沉淀,所以硅酸的酸性小于碳酸 |
| B.金属钠着火燃烧时,用泡沫灭火器灭火 |
| C.铁比较活泼,所以不能用铁罐运输浓硫酸 |
| D.正常雨水pH等于7,酸雨的pH小于7 |
您最近一年使用:0次
8 . 已知A是灰黑色的硬而脆的固体,B是气态物质,A~E各种物质的相互转化关系如下图所示。
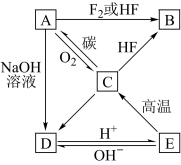
(1)写出B、D、E三种物质的化学式: B______ ,D_______ ,E________ ;
(2)画出A的原子结构示意图__________ ;
(3)写出C→A的化学方程式___________ 。

(1)写出B、D、E三种物质的化学式: B
(2)画出A的原子结构示意图
(3)写出C→A的化学方程式
您最近一年使用:0次
9 . 现有如下仪器,仪器中已注入溶液,回答下列问题。
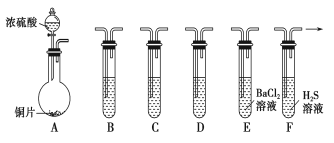
(1)加热装置A,写出铜与浓硫酸反应的化学方程式:_______________________________
(2)验证碳、硅非金属性的相对强弱(已知酸性:H2SO3>H2CO3),若选择仪器A、B、C、D并相连接,则B、C、D中所选择的试剂为B________ 、C________ 、D________ 。能说明碳的非金属性比硅强的实验现象是_________________ 。
(3)验证SO2的氧化性、还原性。若选择A、E、F仪器,并按A、E、F顺序连接。
①则证明SO2有氧化性的实验现象是________________ ,反应方程式为________________ 。
②若证明SO2具有还原性,在E中采取的实验操作为_________________________________ ,
其实验现象为__________________ ,反应原理为__________________ (用离子方程式表示)。

(1)加热装置A,写出铜与浓硫酸反应的化学方程式:
(2)验证碳、硅非金属性的相对强弱(已知酸性:H2SO3>H2CO3),若选择仪器A、B、C、D并相连接,则B、C、D中所选择的试剂为B
(3)验证SO2的氧化性、还原性。若选择A、E、F仪器,并按A、E、F顺序连接。
①则证明SO2有氧化性的实验现象是
②若证明SO2具有还原性,在E中采取的实验操作为
其实验现象为
您最近一年使用:0次
名校
解题方法
10 . 下列实验操作能达到实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 向硅酸钠溶液中通入 气体,有白色沉淀产生 气体,有白色沉淀产生 | 验证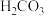 的酸性强于 的酸性强于 |
| B | 将 通入滴有酚酞的NaOH溶液中,溶液红色褪去 通入滴有酚酞的NaOH溶液中,溶液红色褪去 | 证明 的漂白性 的漂白性 |
| C | 将海带灰溶于水,过滤,向滤液中滴加淀粉溶液 | 检测海带中含有碘元素 |
| D | 向市售乙醇中加入一小粒钠,有气泡产生 | 检测市售乙醇中存在水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



