名校
1 . 下列实验操作能达到实验目的的是
| 实验目的 | 实验操作 | |
| A | 制备SO2 | 常温下将铁丝插入浓硫酸中 |
| B | 防止白磷自燃 | 实验结束,将剩余白磷固体放回原试剂瓶 |
| C | 测定新制氯水的pH值 | 用洁净的玻璃棒蘸取少许新制氯水滴在pH试纸上 |
| D | 除去混在铜粉中的镁粉和铝粉 | 加硝酸后过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 根据实验操作及现象,下列结论正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向 溶液中滴加KSCN溶液,溶液变红,再加入少量KCl固体,溶液颜色无明显变化 溶液中滴加KSCN溶液,溶液变红,再加入少量KCl固体,溶液颜色无明显变化 |  与 与 的反应不可逆 的反应不可逆 |
| B | 两支试管各盛 酸性高锰酸钾溶液,分别加入 酸性高锰酸钾溶液,分别加入 草酸溶液和 草酸溶液和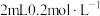 草酸溶液,观察溶液颜色变化 草酸溶液,观察溶液颜色变化 | 其他条件相同,反应物浓度越大,反应速率越快 |
| C | 加热足量的锌与少量浓硫酸的混合物,有大量气体产生 | 气体一定为 |
| D | 向2mL浓度均为 的KCl、KI混合溶液中滴加2滴 的KCl、KI混合溶液中滴加2滴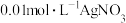 溶液,振荡,产生黄色沉淀 溶液,振荡,产生黄色沉淀 | 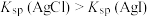 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 铁、铝在生产生活中有广泛的应用。完成下列填空:
(1)铝用作电线是利用了铝的___________ 性;铁用作炊具是利用了铁的___________ 性。
(2)常温下由于浓硫酸能使铁___________ ,因此浓硫酸可用铁槽车运输。
(3)铁器时代标志着较高水平的生产力发展,铁及其化合物被广泛应用于我们的生活中。学生甲学了有关铁的内容后非常感兴趣,他选择①使用铁粉与硫粉混合在空气中加热;②铁粉与CuSO4溶液反应将0价铁转化成+2价铁的化合物,写出这两种途径的化学方程式:①___________ ;②___________ 。
(1)铝用作电线是利用了铝的
(2)常温下由于浓硫酸能使铁
(3)铁器时代标志着较高水平的生产力发展,铁及其化合物被广泛应用于我们的生活中。学生甲学了有关铁的内容后非常感兴趣,他选择①使用铁粉与硫粉混合在空气中加热;②铁粉与CuSO4溶液反应将0价铁转化成+2价铁的化合物,写出这两种途径的化学方程式:①
您最近一年使用:0次
2022高一·上海·专题练习
解题方法
4 . 下列关于金属的叙述正确的是
| A.金属都是银白色的固体,都具有较高的硬度和密度 |
| B.金属在化合物中一定显正化合价 |
| C.金属单质都可以和酸发生置换反应产生氢气 |
| D.金属元素的单质在常温下均为固体 |
您最近一年使用:0次
2021高三·全国·专题练习
5 . 高纯硫酸锰在电池材料领域有重要用途。以软锰矿(主要成分为 ,含有少量铁和铝的氧化物)、硫铁矿(主要成分为
,含有少量铁和铝的氧化物)、硫铁矿(主要成分为 )、钛白废酸(主要成分为
)、钛白废酸(主要成分为 )为原料制备
)为原料制备 的工艺流程如图:
的工艺流程如图:

某工厂用10t软锰矿(含87% )制备
)制备 ,最终得到
,最终得到 13.52t,则
13.52t,则 的产率为
的产率为_______ 。
 ,含有少量铁和铝的氧化物)、硫铁矿(主要成分为
,含有少量铁和铝的氧化物)、硫铁矿(主要成分为 )、钛白废酸(主要成分为
)、钛白废酸(主要成分为 )为原料制备
)为原料制备 的工艺流程如图:
的工艺流程如图:
某工厂用10t软锰矿(含87%
 )制备
)制备 ,最终得到
,最终得到 13.52t,则
13.52t,则 的产率为
的产率为
您最近一年使用:0次
6 . 下列各组物质用稀硫酸不能完全区分开的是
| A.镁粉、氧化铜粉、木炭粉 | B.NaOH溶液、Ba(OH)2溶液、KOH溶液 |
| C.Na2CO3溶液、NaCl溶液、BaCl2溶液 | D.铝片、铁片、银片 |
您最近一年使用:0次
解题方法
7 . 将 锌粉与少量浓硫酸在加热条件下充分反应,共收集到混合气体
锌粉与少量浓硫酸在加热条件下充分反应,共收集到混合气体 (标准状况),则剩余锌粉的质量为( )
(标准状况),则剩余锌粉的质量为( )
 锌粉与少量浓硫酸在加热条件下充分反应,共收集到混合气体
锌粉与少量浓硫酸在加热条件下充分反应,共收集到混合气体 (标准状况),则剩余锌粉的质量为( )
(标准状况),则剩余锌粉的质量为( )A. | B. | C. | D.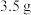 |
您最近一年使用:0次
2020-09-10更新
|
418次组卷
|
3卷引用:苏教版(2020)高一必修第一册专题4 总结检测
名校
解题方法
8 . 归纳与推理是化学学习常用的方法。下列推理正确的是
| A.因为稀硫酸能与铁反应放出H2,所以稀硝酸与铁反应也一定能放出H2 |
| B.因为Na可以与水反应放出H2,所以K也可以与水反应放出H2 |
| C.因为Na失一个电子显强还原性,所以Al失三个电子显更强还原性 |
| D.因为硅酸酸性比碳酸弱,所以SiO2一定不能跟Na2CO3反应 |
您最近一年使用:0次
19-20高二·浙江·期末
名校
9 . 下列有关H2SO4的叙述正确的是( )
| A.浓H2SO4与铜片共热的反应中,浓H2SO4既表现出强氧化性,又表现出酸性 |
| B.浓H2SO4与金属活动性顺序中氢后面的金属反应生成的气体一般为SO2,与氢前面的金属反应生成的气体一般为H2 |
| C.常温下,铁或铝不与浓H2SO4反应,所以可用铁或铝制的容器贮存浓H2SO4 |
| D.浓H2SO4是不挥发性强酸,氢硫酸是挥发性弱酸,所以可用浓H2SO4与FeS反应制取H2S气体 |
您最近一年使用:0次
2020-08-14更新
|
459次组卷
|
8卷引用:【新东方】2020-80.
(已下线)【新东方】2020-80.(已下线)4.1.2 硫酸的工业制备 浓硫酸的性质练习(1)——《高中新教材同步备课》(苏教版 必修第一册)福建省漳州市平和县第一中学2021届高三上学期期中考试化学试题(已下线)5.1.2 硫酸(练好题)(能力提升)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)(已下线)4.1.2 硫酸的工业制备 浓硫酸的性质(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)云南省玉溪市峨山彝族自治县第一中学2021-2022学年高一下学期3月月考化学试题(已下线)3.1.2 浓硫酸和硫酸盐-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)陕西省西安市雁塔区第二中学2021-2022学年高一下学期第一次月考化学试题
10 . 根据下列实验操作和现象,所得结论正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 将两根打磨光亮的镁条分别插入硫酸铜溶液和硝酸银溶液 | 两根镁条上均有固体附着 | 金属的活动性顺序为Mg>Cu>Ag |
| B | 将KSCN溶液滴入盛有无色溶液的试管中 | 溶液变为血红色 | 溶液中含有Fe3+ |
| C | 将铝片插入盛有浓硫酸的试管中 | 无明显现象 | 铝与浓硫酸不反应 |
| D | 将混有乙烯的甲烷气体通入到酸性KMnO4溶液中 | 紫红色溶液褪色 | 甲烷与酸性KMnO4溶液发生了反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



