1 . 实验小组研究SO2与Na2O2的反应。
(1)实验前分析物质的化学性质,提出假设:
假设1:SO2和CO2都是酸性氧化物。类比CO2与Na2O2的反应可知,SO2与Na2O2反应生成Na2SO3和O2;
假设2:SO2具有_______ 性,SO2与Na2O2反应生成Na2SO4。
(2)用如图所示装置进行SO2与Na2O2反应的实验。实验过程中,观察到C中淡黄色粉末逐渐变为白色,用带火星的木条靠近D中导气管口,木条复燃。

①A中反应产生SO2的化学方程式是_______ 。
②B中的试剂为_______ ,其主要作用是_______ 。
③实验证明假设_______ 正确。
(3)为检验C中是否有Na2SO4生成,设计如下方案:取少量C中反应后的白色固体溶解于水,加入BaCl2溶液,产生白色沉淀,再加入足量的稀HNO3,仍有白色沉淀不溶解,证明有Na2SO4生成。该方案是否合理?_______ (填“合理”或“不合理”)。请简要说明理由:_______ 。
(4)进一步实验证明C中反应后的固体中既有Na2SO3又有Na2SO4.从氧化还原反应的角度分析,+4价硫元素能被氧化为+6价。在上述实验条件下,+4价硫元素未完全转化为+6价,可见化学反应实际进行的情况与反应的_______ (只写一条)有关。
(1)实验前分析物质的化学性质,提出假设:
假设1:SO2和CO2都是酸性氧化物。类比CO2与Na2O2的反应可知,SO2与Na2O2反应生成Na2SO3和O2;
假设2:SO2具有
(2)用如图所示装置进行SO2与Na2O2反应的实验。实验过程中,观察到C中淡黄色粉末逐渐变为白色,用带火星的木条靠近D中导气管口,木条复燃。

①A中反应产生SO2的化学方程式是
②B中的试剂为
③实验证明假设
(3)为检验C中是否有Na2SO4生成,设计如下方案:取少量C中反应后的白色固体溶解于水,加入BaCl2溶液,产生白色沉淀,再加入足量的稀HNO3,仍有白色沉淀不溶解,证明有Na2SO4生成。该方案是否合理?
(4)进一步实验证明C中反应后的固体中既有Na2SO3又有Na2SO4.从氧化还原反应的角度分析,+4价硫元素能被氧化为+6价。在上述实验条件下,+4价硫元素未完全转化为+6价,可见化学反应实际进行的情况与反应的
您最近一年使用:0次
2 . 下列现象或事实的叙述及解释均正确的是
| 选项 | 现象或事实 | 解释 |
| A |  固体加入紫色石蕊溶液,先变蓝,后褪色 固体加入紫色石蕊溶液,先变蓝,后褪色 | 先变蓝是因为有碱性物质生成,后褪色是因为 有氧化性 有氧化性 |
| B | 漂白粉中滴加浓盐酸会增强漂白性 | 漂白粉中的 与 与 反应生成 反应生成 的原因 的原因 |
| C | 让光束通过 胶体时,可以看到一条光亮的通路 胶体时,可以看到一条光亮的通路 | 丁达尔效应是胶体和溶液的本质区别 |
| D |  可与 可与 反应制取单质 反应制取单质 |  有还原性,能把 有还原性,能把 置换出来 置换出来 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 某些资料认为NO、NO2不能与Na2O2反应。南开中学化学学习小组提出质疑,他们分析过氧化钠和二氧化氮都有氧化性,根据化合价升降原则提出假设:
假设I:过氧化钠氧化二氧化氮,生成NaNO3;
假设II:二氧化氮氧化过氧化钠,生成O2。
(1)小组甲同学设计实验如下:
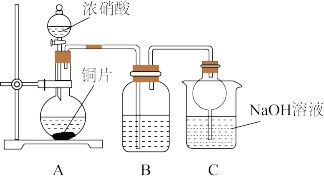
①试管A中反应的化学方程式是__________ 。
②待试管B中收集满气体,向试管B中加入适量Na2O2,塞紧塞子,振荡试管,观察到红棕色气体迅速消失;再将带火星木条迅速伸进试管内,木条复燃。甲同学认为假设II正确;乙同学认为该装置不能达到实验目的,为达到实验目的,应在A、B之间增加一个浓硫酸洗气装置,该装置的作用是_______ 。
③乙同学用改进后装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;带火星木条未复燃。得出结论:假设I正确。NO2和Na2O2反应的方程式是________ 。
(2)丙同学认为NO易与O2发生反应,应更易被Na2O2氧化。
查阅资料:①2NO+Na2O2=2NaNO2
②亚硝酸盐在酸性条件下不稳定:2H++3 =
= +2NO↑+H2O。
+2NO↑+H2O。
丙同学用下图所示装置(部分夹持装置略)探究NO与Na2O2的反应。
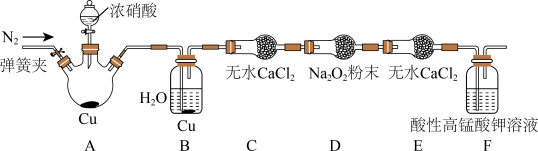
①在反应前,打开弹簧夹,通入一段时间N2,目的是_________ 。
②充分反应后,取D装置中产物少许,加入稀盐酸,若观察到________ 现象,则产物是亚硝酸钠。
③F装置的作用是________ 。该装置中发生反应的离子方程式为_________ 。
假设I:过氧化钠氧化二氧化氮,生成NaNO3;
假设II:二氧化氮氧化过氧化钠,生成O2。
(1)小组甲同学设计实验如下:

①试管A中反应的化学方程式是
②待试管B中收集满气体,向试管B中加入适量Na2O2,塞紧塞子,振荡试管,观察到红棕色气体迅速消失;再将带火星木条迅速伸进试管内,木条复燃。甲同学认为假设II正确;乙同学认为该装置不能达到实验目的,为达到实验目的,应在A、B之间增加一个浓硫酸洗气装置,该装置的作用是
③乙同学用改进后装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;带火星木条未复燃。得出结论:假设I正确。NO2和Na2O2反应的方程式是
(2)丙同学认为NO易与O2发生反应,应更易被Na2O2氧化。
查阅资料:①2NO+Na2O2=2NaNO2
②亚硝酸盐在酸性条件下不稳定:2H++3
 =
= +2NO↑+H2O。
+2NO↑+H2O。丙同学用下图所示装置(部分夹持装置略)探究NO与Na2O2的反应。

①在反应前,打开弹簧夹,通入一段时间N2,目的是
②充分反应后,取D装置中产物少许,加入稀盐酸,若观察到
③F装置的作用是
您最近一年使用:0次



