1 . 为探究某食品包装袋内一小包脱氧剂中的还原铁粉是否变质,分别取少量样品溶于盐酸,再进行下列实验,其中说法正确的是
| A.若滴加KSCN溶液,溶液变红,说明铁粉变质 |
| B.若滴加KSCN溶液,溶液未变红,说明铁粉未变质 |
| C.若依次滴加氯水、KSCN溶液,溶液变红,说明铁粉全部变质 |
| D.若溶于盐酸未观察到有气泡且滴加KSCN溶液后溶液未变红,说明铁粉未变质 |
您最近一年使用:0次
名校
2 . 下列实验操作、现象和结论正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 将Fe(NO3)2样品溶于稀硫酸,滴加KSCN溶液 | 溶液变红 | Fe(NO3)2样品已变质 |
| B | 向稀硫酸中加入铜片,然后通入O2加热 | 先无明显现象,通入O2加热后变蓝 | 氧化性:稀硫酸>Cu2+ |
| C | 向稀硫酸酸化的H2O2溶液中滴入FeCl2溶液 | 溶液变黄色 | 氧化性:H2O2>Fe3+ |
| D | 溶有SO2的BaCl2溶液中通入气体 | 有白色沉淀生成 | X一定是Cl2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 一定条件下,铁与空气接触时表面会形成氧化物,如一块低碳钢可以被三种氧化物膜所覆盖:与金属接触的一侧是FeO,中间是 ,与空气接触的一侧则是
,与空气接触的一侧则是 。回答下列问题:
。回答下列问题:
(1) 是磁铁矿的主要成分,也是中国古代“四大发明”之一“司南”的指针材料。用Al粉和
是磁铁矿的主要成分,也是中国古代“四大发明”之一“司南”的指针材料。用Al粉和 反应焊接钢轨的化学方程式为
反应焊接钢轨的化学方程式为_______ 。
(2)FeO可以合成补铁剂 。欲验证
。欲验证 超过保质期后已变质,可进行的操作是:取定量样品加水溶解静置、取少许溶液于试管中,向其中加入
超过保质期后已变质,可进行的操作是:取定量样品加水溶解静置、取少许溶液于试管中,向其中加入_______ 溶液(填试剂名称),若液体出现红色,则证明该药物已变质。
(3)某实验小组设计了如下实验步骤,利用部分变质的废弃 溶液制备
溶液制备 。
。

框图中热空气的作用为_______ ,写出a→b的离子方程式_______ ,写出 的一种用途:
的一种用途:_______ 。
 ,与空气接触的一侧则是
,与空气接触的一侧则是 。回答下列问题:
。回答下列问题:(1)
 是磁铁矿的主要成分,也是中国古代“四大发明”之一“司南”的指针材料。用Al粉和
是磁铁矿的主要成分,也是中国古代“四大发明”之一“司南”的指针材料。用Al粉和 反应焊接钢轨的化学方程式为
反应焊接钢轨的化学方程式为(2)FeO可以合成补铁剂
 。欲验证
。欲验证 超过保质期后已变质,可进行的操作是:取定量样品加水溶解静置、取少许溶液于试管中,向其中加入
超过保质期后已变质,可进行的操作是:取定量样品加水溶解静置、取少许溶液于试管中,向其中加入(3)某实验小组设计了如下实验步骤,利用部分变质的废弃
 溶液制备
溶液制备 。
。
框图中热空气的作用为
 的一种用途:
的一种用途:
您最近一年使用:0次
14-15高一上·山东潍坊·期末
名校
解题方法
4 . 铁是人体不可缺少的微量元素,硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
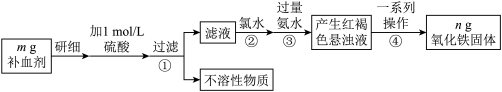
(1)实验中用已经准确量取的浓硫酸配制500 mL 1 mol/L的硫酸溶液,则配制时用到的仪器除烧杯、500 mL容量瓶外,还需要____________________ 。
(2)步骤②加入过量氯水后发生反应的离子方程式为_________________________ 。
(3)步骤④中一系列操作步骤为_________ 、洗涤、灼烧、冷却、称量。
(4)若实验无损耗,则该补血剂含铁元素的质量分数为____________ 。
(5)某同学发现部分补血剂药片表面发黄,取样品研细,溶于1 mol/L的硫酸溶液,过滤。取滤液加_______________ 溶液,溶液变红说明该补血剂已部分变质。向变色后的溶液中加入橙汁,溶液红色褪去,说明橙汁含具有___________ 性(填“氧化”或“还原”)的物质。
(6)下列检验(5)中滤液中是否有Fe2+应选用的试剂是________ 。
A. KSCN溶液 B. 酸性KMnO4溶液 C. 铁粉 D. FeCl3溶液

(1)实验中用已经准确量取的浓硫酸配制500 mL 1 mol/L的硫酸溶液,则配制时用到的仪器除烧杯、500 mL容量瓶外,还需要
(2)步骤②加入过量氯水后发生反应的离子方程式为
(3)步骤④中一系列操作步骤为
(4)若实验无损耗,则该补血剂含铁元素的质量分数为
(5)某同学发现部分补血剂药片表面发黄,取样品研细,溶于1 mol/L的硫酸溶液,过滤。取滤液加
(6)下列检验(5)中滤液中是否有Fe2+应选用的试剂是
A. KSCN溶液 B. 酸性KMnO4溶液 C. 铁粉 D. FeCl3溶液
您最近一年使用:0次



