14-15高二上·上海宝山·期中
名校
解题方法
1 . 氧化铁俗称铁红,可用于水泥制件、橡胶制品、塑料制品的着色,在工业上有广泛的用途,某工厂采用生产钦白粉的下脚料(含大量FeSO4的废液)为原料来制备氧化铁。

已知煅烧过程中的化学反应方程式为:FeCO3 FeO+CO2↑,4FeO+O2
FeO+CO2↑,4FeO+O2 2Fe2O3
2Fe2O3
(1)用98%的H2SO4配制20%的H2SO4,所需玻璃仪器除量筒外还有( ) 。
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
(2)向下脚料废液中加入铁皮的作用是(用有关的离子方程式表示)_____ 。
(3)加入20%H2SO4的作用是_________________ 。
(4)浓缩结晶后得到的晶体是_____________ (填化学式),A中所含的离子除H+、OH-、NH4+外,还含有大量的___________ ,检验该离子的方法是_____________________ 。
(5)写出步骤“合成”中发生的化学变化(用化学方程式表示)_____ 。

已知煅烧过程中的化学反应方程式为:FeCO3
 FeO+CO2↑,4FeO+O2
FeO+CO2↑,4FeO+O2 2Fe2O3
2Fe2O3(1)用98%的H2SO4配制20%的H2SO4,所需玻璃仪器除量筒外还有
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
(2)向下脚料废液中加入铁皮的作用是(用有关的离子方程式表示)
(3)加入20%H2SO4的作用是
(4)浓缩结晶后得到的晶体是
(5)写出步骤“合成”中发生的化学变化(用化学方程式表示)
您最近一年使用:0次
名校
2 . 铁的化合物有广泛用途,如碳酸亚铁(FeCO3)可作为补血剂,铁红(Fe2O3)可作为颜料。利用某硫酸厂产生的烧渣(主要含FeCO3、FeO,还有一定量的SiO2)制备碳酸亚铁的流程如图:
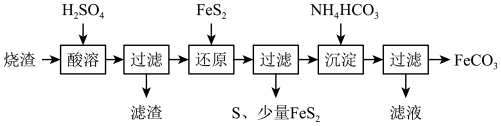
(1)“酸溶”时加快反应速率的方法有____ (写出一种)。
(2)①“还原”时,FeS2与H2SO4不反应,Fe3+通过两个反应被还原,其中一个反应如下:FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+,则另一个反应的离子方程式为:___ 。
②FeS2还原后,检验Fe3+是否反应完全的方法是___ 。
(3)①“沉淀”时,需控制pH不宜过高,否则生成的FeCO3中可能混有___ 杂质;
②能否将NH4HCO3换成(NH4)2CO3___ 。
(4)FeCO3浊液长时间暴露在空气中,会有部分固体表面变为红褐色,同时释放出CO2,则与FeCO3反应的物质为___ (填化学式)。
(5)FeCO3在空气中煅烧生成Fe2O3时,也会生成FeO。现煅烧34.8g的FeCO3,得到Fe2O3和FeO的混合物23.76g,则Fe2O3的质量为___ g。

(1)“酸溶”时加快反应速率的方法有
(2)①“还原”时,FeS2与H2SO4不反应,Fe3+通过两个反应被还原,其中一个反应如下:FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+,则另一个反应的离子方程式为:
②FeS2还原后,检验Fe3+是否反应完全的方法是
(3)①“沉淀”时,需控制pH不宜过高,否则生成的FeCO3中可能混有
②能否将NH4HCO3换成(NH4)2CO3
(4)FeCO3浊液长时间暴露在空气中,会有部分固体表面变为红褐色,同时释放出CO2,则与FeCO3反应的物质为
(5)FeCO3在空气中煅烧生成Fe2O3时,也会生成FeO。现煅烧34.8g的FeCO3,得到Fe2O3和FeO的混合物23.76g,则Fe2O3的质量为
您最近一年使用:0次



