名校
解题方法
1 . 铁是人类较早使用的金属之一,运用所学知识,回答下列问题。
I.某学习小组研究 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
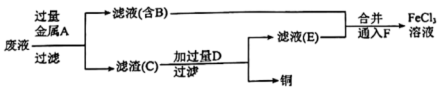
(1)滤渣C中所含物质的化学式为___________ ;通入F发生反应的离子方程式为___________ 。
(2)滤渣C与试剂D反应的离子方程式为_______ ,为测定滤渣中铜的质量分数,取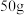 的滤渣与足量的试剂D反应,得到
的滤渣与足量的试剂D反应,得到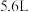 气体(标准状况下),试计算滤渣中铜的质量分数
气体(标准状况下),试计算滤渣中铜的质量分数______ 。
Ⅱ.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验
请回答:
(3)实验I中反应的化学方程式是___________ 。
(4)甲同学观察到实验Ⅰ中持续产生肥皂泡,但实验Ⅱ中溶液B未呈现红色,则溶液B未呈现红色的原因是___________ 。(写出反应的离子方程式)
(5)实验室在制备 时必须隔绝空气,否则发生的现象是
时必须隔绝空气,否则发生的现象是___________ ;反应化学方程式为___________ 。
I.某学习小组研究
 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
(1)滤渣C中所含物质的化学式为
(2)滤渣C与试剂D反应的离子方程式为
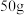 的滤渣与足量的试剂D反应,得到
的滤渣与足量的试剂D反应,得到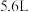 气体(标准状况下),试计算滤渣中铜的质量分数
气体(标准状况下),试计算滤渣中铜的质量分数Ⅱ.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验
| 实验I | 实验Ⅱ |
 | 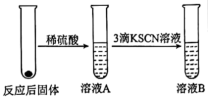 |
(3)实验I中反应的化学方程式是
(4)甲同学观察到实验Ⅰ中持续产生肥皂泡,但实验Ⅱ中溶液B未呈现红色,则溶液B未呈现红色的原因是
(5)实验室在制备
 时必须隔绝空气,否则发生的现象是
时必须隔绝空气,否则发生的现象是
您最近一年使用:0次
名校
解题方法
2 . 5.76g某部分氧化的Fe、Cu合金样品(氧化产物为 、CuO),经如下处理,下列说法正确的是
、CuO),经如下处理,下列说法正确的是

 、CuO),经如下处理,下列说法正确的是
、CuO),经如下处理,下列说法正确的是
| A.V=448 |
| B.样品中Fe元素的质量为2.14g |
| C.未氧化前Fe元素的质量分数约为38.89% |
| D.样品中CuO的质量为3.52g |
您最近一年使用:0次
3 . 以铁屑(表面含少量 )为原料先制备
)为原料先制备 ,再通过灼烧、还原制备高纯度还原铁粉的工艺流程如下:
,再通过灼烧、还原制备高纯度还原铁粉的工艺流程如下:

(1)酸溶。将铁屑溶于足量的稀 中过滤所得溶液经检验不含
中过滤所得溶液经检验不含 。
。
①检验酸溶后的溶液是否含 的实验操作是
的实验操作是_______ 。
②滤液中不存在 的原因是
的原因是_______ 。
(2)沉淀、过滤。向酸溶后的溶液中滴加稍过量的 ,过滤得
,过滤得 。
。
①沉淀反应的离子方程式为_______ 。
②沉淀中 含量的测定:准确称取6.300g沉淀,加入适量蒸馏水和稀硫酸溶解、酸化,并转移入250mL容量瓶中定容,取25.00mL溶液,向其中滴加
含量的测定:准确称取6.300g沉淀,加入适量蒸馏水和稀硫酸溶解、酸化,并转移入250mL容量瓶中定容,取25.00mL溶液,向其中滴加
 溶液,完全反应时,消耗
溶液,完全反应时,消耗 溶液20.00mL。
溶液20.00mL。
过程中发生的反应为: (未配平,假设杂质不参与反应)。计算沉淀中
(未配平,假设杂质不参与反应)。计算沉淀中 (相对分子质量为180)的质量分数
(相对分子质量为180)的质量分数_______ (写出计算过程)。
(3)灼烧。在氧气流中灼烧 得
得 、
、 。
。
①灼烧时发生反应的化学方程式为_______ 。
②研究发现, 也可以灼烧得到
也可以灼烧得到 ,但灼烧
,但灼烧 得到的
得到的 比灼烧
比灼烧 得到的
得到的 更容易被还原,可能的原因是
更容易被还原,可能的原因是_______ 。
(4)还原。为制得高纯度的还原铁粉,以下还原剂最合适的是_______ 。
A.碳粉 B.铝粉 C.氢气
 )为原料先制备
)为原料先制备 ,再通过灼烧、还原制备高纯度还原铁粉的工艺流程如下:
,再通过灼烧、还原制备高纯度还原铁粉的工艺流程如下:
(1)酸溶。将铁屑溶于足量的稀
 中过滤所得溶液经检验不含
中过滤所得溶液经检验不含 。
。①检验酸溶后的溶液是否含
 的实验操作是
的实验操作是②滤液中不存在
 的原因是
的原因是(2)沉淀、过滤。向酸溶后的溶液中滴加稍过量的
 ,过滤得
,过滤得 。
。①沉淀反应的离子方程式为
②沉淀中
 含量的测定:准确称取6.300g沉淀,加入适量蒸馏水和稀硫酸溶解、酸化,并转移入250mL容量瓶中定容,取25.00mL溶液,向其中滴加
含量的测定:准确称取6.300g沉淀,加入适量蒸馏水和稀硫酸溶解、酸化,并转移入250mL容量瓶中定容,取25.00mL溶液,向其中滴加
 溶液,完全反应时,消耗
溶液,完全反应时,消耗 溶液20.00mL。
溶液20.00mL。过程中发生的反应为:
 (未配平,假设杂质不参与反应)。计算沉淀中
(未配平,假设杂质不参与反应)。计算沉淀中 (相对分子质量为180)的质量分数
(相对分子质量为180)的质量分数(3)灼烧。在氧气流中灼烧
 得
得 、
、 。
。①灼烧时发生反应的化学方程式为
②研究发现,
 也可以灼烧得到
也可以灼烧得到 ,但灼烧
,但灼烧 得到的
得到的 比灼烧
比灼烧 得到的
得到的 更容易被还原,可能的原因是
更容易被还原,可能的原因是(4)还原。为制得高纯度的还原铁粉,以下还原剂最合适的是
A.碳粉 B.铝粉 C.氢气
您最近一年使用:0次
2022-08-29更新
|
647次组卷
|
3卷引用:17 2024年苏州昆山周市高级中学高一3月月考
名校
解题方法
4 . 工业废水处理是我国环保产业的重要分支。一种处理钢厂酸洗废水(含Fe3+、Fe2+、Al3+等)的工艺流程如下图所示:
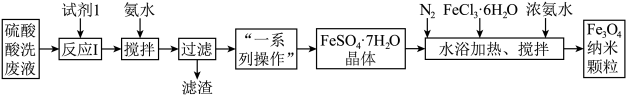
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
回答下列问题:
(1)反应I的离子方程式为___________ 。
(2)加入少量氨水的目的是调节pH,操作时需控制pH值的范围为___________ 。
(3)通入N2的目的是___________ 。
(4)制备Fe3O4纳米颗粒的离子方程式为___________ 。
(5)如何检验硫酸酸洗废液中是否含有Fe2+?___________
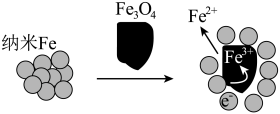
(6)纳米Fe和Fe3O4均可将Cr(Ⅵ)还原为Cr(Ⅲ)从而降解含Cr2O 的酸性废水,实验证明Fe3O4纳米颗粒辅助纳米Fe去除Cr2O
的酸性废水,实验证明Fe3O4纳米颗粒辅助纳米Fe去除Cr2O 的效果更佳,结合下图,分析其原因:
的效果更佳,结合下图,分析其原因:___________ 。
(7)将酸洗废液进行如下实验,检测废液中铁元素含量是否符合国家排放标准。
实验步骤:取100 ml酸洗废液,向其中滴加过量H2O2,微热;用淀粉作指示剂,滴加足量碘化钾至溶液变蓝;最后滴加 0.002 mol/L的硫代硫酸钠溶液至无色,消耗硫代硫酸钠溶液体积为12.7 ml。
已知:I2+2S2O =S4O
=S4O +2I-。废液中铁元素的物质的量浓度为
+2I-。废液中铁元素的物质的量浓度为 ___________ (保留至小数点后两位)。

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)反应I的离子方程式为
(2)加入少量氨水的目的是调节pH,操作时需控制pH值的范围为
(3)通入N2的目的是
(4)制备Fe3O4纳米颗粒的离子方程式为
(5)如何检验硫酸酸洗废液中是否含有Fe2+?
(6)纳米Fe和Fe3O4均可将Cr(Ⅵ)还原为Cr(Ⅲ)从而降解含Cr2O
 的酸性废水,实验证明Fe3O4纳米颗粒辅助纳米Fe去除Cr2O
的酸性废水,实验证明Fe3O4纳米颗粒辅助纳米Fe去除Cr2O 的效果更佳,结合下图,分析其原因:
的效果更佳,结合下图,分析其原因:
(7)将酸洗废液进行如下实验,检测废液中铁元素含量是否符合国家排放标准。
实验步骤:取100 ml酸洗废液,向其中滴加过量H2O2,微热;用淀粉作指示剂,滴加足量碘化钾至溶液变蓝;最后滴加 0.002 mol/L的硫代硫酸钠溶液至无色,消耗硫代硫酸钠溶液体积为12.7 ml。
已知:I2+2S2O
 =S4O
=S4O +2I-。废液中铁元素的物质的量浓度为
+2I-。废液中铁元素的物质的量浓度为
您最近一年使用:0次



