1 .  为阿伏加德罗常数的值。利用反应
为阿伏加德罗常数的值。利用反应 可以制备磁性氧化铁。下列叙述正确的是
可以制备磁性氧化铁。下列叙述正确的是
 为阿伏加德罗常数的值。利用反应
为阿伏加德罗常数的值。利用反应 可以制备磁性氧化铁。下列叙述正确的是
可以制备磁性氧化铁。下列叙述正确的是A.0.8mol 完全反应时生成氧化产物的分子数为 完全反应时生成氧化产物的分子数为 |
B.标准状况下,生成2.24L 时转移电子数目为 时转移电子数目为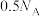 |
| C.上述反应中,氧化剂与还原剂的物质的量之比为16:1 |
D.生成1.1mo 时,参加反应的 时,参加反应的 中阴离子数目为 中阴离子数目为 |
您最近一年使用:0次
2010·海南·一模
2 . Fe2O3和Cu2O都是砖红色粉末,课外小组通过实验探究某砖红色粉末是Fe2O3、Cu2O或者是二者混合物。探究过程如下:
查阅资料:Cu2O是碱性氧化物,Cu2O与H+反应生成的Cu+不稳定,立即转化成Cu2+和Cu。提出假设:假设1:红色粉末是Fe2O3;假设2:红色粉末是Cu2O;假设3:红色粉末为Fe2O3、Cu2O的混合物
设计探究实验:
取少量粉末,向其加入足量稀盐酸在所得溶液中滴加苯酚溶液
(1)若假设1成立,则实验现象是__________ 。
(2)若滴加苯酚后溶液不变紫色,则证明原固体粉末不含Fe2O3。你认为结论是否合理______ (填“合理”或“不合理”),简述理由___________ 。
(3)若固体粉末完全溶解无固体存在,滴加苯酚时溶液不变紫色,证明原固体粉末是_____ ,相关的离子方程式为______________ 。(任写其中一个)
查阅资料:Cu2O是碱性氧化物,Cu2O与H+反应生成的Cu+不稳定,立即转化成Cu2+和Cu。提出假设:假设1:红色粉末是Fe2O3;假设2:红色粉末是Cu2O;假设3:红色粉末为Fe2O3、Cu2O的混合物
设计探究实验:
取少量粉末,向其加入足量稀盐酸在所得溶液中滴加苯酚溶液
(1)若假设1成立,则实验现象是
(2)若滴加苯酚后溶液不变紫色,则证明原固体粉末不含Fe2O3。你认为结论是否合理
(3)若固体粉末完全溶解无固体存在,滴加苯酚时溶液不变紫色,证明原固体粉末是
您最近一年使用:0次



