名校
1 . 甲醛与新制氢氧化铜反应的产物随反应条件改变而有所不同。实验室对该反应在一定条件下所得产物成分进行探究,具体过程如下。
取一定量的NaOH溶液、CuSO4溶液和甲醛于锥形瓶,控制温度40-50℃回流1h,收集到大量气体X,并有红色沉淀生成。
(1)①“控制温度40-50℃”的常用加热方法是___ 。
②气体X能燃烧且完全燃烧产物不会使澄清石灰水变军浊,说明该气体是___ 。
(2)在探究甲醛的氧化产物时,发现未生成CO 。为了进一步确定甲醛是否被氧化为HCOONa,进行如图实验(如图省略夹持和加热装置,甲酸与浓硫酸反应能生成CO,而CO可将银氨溶液还原成银单质)。
。为了进一步确定甲醛是否被氧化为HCOONa,进行如图实验(如图省略夹持和加热装置,甲酸与浓硫酸反应能生成CO,而CO可将银氨溶液还原成银单质)。

①仪器a的名称是___ 。
②b中,NaOH溶液的作用是___ 。
③c中,银氨溶液中出现黑色沉淀,则氧化剂与还原剂的物质的量之比为___ 。
(3)已知:2NH3+Cu+ [Cu(NH3)2]+(无色),[Cu(NH3)2]+遇空气容易被氧化成[Cu(NH3)4]2+(蓝色);验证红色沉淀中含Cu2O,进行如下实验步骤和现象记录:取样品,
[Cu(NH3)2]+(无色),[Cu(NH3)2]+遇空气容易被氧化成[Cu(NH3)4]2+(蓝色);验证红色沉淀中含Cu2O,进行如下实验步骤和现象记录:取样品,___ ,说明红色固体中含Cu2O。
(4)若最终测得沉淀中Cu单质和气体产物物质的量比为1:1,该条件下甲醛与新制氢氧化铜发生的主要反应化学方程式为___ 。
取一定量的NaOH溶液、CuSO4溶液和甲醛于锥形瓶,控制温度40-50℃回流1h,收集到大量气体X,并有红色沉淀生成。
(1)①“控制温度40-50℃”的常用加热方法是
②气体X能燃烧且完全燃烧产物不会使澄清石灰水变军浊,说明该气体是
(2)在探究甲醛的氧化产物时,发现未生成CO
 。为了进一步确定甲醛是否被氧化为HCOONa,进行如图实验(如图省略夹持和加热装置,甲酸与浓硫酸反应能生成CO,而CO可将银氨溶液还原成银单质)。
。为了进一步确定甲醛是否被氧化为HCOONa,进行如图实验(如图省略夹持和加热装置,甲酸与浓硫酸反应能生成CO,而CO可将银氨溶液还原成银单质)。
①仪器a的名称是
②b中,NaOH溶液的作用是
③c中,银氨溶液中出现黑色沉淀,则氧化剂与还原剂的物质的量之比为
(3)已知:2NH3+Cu+
 [Cu(NH3)2]+(无色),[Cu(NH3)2]+遇空气容易被氧化成[Cu(NH3)4]2+(蓝色);验证红色沉淀中含Cu2O,进行如下实验步骤和现象记录:取样品,
[Cu(NH3)2]+(无色),[Cu(NH3)2]+遇空气容易被氧化成[Cu(NH3)4]2+(蓝色);验证红色沉淀中含Cu2O,进行如下实验步骤和现象记录:取样品,(4)若最终测得沉淀中Cu单质和气体产物物质的量比为1:1,该条件下甲醛与新制氢氧化铜发生的主要反应化学方程式为
您最近一年使用:0次
2 . 硫酸铜是一种常见的化工产品,它在纺织、印染、 医药、化工、电镀以及木材和纸张的防腐等方面有极其广泛的用途。实验室制备硫酸铜的步骤如下:
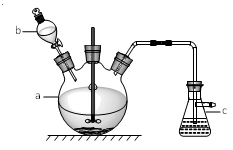
①在仪器a中先加入20 g铜片、60 mL水,再缓缓加入 17 mL浓硫酸;在仪器b中加入39 mL浓硝酸;在仪器c中 加入20%的石灰乳150 mL。
②从仪器b中放出约5 mL浓硝酸,开动搅拌器,然后采用滴加的方式逐渐将浓硝酸加到仪器a中,搅拌器间歇开动。当最后一滴浓硝酸加完以后,完全开动搅拌器,等反应基本停止下来时,开始用电炉加热直至仪器a中的红棕色气体完全消失,立即将导气管从仪器c中取出,再停止加热
③将仪器a中的液体倒出,取出未反应完的铜片,溶液冷却至室温,析出蓝色晶体。
试回答下列问题:
(1)仪器b的名称为_______ ;
(2)写出仪器a中反应的离子方程式:____________________ 。
(3)步骤②中将导气管先从仪器c中取出再停止加热的目的是_______________ 。
(4)为提高尾气吸收,防止空气污染,下列装置___________ (填字母)适合吸收逸出的气体(反应中产生的气体因来不及被石灰乳吸收而逸出)。

(5)根据表中五水硫酸铜和硝酸铜在不同温度下的溶解度,分析步骤③中溶液冷却至室温析出蓝色晶体的主要原因:___________ 。除去硫酸铜晶体中的少量硝酸铜可采用重结晶方法,检验硝酸铜是否被除净的方法:__________________ 。
(6)用滴定法测定蓝色晶体中Cu2+的含量。取a g试样配成 100 mL 溶液,每次取 20. 00 mL,用 c mol • L-1 EDTA (H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液bmL。 滴定反应为Cu2++ H2Y2-→CuY2-+2H+。计算蓝色晶体中Cu2+质量分数w=____ 。

①在仪器a中先加入20 g铜片、60 mL水,再缓缓加入 17 mL浓硫酸;在仪器b中加入39 mL浓硝酸;在仪器c中 加入20%的石灰乳150 mL。
②从仪器b中放出约5 mL浓硝酸,开动搅拌器,然后采用滴加的方式逐渐将浓硝酸加到仪器a中,搅拌器间歇开动。当最后一滴浓硝酸加完以后,完全开动搅拌器,等反应基本停止下来时,开始用电炉加热直至仪器a中的红棕色气体完全消失,立即将导气管从仪器c中取出,再停止加热
③将仪器a中的液体倒出,取出未反应完的铜片,溶液冷却至室温,析出蓝色晶体。
试回答下列问题:
(1)仪器b的名称为
(2)写出仪器a中反应的离子方程式:
(3)步骤②中将导气管先从仪器c中取出再停止加热的目的是
(4)为提高尾气吸收,防止空气污染,下列装置

(5)根据表中五水硫酸铜和硝酸铜在不同温度下的溶解度,分析步骤③中溶液冷却至室温析出蓝色晶体的主要原因:
T/K | 273 | 293 | 313 | 333 | 353 | 373 | |
溶解度/ (g/100 g) | 五水硫酸铜 | 23.1 | 32.0 | 44.6 | 61.8 | 83.8 | 114.0 |
硝酸铜 | 83.5 | 125.0 | 163.0 | 182.0 | 208.0 | 247.0 | |
您最近一年使用:0次



