1 . 某工厂的固体废渣中主要含Cu和CuO,还含有少量Cu2O和SiO2。利用该固体废渣制取Cu(NO3)2溶液的工艺流程如图所示:
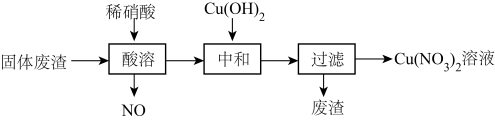
已知:①Cu+在酸性溶液中不稳定,会转变成Cu和Cu2+。
②SiO2是酸性氧化物,难于水和酸。
(1)写出Cu2O与稀硝酸反应的离子反应方程式为___________ ;
(2)酸溶时,反应温度不宜超过70℃,其主要原因是___________ ;
(3)将酸溶步骤排放的NO循环利用既环保又能提高产量,具体操作流程是___________ ;
(4)酸溶试剂改用绿色氧化剂(10%H2O2和20%稀硝酸的混合液),基本无氮氧化物排放,写出废渣中Cu与绿色氧化剂反应的离子反应方程式___________ ;
(5)中和试剂选择Cu(OH)2,若改为NaOH,缺点是___________ ;
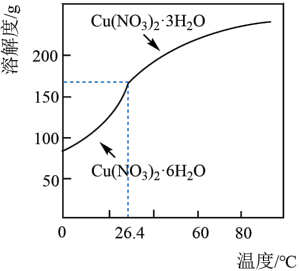
(6)以某工业废水(主要含Cu2+、Na+、SO )为原料,设计制取Cu(NO3)2·3H2O晶体的实验方案:向工业废水中加入
)为原料,设计制取Cu(NO3)2·3H2O晶体的实验方案:向工业废水中加入___________ ,洗涤,干燥。(须使用的试剂有:蒸馏水、1mol/L NaOH溶液、1mol/LHNO3溶液;Cu(NO3)2的溶解度曲线如图所示。)

已知:①Cu+在酸性溶液中不稳定,会转变成Cu和Cu2+。
②SiO2是酸性氧化物,难于水和酸。
(1)写出Cu2O与稀硝酸反应的离子反应方程式为
(2)酸溶时,反应温度不宜超过70℃,其主要原因是
(3)将酸溶步骤排放的NO循环利用既环保又能提高产量,具体操作流程是
(4)酸溶试剂改用绿色氧化剂(10%H2O2和20%稀硝酸的混合液),基本无氮氧化物排放,写出废渣中Cu与绿色氧化剂反应的离子反应方程式
(5)中和试剂选择Cu(OH)2,若改为NaOH,缺点是
(6)以某工业废水(主要含Cu2+、Na+、SO
 )为原料,设计制取Cu(NO3)2·3H2O晶体的实验方案:向工业废水中加入
)为原料,设计制取Cu(NO3)2·3H2O晶体的实验方案:向工业废水中加入
您最近一年使用:0次
2 . 某铜矿石的主要成分为Cu2O,还含有少量Al2O3、Fe2O3、SiO2。工业上用该矿石获取铜和胆矾的操作流程如下:
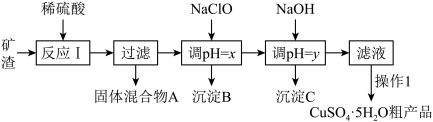
已知:①Cu2O+2H+=Cu+Cu2++H2O
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)实际生产中将矿石粉碎为矿渣的目的是___________ 。
(2)固体混合物A中含有较多的铜,加入某试剂可以提纯铜。该反应的离子方程式为___________ 。
(3)反应Ⅰ完成后的滤液中铁元素的存在形式为___________ (填离子符号),检验该离子常用的试剂为___________ ,生成该离子的离子方程式为___________ 。
(4)加入NaClO调节溶液pH可生成沉淀B,利用题中所给信息,沉淀B为___________ ,该反应中氧化剂与还原剂物质的量之比为___________ 。
(5)加入NaOH调节pH,得到沉淀C,利用题中所给信息分析y的范围___________ 。
(6)操作1主要包括:蒸发浓缩、冷却结晶、过滤、 冷水洗涤得到CuSO4·5H2O。如何洗涤CuSO4·5H2O粗品___________ 。

已知:①Cu2O+2H+=Cu+Cu2++H2O
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 5.4 | 4.0 | 2.7 | 5.8 |
| 沉淀完全的pH | 6.7 | 5.2 | 3.7 | 8.8 |
(1)实际生产中将矿石粉碎为矿渣的目的是
(2)固体混合物A中含有较多的铜,加入某试剂可以提纯铜。该反应的离子方程式为
(3)反应Ⅰ完成后的滤液中铁元素的存在形式为
(4)加入NaClO调节溶液pH可生成沉淀B,利用题中所给信息,沉淀B为
(5)加入NaOH调节pH,得到沉淀C,利用题中所给信息分析y的范围
(6)操作1主要包括:蒸发浓缩、冷却结晶、过滤、 冷水洗涤得到CuSO4·5H2O。如何洗涤CuSO4·5H2O粗品
您最近一年使用:0次
2023-04-17更新
|
261次组卷
|
2卷引用:黑龙江省哈尔滨市第四中学校2022-2023学年高一下学期4月月考化学试题
3 . 工业上由含铜废料(含有Cu、CuS、 等)制备硝酸铜晶体的流程如下:
等)制备硝酸铜晶体的流程如下:
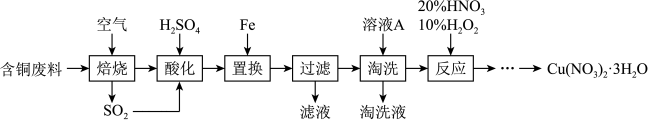
(1)写出CuS“焙烧”生成 和CuO的化学反应方程式:
和CuO的化学反应方程式:___________ 。
(2)图中 经转化生成的硫酸可用于“酸化”,该转化过程中若有2mol
经转化生成的硫酸可用于“酸化”,该转化过程中若有2mol  与1mol
与1mol  充分反应,所得生成物的分子数
充分反应,所得生成物的分子数___________ (填“大于2 ”、“等于2
”、“等于2 ”或“小于2
”或“小于2 ”)。
”)。 属于
属于___________ (填“酸性”或“碱性”)氧化物。
(3)“过滤”所得的滤液中溶质的主要成分为___________ 。
(4)“淘洗”所用的溶液A应选用___________ (填序号)
a.稀硫酸 b.浓硫酸 c.稀硝酸 d.浓硝酸
(5)“反应”步骤中,10% 为氧化剂,20%
为氧化剂,20%  提供
提供 ,可以避免污染性气体的产生。写出该反应的离子方程式:
,可以避免污染性气体的产生。写出该反应的离子方程式:___________ 。
(6)有一份氧化铁、氧化铜和铁粉组成的混合物,将其投入到3mol/L 200mL的盐酸中,充分反应后,产生标准状况下的 896mL,溶液呈现浅绿色,剩余固体1.28g。过滤,将滤液稀释到300mL,经测定溶液中
896mL,溶液呈现浅绿色,剩余固体1.28g。过滤,将滤液稀释到300mL,经测定溶液中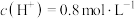 。则原混合物中铁粉的物质的量为
。则原混合物中铁粉的物质的量为___________ 。
 等)制备硝酸铜晶体的流程如下:
等)制备硝酸铜晶体的流程如下:
(1)写出CuS“焙烧”生成
 和CuO的化学反应方程式:
和CuO的化学反应方程式:(2)图中
 经转化生成的硫酸可用于“酸化”,该转化过程中若有2mol
经转化生成的硫酸可用于“酸化”,该转化过程中若有2mol  与1mol
与1mol  充分反应,所得生成物的分子数
充分反应,所得生成物的分子数 ”、“等于2
”、“等于2 ”或“小于2
”或“小于2 ”)。
”)。 属于
属于(3)“过滤”所得的滤液中溶质的主要成分为
(4)“淘洗”所用的溶液A应选用
a.稀硫酸 b.浓硫酸 c.稀硝酸 d.浓硝酸
(5)“反应”步骤中,10%
 为氧化剂,20%
为氧化剂,20%  提供
提供 ,可以避免污染性气体的产生。写出该反应的离子方程式:
,可以避免污染性气体的产生。写出该反应的离子方程式:(6)有一份氧化铁、氧化铜和铁粉组成的混合物,将其投入到3mol/L 200mL的盐酸中,充分反应后,产生标准状况下的
 896mL,溶液呈现浅绿色,剩余固体1.28g。过滤,将滤液稀释到300mL,经测定溶液中
896mL,溶液呈现浅绿色,剩余固体1.28g。过滤,将滤液稀释到300mL,经测定溶液中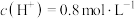 。则原混合物中铁粉的物质的量为
。则原混合物中铁粉的物质的量为
您最近一年使用:0次



